INTRODUCCIÓN
La fibrilación auricular (FA) es la arritmia cardíaca sostenida más común en adultos, con una prevalencia que se encuentra en aumento a lo largo de las últimas décadas debido al envejecimiento poblacional y al aumento de la sobrevida de otras condiciones cardíacas. (1) Se asocia con un mayor riesgo de eventos tromboembólicos, (2) deterioro cognitivo, (3) insuficiencia cardíaca, hospitalizaciones y muerte. (4)
A su vez, es la complicación arrítmica más frecuente en pacientes con síndrome coronario agudo (SCA), con una incidencia de entre 2,3 y 21%. (5) En Argentina tenemos en este contexto una incidencia de FA de novo del 3,2%, observada en el registro ARGEN-IAM-ST. (6) A lo largo de las últimas décadas y con el avance del tratamiento invasivo y médico, su incidencia parecería haber disminuido. (6) Múltiples estudios han evaluado las características clínicas de los pacientes que presentaron FA de novo posterior a un SCA. Se observó que los principales predictores fueron la edad avanzada, la presencia de signos de insuficiencia cardíaca y la taquicardia al ingreso hospitalario. Estos predictores se han sostenido tanto en estudios realizados en la era fibrinolítica como en la actualidad, con la disponibilidad del tratamiento percutáneo.
Tanto en la población general como en los pacientes que cursan un SCA, la presencia de FA se asocia con peor pronóstico. Cuando la FA se desarrolla de novo dentro del marco de un SCA se asocia a mayor morbimortalidad. (9,10) A su vez, múltiples estudios observacionales han evidenciado que los pacientes en los que coexisten un SCA y FA de novo tienen menos chances de recibir tratamiento antitrombótico apropiado. (11,12) Sin embargo, faltan estudios que analicen predictores y pronóstico de estos pacientes dentro del marco del tratamiento invasivo y médico recomendado por las últimas guías.
Los objetivos de este estudio fueron evaluar la incidencia de FA de novo durante la internación por un infarto agudo de miocardio con elevación del segmento ST (IAMCEST) y determinar predictores asociados con su desarrollo.
MATERIAL Y MÉTODOS
Diseño y población del estudio
Se trata de un estudio observacional y retrospectivo a partir del análisis del registro continuo de Infarto agudo de miocardio con elevación del segmento ST (ARGEN-IAM-ST), que incluye pacientes con IAMCEST de numerosos centros de la República Argentina. Su protocolo fue publicado previamente, y se encuentra activo desde el año 2015. (13,14) El protocolo fue registrado en ClinicalsTrials.gov NCT 2458885. Se realizó un corte para el análisis de este trabajo hasta mayo del 2024.
Definiciones y desenlace de interés
Nuestro desenlace de interés fue la FA de novo durante la internación. La definimos como FA en aquellos pacientes que se habían presentado a su ingreso con un electrocardiograma (ECG) en ritmo sinusal y que durante su evolución presentaron como complicación un episodio de FA. La misma fue modelada como una variable binaria. Excluimos de esta definición a aquellos pacientes que presentaban como antecedente FA y aleteo auricular.
Análisis estadístico
Las variables continuas se expresan como media y desviación estándar (DE) o mediana y rango intercuartílico (RIC), según su tipo de distribución. Las variables edad y frecuencia cardíaca fueron analizadas por estratos. Las variables cualitativas se expresan como frecuencias absolutas y relativas. Las variables cualitativas se compararon mediante la prueba de chi cuadrado o la prueba exacta de Fisher, mientras que las variables continuas con distribución paramétrica y no paramétrica se compararon mediante la prueba de t de Student y la prueba de la U de Mann Whitney, respectivamente.
Para reducir la dimensionalidad e identificar aquellas variables asociadas con nuestro desenlace de interés, se utilizó el algoritmo de Machine Learning Boruta. (15) Para garantizar que la selección de variables fuera estable y reproducible, el algoritmo realizó hasta 50 iteraciones, permitiendo evaluar de manera robusta la importancia de cada predictor en la clasificación de FA de novo. Además, se monitoreó su desempeño durante el proceso para verificar la coherencia en la selección de características. Con aquellas variables de mayor peso se realizó análisis multivariable por medio de regresión logística para identificar los factores asociados de manera independiente a la presencia de FA de novo. Los modelos fueron entrenados y testeados en dos bases de datos distintas generadas de forma aleatoria a partir de la base de datos general. El desempeño de los modelos y su capacidad de discriminación fue evaluada a través de la generación de curvas ROC (Receiver Operating Characteristic). Dado que el objetivo del modelo fue maximizar la sensibilidad para identificar la mayor cantidad de casos de FA de novo, se seleccionó el punto de corte óptimo a partir de la curva ROC con el criterio de mayor sensibilidad posible, manteniendo una especificidad clínicamente aceptable. Para evaluar la bondad de ajuste del modelo se utilizó la prueba de Hosmer Lemeshow. La asociación entre los predictores y la incidencia de eventos se expresó como Odds ratio (OR) con sus intervalos de confianza del 95% (IC 95%). Además, se realizó un modelo multivariable para explorar la FA de novo como predictor independiente de mortalidad. Todas las pruebas fueron a dos colas y la significación estadística se estableció en un valor de p <0,05.
El análisis se realizó con R Studio, versión 1.4.1106 (The R Foundation for Statistical Computing, Viena, Austria).
Consideraciones éticas
El protocolo del registro Argen IAM-ST fue aprobado por el comité de ética de la Sociedad Argentina de Cardiología.
RESULTADOS
Características basales de la población
Se incluyeron en total 7292 pacientes que presentaron IAMCEST y evidencia de ritmo sinusal en el ECG de ingreso, de los cuales el 79% pertenecían al género masculino, con una mediana (RIC) de edad de 61 (53-69) años. Las características basales se muestran en la Tabla 1.
Tabla 1:
Características Clínicas Basales de los Participantes con y sin FA de novo
| Global | No FA de novo | FA de novo | p | |
|---|---|---|---|---|
| n | 7292 | 6974 | 318 | |
| Género Masculino, n (%) | 5754 (79) | 5512 (79) | 248 (78) | 0,705 |
| Edad, años, mediana (RIC) | 61 (53-69) | 60 (53-68) | 67(60-77) | <0,001 |
| IMC, kg/m2, mediana (RIC) | 27,65 | 27,68 | 27,41 | 0,041 |
| (25,47-30,61) | (25,51-30,76) | (25,28-29,97) | ||
| DM, n (%) | 1980 (27,2) | 1900 (27,2) | 80 (25,2) | 0,451 |
| TBQ, n (%) | 591 ( 8,1) | 563 ( 8,1) | 28 ( 8,8) | 0,717 |
| DLP, n (%) | 2662 (36,5) | 2553 (36,6) | 109 (34,3) | 0,433 |
| HTA, n (%) | 3870 (53,1) | 3661 (52,5) | 209 (65,7) | <0,001 |
| Enfermedad coronaria previa, n (%) | 897 (12,3) | 846 (12,1) | 51 (16,0) | 0,047 |
| Betabloqueantes, n (%) | 3635 (50,0) | 3519 (50,5) | 120 (37,7) | <0,001 |
| IECA, n (%) | 3301 (45,4) | 3178 (45,6) | 129 (40,6) | 0,090 |
| Glucemia, mg/dL, mediana (RIC) | 135 (113-179) | 134 (113-177) | 153 (124-212,50) | <0,001 |
| Creatinina, mg/dL, mediana (RIC) | 0,97 (0,80-1,18) | 0,97 (0,80-1,17) | 1,08 (0,90-1,40) | <0,001 |
| Motivo de la ATC, n (%) | 0,949 | |||
| Primaria | 5003 (91,1) | 4887 (70,1) | 207 (65,1) | |
| Fármaco invasiva | 273 (5,0) | 646 (9,3) | 37 (11,6) | |
| Rescate | 154 (2,8) | 976 (14,0) | 45 (14,2) | |
| Electiva | 59 (1,1) | 465 (6,7) | 29 (9,1) | |
| TAS, mm Hg, media (DE) | 131 (29) | 132 (29) | 121 (29) | <0,001 |
| FC, lpm, media (DE) | 80 (19) | 80 (18) | 86 (26) | <0,001 |
| Killip y Kimball, n (%) | <0,001 | |||
| A | 5485 (77,0) | 5456 (78,2) | 153 (48,1) | |
| B | 1024 (14,4) | 955 (13,7) | 90 (28,3) | |
| C | 100 (1,4) | 95 (1,4) | 8 (2,5) | |
| D | 516 (7,2) | 468 (6,7) | 67 (21,1) | |
| Tiempo puerta-balón, min, mediana (RIC) | 84 (47-147) | 91 (50, 175) | 92 (51,25- 209,75) | 0,439 |
| Tiempo ventana, min, mediana (RIC) | 230 | 252,50 | 289,50 | |
| (135-440) | (146-510) | (162,25- 612,25) | 0,019 | |
| ATC a múltiples vasos en procedimiento inicial, n (%) | 351 (6,4) | 360 (5,2) | 26 (8,2) | 0,026 |
| FSVI, n (%) | <0,001 | |||
| Normal | 2397 (37,4) | 2660 (38,1) | 75 (23,6) | |
| Deterioro leve | 1842 (28,7) | 1994 (28,6) | 58 (18,2) | |
| Deterioro moderado | 1397 (21,8) | 1466 (21,0) | 93 (29,2) | |
| Deterioro grave | 774 (12,1) | 854 (12,2) | 92 (28,9) |
ATC: angioplastia transluminal coronaria; DE: desviación estándar; DM: diabetes mellitus; DLP: dislipidemia; FA: fibrilación auricular; FC: frecuencia cardíaca; FSVI: función sistólica del ventrículo izquierdo; HTA: hipertensión arterial; IECA: inhibidores de la enzima convertidora de angiotensina; IMC: índice de masa corporal; lpm: latidos por minuto; RIC: rango intercuartílico; TAS: tensión arterial sistólica; TBQ: tabaquismo
Se identificó que el 4,3% de la muestra presentó FA de novo durante la internación. Estos pacientes eran mayores que aquellos que permanecieron libres de FA (mediana de edad de 67 vs. 60 años; p <0,001). No encontramos diferencias entre los grupos respecto del índice de masa corporal (IMC), diabetes mellitus y dislipidemia. Sin embargo, el 53,1% presentaba hipertensión arterial (HTA), con mayor prevalencia en el grupo de pacientes que evolucionó con FA durante la internación (65,7% vs. 52,5%; p <0,001). A su vez, el antecedente de enfermedad coronaria, presente en el 12,3% de la muestra total, también fue más frecuente en el grupo con FA de novo (16% vs. 12,1%; p = 0,047).
En cuanto a las estrategias de reperfusión, en el 91% del total de pacientes se realizó angioplastia primaria, en el 5% estrategia farmacoinvasiva, en el 2,8% angioplastia de rescate y en el 1,1% angioplastia electiva, sin diferencias significativas entre los grupos de estudio. Sin embargo, se realizó angioplastia a múltiples vasos en el procedimiento inicial en mayor proporción en los pacientes que evolucionaron con FA durante la internación. No se evidenciaron diferencias significativas en cuanto al tratamiento del vaso culpable del IAM.
En cuanto al tratamiento con betabloqueantes e inhibidores de la enzima convertidora al ingreso, encontramos un menor uso de estos en aquellos pacientes con FA de novo: 50% vs. 37% (p = 0,001) y 45% vs. 40% (p = 0,090) respectivamente.
Al ingreso hospitalario, aquellos pacientes que evolucionaron con FA presentaban mayor frecuencia cardíaca (86 lpm vs. 80 lpm; p <0,001) y, en el laboratorio, mayores valores de glucemia, con mediana (RIC) de 153 mg/dL (124-212) vs. 134 mg/dL (113-177), p<0,001, y de creatinina: 1,08 mg/dL (0,90-1,40) vs. 0,97 mg/dL (0,8-1,17), p<0,001.
Este grupo de pacientes también presentó mayor tiempo de isquemia total (medianas de 289 min vs. 252 min; p=0,019), un score de Killip y Kimball más grave (p<0,001) y una menor fracción de eyección del ventrículo izquierdo (FEVI) (p <0,001).
Eventos intrahospitalarios
La presencia de FA de novo se asoció con una mayor incidencia de accidente cerebrovascular (ACV) isquémico (2,5% vs. 0,8%; p = 0,002) y más días de internación (medianas de 6 vs. 4 días; p <0,001). En relación con la muerte intrahospitalaria por todas las causas también fue mayor en el grupo con FA de novo (23,3% vs. 8,2%; p <0,001) (Tabla 2)
Tabla 2:
Eventos intrahospitalarios de los participantes con y sin FA de novo
| Global | No FA de novo | FA de novo | p | |
|---|---|---|---|---|
| n | 7292 | 6974 | 318 | |
| ReIAM, n (%) | 123 (1,7) | 113 (1,6) | 10 (3,1) | 0,066 |
| ACV, n (%) | 61 (0,8) | 53 (0,8) | 8 (2,5) | 0,002 |
| Shock cardiogénico, n (%) | 682 (9,4) | 576 (8,3) | 106 (33,3) | <0,001 |
| IC, n (%) | 967 (13,3) | 818 (11,7) | 149 (46,9) | <0,001 |
| Muerte hospitalaria, n (%) | 591 (8,1) | 563 (8,1) | 28 (8,8) | 0,717 |
| Días de internación, mediana (RIC) | 4 (3- 6) | 4 (3-6) | 6 (4-11) | <0,001 |
ACV: accidente cerebrovascular; FA: fibrilación auricular; IC: insuficiencia cardíaca; RIC: rango intercuartílico; ReIAM: reinfarto
Selección de variables relevantes
Mediante el algoritmo Boruta se realizó una selección automatizada con el objetivo de identificar las variables con mayor relevancia en la predicción de FA de novo. En el análisis, las variables Killip y Kimball, frecuencia cardíaca y FEVI, se identificaron como las de mayor importancia, seguidas por género, edad, dislipidemia y creatinina. En laFigura 1, se presentan las medias de importancia de cada variable en el ranking obtenido. Posteriormente, estas variables fueron incluidas en el modelo de regresión logística multivariable para evaluar su asociación con el desenlace.
Fig. 1
Importancia de las variables predictoras de FA de novo
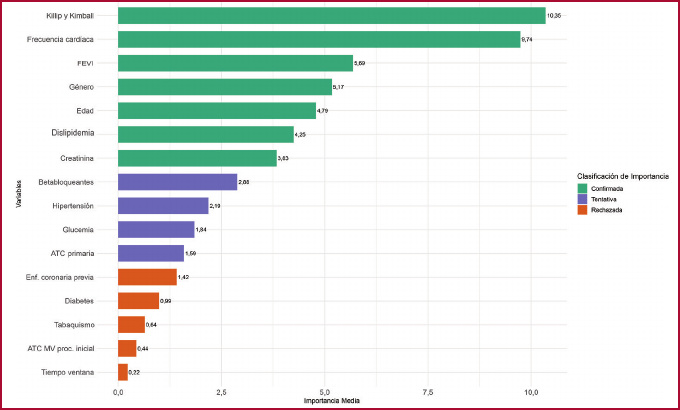
FEVI: fracción de eyección del ventrículo izquierdo; MV: múltiples vasos; proc: procedimiento; Tiempo ventana: tiempo en minutos desde el inicio de los síntomas hasta el comienzo de la infusión en el caso de fibrinolíticos o hasta el insuflado del balón en el caso de ATC.
Análisis multivariable. Predictores independientes de FA de novo
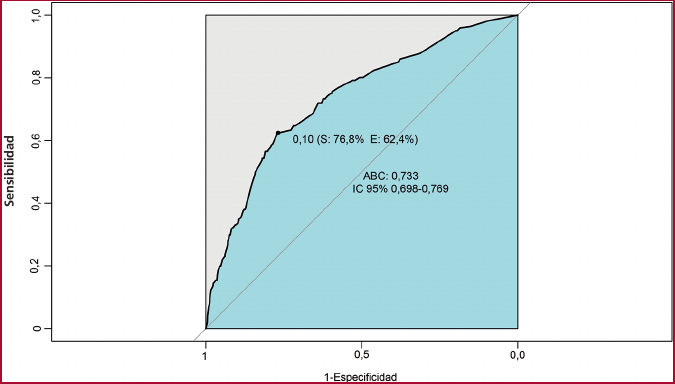
Aquellas variables de mayor peso asociadas a presencia de FA de novo fueron incluidas en un modelo multivariable de regresión logística. La variable edad estratificada (50 a 59 años, 60 a 69 años y 70 a 100 años) se asoció independientemente a incidencia de FA de novo (OR 1,72, IC95% 1,11-2,73; OR 1,77, IC95% 1,07-2,96; OR 3,98, IC95% 2,60-6,25 respectivamente). También fueron predictores independientes la presentación clínica según el score Killip y Kimball (B: OR 1,72, IC95% 1,19-2,46; C: OR 1,09, IC95% 0,315-2,90; D: OR 2,48, IC95%1,60-3,78), la presencia de taquicardia (OR 2,41, IC95% 1,74-3,31) y una FEVI deteriorada (<35%) (OR 1,62, IC95% 1,04-2,50) (Figura 2). Para evaluar el rendimiento del modelo, se construyó una curva ROC, obteniendo un área bajo la curva (ABC) de 0,733 (IC 95% 0,698-0,769). Se determinó el punto de corte óptimo en 0,10, seleccionado con el objetivo de maximizar la sensibilidad. Con este umbral, el modelo identificó correctamente el 77% de los pacientes con FA de novo (sensibilidad) y el 62% de los pacientes sin FA de novo (especificidad). Este punto de corte representa el umbral donde el balance entre sensibilidad y especificidad resulta clínicamente más adecuado para la detección de FA de novo (Figura 3). La bondad de ajuste del modelo fue evaluada mediante el test de Hosmer-Lemeshow, que mostró un buen ajuste (χ² = 5,33, p = 0,618).
Fig. 2
Predictores de FA de novo
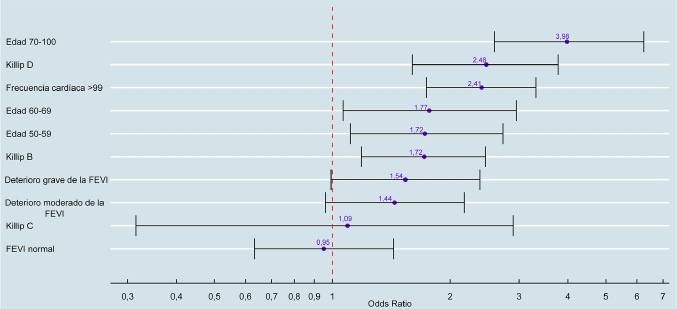
FA: fibrilación auricular ; FEVI: fracción de eyección ventricular izquierda
Análisis multivariable: FA de novo como predictor independiente de mortalidad
Se incluyó la FA de novo junto a las principales variables relacionadas con la mortalidad intrahospitalaria en un modelo multivariable. Se observó que la FA de novo no se comportó como predictor independiente de mortalidad intrahospitalaria (OR 0,79, IC95% 0,41-1,50) (Figura 4)
DISCUSIÓN
Se presentan los datos de incidencia de FA de novo durante la internación por IAMCEST del registro ARGEN-IAM-ST. En esta ocasión se excluyeron los casos con registro de FA en el ECG de ingreso o con antecedente de esta, para evaluar las consecuencias de este evento luego del IAM. La incidencia fue 4,3%, y los hallazgos sugieren una asociación con mayor número de eventos intrahospitalarios, así como una estancia hospitalaria más prolongada. Por otro lado, encontramos que ciertos factores como la edad, la presencia de insuficiencia cardíaca evaluada con el score Killip y Kimball, la taquicardia y el deterioro de la FEVI fueron predictores independientes de FA de novo durante la internación. Dichos predictores fueron incorporados en un modelo de clasificación para predecir FA de novo, que presentó un ABC de 0,733, (IC 95% 0,698-0,769)
La FA y el SCA son dos entidades cardiológicas frecuentes por lo que a lo largo de los años se han desarrollado múltiples estudios con el objetivo de analizar la relación entre ambas patologías. El riesgo de FA de novo aumenta un 60-77% en pacientes cursando un IAM. (16) En la era fibrinolítica, los estudios randomizados GUSTO-I (1997) y GUSTO-III (2000), compararon distintos esquemas fibrinolíticos en pacientes con IAMCEST, y destacaron una incidencia de FA de novo posterior a un SCA de 7,9% y 6,5% respectivamente. (8, 17) Por otro lado, en el año 2003, se publicó el estudio prospectivo observacional OACIS, que analizó pacientes con IAM (con y sin elevación del segmento ST) tratados con angioplastia percutánea coronaria dentro de las 24 h, en donde se observó una incidencia de FA de novo de 7,7%. (18) En cuanto a resultados nacionales, datos del registro Buenos Aires I, que incluía pacientes con síndrome coronario agudo sin elevación del segmento ST (SCASEST), demostraron una incidencia de FA de novo intrahospitalaria de 4,3% y 7,7% en pacientes con IAM y angina inestable, respectivamente. (19) De manera similar, en una publicación previa, el registro ARGEN-IAM-ST mostró una incidencia de FA de novo de 3,2%, y los factores predisponentes fueron la edad avanzada, el antecedente de HTA y la enfermedad coronaria previa. (6) Definitivamente no se cuenta con estudios aleatorizados que hayan comparado la incidencia de FA de novo en pacientes con IAMCEST tratado con fibrinolíticos vs. angioplastia primaria y las diferencias en las poblaciones y las metodologías de los estudios publicados impiden una correcta evaluación de la incidencia de esta complicación, y de si se ve afectada por el tipo de revascularización.
En nuestra cohorte, la edad se comportó como un predictor independiente de FA de novo. Específicamente en el estrato de edad de 70-100 años es donde observamos el mayor impacto, con un OR de 3,98. Al igual que la FA fuera del contexto de un SCA, la edad estuvo íntimamente relacionada con la incidencia de esta arritmia. En uno de los estudios con mayor número de pacientes, realizado a partir de la base de datos del Cooperative Cardiovascular Project publicado en el año 2000, (11) que incluyó únicamente pacientes ≥65 años, se observó que la tasa de FA de novo posterior a un SCA era del 22%, significativamente mayor a la de estudios que incluyeron pacientes de todas las edades. Adicionalmente, en la revisión realizada en el 2009 por Schmitt et al., se observó que todos los estudios publicados desde 1992 hasta el 2007 identificaron a la edad avanzada como predictor independiente de FA de novo posterior a un SCA. (20)
Si bien la FA es la arritmia supraventricular más frecuente en la población general, su incidencia es notablemente mayor en pacientes con insuficiencia cardíaca (IC). Estas dos patologías se relacionan estrechamente entre sí, y cada una perpetúa la presencia de la otra. (21) En nuestro análisis, pudimos observar que la presencia de IC evaluada a través del score Killip y Kimball se asoció de manera independiente con la presencia de FA de novo, al igual que en los estudios previamente mencionados GUSTO-I y III. Cabe destacar un subanálisis del estudio internacional GRACE, que incluyó más de
21 000 pacientes con SCA, clasificándolos según la presencia de FA de novo, FA previa y sin FA, el cual identificó a un score de Killip y Kimball ≥ 2 como predictor independiente de FA de novo. (22) De la misma forma, la presencia de taquicardia, probablemente secundaria a la presencia de IC, también fue un predictor de FA de novo en nuestro estudio y en el previamente mencionado. Estos resultados traducen el impacto del estado hemodinámico dentro de los mecanismos fisiopatológicos de la FA en el marco de un SCA, y señalan que un paciente con un estado hemodinámico alterado (IC, taquicardia y/o hipotensión) tiene mayor riesgo de presentar FA.
Paralelamente, el deterioro grave de la FEVI (<35%) también se comportó como predictor independiente de FA de novo en nuestro análisis. Si bien la asociación entre la disfunción ventricular y la presentación clínica al ingreso (reflejada en el score de Killip y Kimball y la frecuencia cardíaca) es clara, otros estudios no han evidenciado esta variable como predictor independiente de FA de novo.
LIMITACIONES
El registro ARGEN-IAM-ST es un registro de participación voluntaria sin estrategia de auditoría. Si bien se realizó análisis multivariable por regresión no podemos descartar por completo que haya variables no consideradas que hayan podido alterar nuestros resultados. Además, si bien se trata de un estudio multicéntrico, solo representa la realidad de los centros participantes. Por último, no podemos determinar el momento de la internación en el cual se produjo la FA, por lo cual no podemos estudiar la relación temporal de la misma.
CONCLUSIONES
En esta cohorte de pacientes del registro ARGEN-IAM-ST, la FA de novo fue una complicación relativamente frecuente. Factores como la edad, frecuencia cardíaca, el perfil hemodinámico al ingreso y la función ventricular mostraron ser predictores de una FA de novo en la internación por un IAM. Sin embargo, la FA de novo no se asoció de manera independiente con la mortalidad intrahospitalaria.
Declaración de conflicto de interés
Los autores declaran que no tienen conflicto de intereses. (Ver formulario de conflicto de intereses en la web)