INTRODUCCIÓN
La aurícula izquierda (AI) desempeña un papel importante en la fisiología cardíaca, y su volumen se ha asociado con diversas condiciones clínicas como fibrilación auricular, insuficiencia cardíaca y mayor riesgo cardiovascular. (1-3) Su medición volumétrica constituye, por este motivo, un parámetro esencial en estudios de imagen para la práctica clínica.
Los métodos más utilizados por ecocardiografía para estimar el volumen de la AI son: área-longitud (AL) y Simpson. (4,5) La resonancia magnética cardíaca (RMC) puede valerse de su observación global y en múltiples planos de la AI, y se pueden realizar estimaciones indirectas o una cuantificación directa, esta última la más precisa pero, a su vez, la más laboriosa. El método de AL fue el más utilizado en RMC desde el inicio, y sigue siendo el de elección en nuestro medio. (6-10) Más allá de su mayor simplicidad puede no reflejar con suficiente precisión la volumetría de la AI. Por su parte, la cuantificación directa del volumen de la AI requiere mayor cantidad de cortes para su adquisición en RMC con la consecuente prolongación del estudio y su análisis ulterior. (10-12)
OBJETIVOS
Proponer y validar un método alternativo para la estimación del volumen de la AI con RMC. Comparar la precisión y concordancia de este nuevo método con respecto al método AL, utilizando como patrón de verdad la cuantificación directa por trazado volumétrico completo de la AI en estudios de RMC.
MATERIAL Y MÉTODOS
Población de estudio
De una base de datos de imágenes de RMC de nuestro centro fueron seleccionados de modo aleatorio 25 pacientes de edad mayor a 18 años. Se excluyeron los pacientes que tuvieran una anatomía auricular compleja, como cardiopatía congénita con circulación de Fontan-Kreutzer, o mala calidad de imagen dada por artificio técnico, o que por algún motivo no hubieran completado la adquisición de las imágenes básicas deseadas para el análisis.
Protocolo de RMC
Las imágenes fueron adquiridas con un resonador Siemmens Magneton Aera 1.5 T. La adquisición de imagen fue realizada en decúbito supino, con gatillado por electrocardiografía retrospectiva. Dentro del protocolo básico de adquisición del centro se utilizan imágenes de cine dadas por secuencias de Steady-State Free Precession (SSFP) en las proyecciones de 2 cámaras (2C), 3 cámaras (3C), 4 cámaras (4C) y eje corto completo (ECC). En la adquisición del volumen completo en eje corto de ventrículos, por protocolo del centro se incluye el volumen de las aurículas en forma rutinaria.
Análisis de las imágenes
Todas las imágenes fueron analizadas con el programa gratuito disponible Segment v4.0 (Medviso, Lund, Suecia). Se realizaron 2 análisis independientes por dos investigadores con experiencia en el método. Todas las mediciones fueron realizadas en fin de sístole. Se cuantificó el volumen de la AI en forma directa por trazado manual con exclusión de la orejuela y las venas pulmonares sobre todos los cortes de la misma, y se asumió este como el valor real. Se realizó la estimación por el método habitual biplano de área-longitud (AL) y por el método nuevo propuesto del volumen de un cilindro con base irregular (CBI).
Para el método de AL se realizaron las mediciones de área y altura de la AI en la proyección de cines de 2C y 4C. Se utilizó la siguiente fórmula: 8/3π (área 2C x área 4C)/longitud.
Para el volumen del cilindro de base irregular se realizó la medición de la base del cilindro. Se trazó el área de la aurícula en un corte perpendicular a su eje mayor, dado en la adquisición del eje corto completo del volumen entre el orificio de la orejuela y la emergencia de las venas pulmonares; y se tomó la altura de la aurícula desde el anillo mitral hasta su techo en la proyección de 4 C. Se utilizó la fórmula área x altura para obtener el volumen.
Análisis estadístico
Las variables continuas se presentan como media ± desviación estándar (DE) o mediana y rango intercuartílico (RIC) según su distribución. Las variables categóricas se presentan como frecuencias y porcentajes. Se compararon ambas estimaciones contra el criterio de verdad (volumetría directa) midiendo su correlación simple (r de Pearson). Se realizó un análisis de Bland-Altman para comparación de medias y dispersión con ambos métodos contra el criterio de verdad.
RESULTADOS
Características basales
De la base de datos de imágenes de nuestro centro, se analizaron las imágenes previamente adquiridas de 25 pacientes, con edad media de 44±15 años. El 52% era de sexo masculino y el 84% pacientes habían sido estudiados en forma ambulatoria. Entre los diagnósticos más frecuentes se encontraban miocardiopatía hipertrófica (20%), arritmia ventricular (16%), cardiopatía isquémica (16%), miocardiopatía dilatada (12%). La fracción de eyección ventricular izquierda (FEVI) media fue 59 ± 8% y el volumen de la aurícula izquierda medio 97± 38 mL. El resto de las características basales se presenta en la Tabla 1.
Tabla 1
Características basales de los pacientes
| Variable | Valor |
|---|---|
| Edad, años - media (DE) | 45 (15) |
| Sexo masculino - n (%) | 13 (52) |
| Peso, Kg - media (DE) | 80 (19) |
| Talla, cm - media (DE) | 169 (24) |
| Sup corporal, m2 - media (DE) | 1,94 (0,29) |
| VFD VI, ml - mediana (RIC) | 161 (134-187) |
| VFS VI, ml - mediana (RIC) | 63 (42-85) |
| FEVI, % - media (DE) | 59 (8) |
| Masa VI, gr - media (DE) | 115 (43) |
| Volumen AI, ml - media (DE) | 97 (38) |
| Patología principal | |
| Miocardiopatía hipertrófica - n (%) | 5 (20) |
| Arritmia ventricular - n (%) | 4 (16) |
| Cardiopatía isquémica - n (%) | 4 (16) |
| Miocardiopatía dilatada - n (%) | 3 (12) |
| Otros - n (%) | 9 (36) |
AI: aurícula izquierda; DE: desviación estándar; FEVI: fracción de eyección del ventrículo izquierdo; RIC: rango intercuartílico; VFD: volumen de fin de diástole; VFS: volumen de fin de sístole; VI: ventrículo izquierdo
Métodos de cuantificación
La Figura 1 presenta las imágenes de la medición volumétrica de la AI en forma directa, con el método AL y el método CBI.
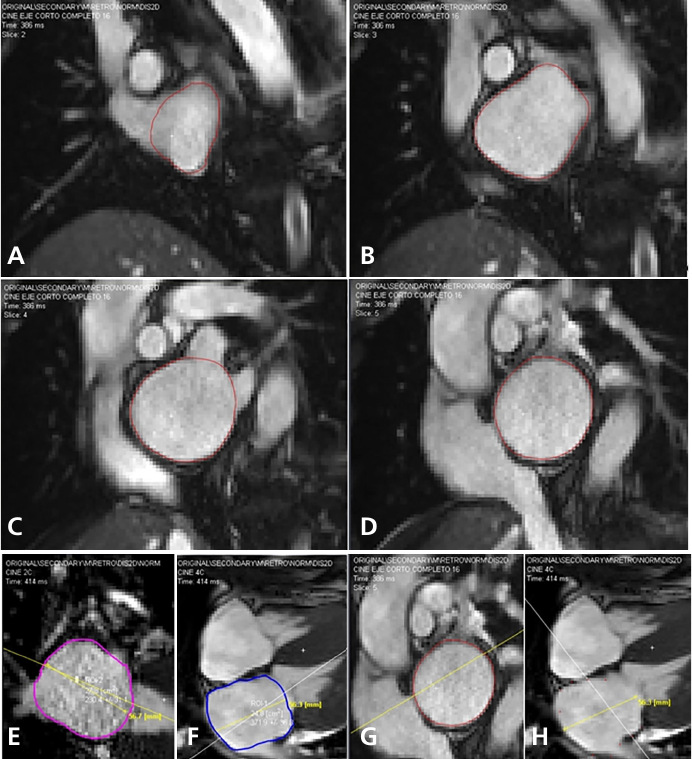
Fig. 1
Mediciones de la aurícula izquierda realizadas en el eje corto completo, 4C y 2C con trazado manual del endocardio en tele-sístole. Volumetria directa (A-B-C-D). Método AL (E-F). Método CBI (G-H)
La correlación medida frente a la cuantificación volumétrica directa fue muy alta para ambos métodos. (Figura 2). El coeficiente de correlación de Pearson fue mayor para el método CBI (r = 0,93; p < 0,001) que para el de AL (r = 0,83; p < 0,001). El análisis de Bland-Altman mostró sesgo bajo para ambos métodos, con menor dispersión para el método CBI [- 5,73 mL (18,6 a -30,11)] que para el método AL [-1,18 mL (43,82 a -46,17)]. La variabilidad interobservador fue menor para el método CBI [4,94 mL (44,76 a -34,88)] que para el método AL [19,7 mL (65,91 a -26,51)] (Figura 3).
Fig. 2
Correlación entre mediciones por métodos de volumetría directa y área-longitud (azul) y cilindro de base irregular (rojo).
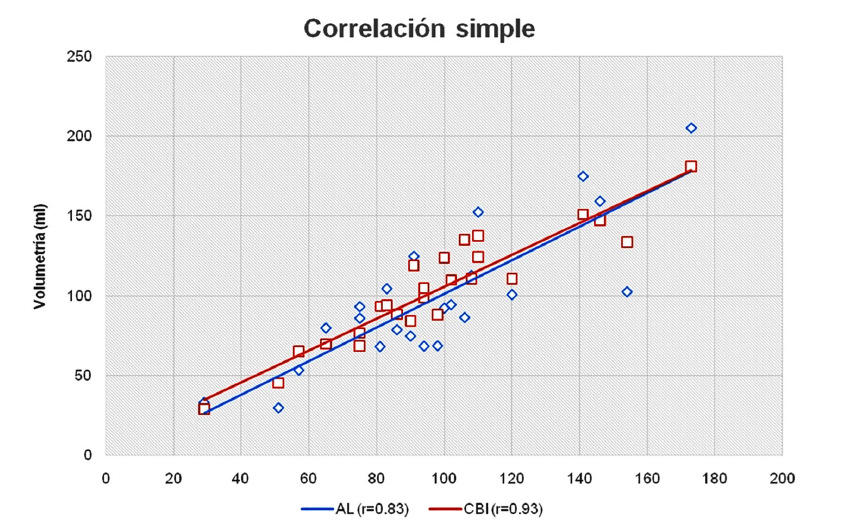
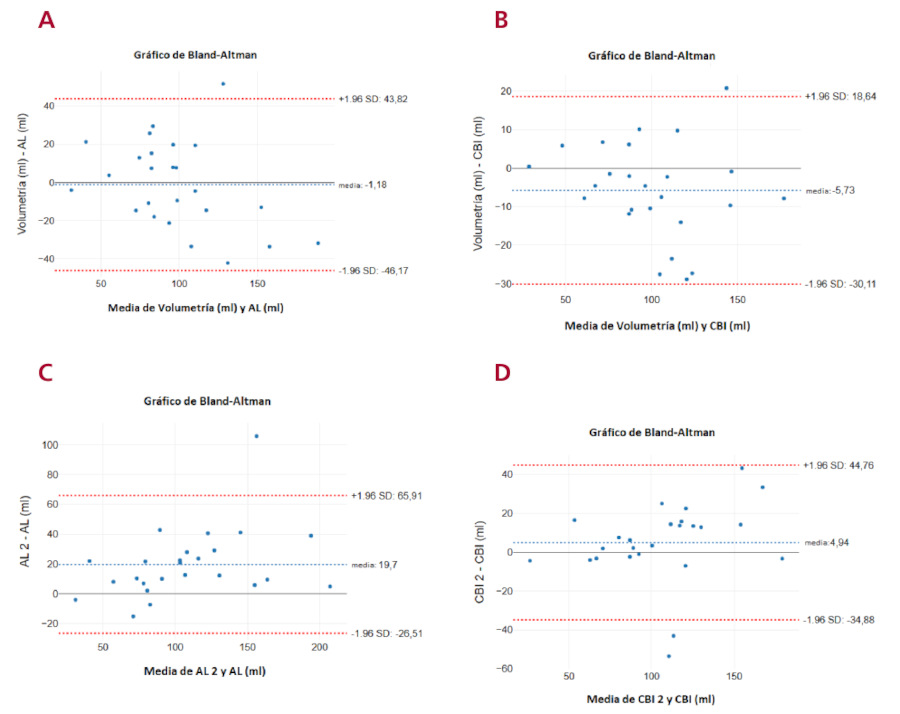
Fig. 3
Diferencia de medias y dispersión en la medición del volumen de la aurícula izquierda: A: Volumetría directa y área-longitud. B: Volumetría directa y cilindro de base irregular. Variabilidad interobservador: C: área-longitud, D: cilindro de base irregular.
Nuestros resultados muestran una excelente correlación de ambos métodos con la cuantificación volumétrica directa, mayor para el nuevo método propuesto (CBI). A su vez, la dispersión para el nuevo método es menor que para el AL y su reproducibilidad interobservador es mayor.
Cabe mencionar que para su realización no es necesaria la adquisición de todo el volumen auricular, ya que con un corte más allá del plano del anillo mitral puede obtenerse la base del cilindro. Esto hace que este método sea práctico y no demande mayor tiempo en la obtención de las imágenes.
El método de AL es excelente, y probablemente su utilización desde la ecocardiografía bidimensional probablemente haya sido la mejor opción para aproximarse al volumen real dada la imposibilidad de una cuantificación directa o interposición de planos estrictamente ortogonales en eje corto. Durante años, en la RMC se adoptó este método desprendido de la ecocardiografía por su buena correlación con la cuantificación directa y la facilidad de obtención y procesamiento de la imagen.
Desde el punto de vista clínico, la estimación precisa del volumen de la AI reviste especial importancia. Con el remodelado, la dilatación de la AI es un marcador de lo que está ocurriendo en la hemodinamia crónica de un paciente. La medición volumétrica puede ofrecer un parámetro de evaluación longitudinal, y constituye un factor pronóstico independiente para eventos cardiovasculares mayores, fibrilación auricular, insuficiencia cardíaca y eventos embólicos. (13-20) En ocasiones, pequeñas diferencias en la estimación volumétrica de la AI pueden generar una interpretación diagnóstica distinta cuando los valores se acercan al punto de corte definido por guías clínicas o consensos. Por ello, una mayor precisión en la estimación haría esperable una mayor exactitud diagnóstica, y esto redundaría en beneficios en la práctica asistencial.
Asimismo, según nuestra observación, la menor variabilidad interobservador haría del CBI un método más robusto que podría resultar particularmente valioso en trabajos multicéntricos o en evaluaciones seriadas, donde la estabilidad metodológica es fundamental para detectar cambios reales en el remodelado auricular.
En síntesis, la RMC tiene la ventaja sobre la ecocardiografía bidimensional de poder realizar cortes con cualquier incidencia deseada y facilita la utilización de figuras y cuerpos geométricos que se amolden mejor a la estimación volumétrica. Creemos que el método de CBI con su aproximación ligeramente más precisa que la utilizada habitualmente sin perjuicio de su practicidad, puede redundar en un beneficio en la interpretación del estudio.
Limitaciones
Se ha utilizado un bajo número de casos previendo un coeficiente r >0,8 y si bien la selección fue aleatoria en la base de datos, probablemente no sea extrapolable este cuerpo geométrico ni tampoco el AL a cualquier morfología auricular.
CONCLUSIÓN
El modelo CBI observó mejor correlación con el estándar de medición directa que la lograda con el método AL. Representa por tal motivo una alternativa válida, igualmente simple y más precisa que el método habitualmente usado para la estimación del volumen de la AI por RMC.
Declaración de conflicto de intereses
Los autores declaran que no tienen conflicto de intereses. (Véane formulariosde conflicto de intereses del autor en la Web).
Financiamiento
No existió financiamiento alguno para realizar este artículo.
BIBLIOGRAFÍA
1. Le TT, Tan RS, De Deyn M, Goh EP, Han Y, Leong BR, et al. Cardiovascular magnetic resonance reference ranges for the heart and aorta in Chinese at 3T. J Cardiovasc Magn Reson 2016;18:21. https://doi.org/10.1186/s12968-016-0236-3
2. Petersen SE, Aung N, Sanghvi MM, Zemrak F, Fung K, Paiva JM, et al. Reference ranges for cardiac structure and function using cardiovascular magnetic resonance (CMR) in Caucasians from the UK Biobank population cohort. J Cardiovasc Magn Reson 2017;19:18. https://doi.org/10.1186/s12968-017-0327-9
3. Zemrak F, Ambale-Venkatesh B, Captur G, Chrispin J, Chamera E, Habibi M, et al. Left Atrial Structure in Relationship to Age, Sex, Ethnicity, and Cardiovascular Risk Factors: MESA (Multi-Ethnic Study of Atherosclerosis). Circ Cardiovasc Imaging 2017;10:9. https://doi.org/10.1161/CIRCIMAGING.116.005379
4. Lang RM, Badano LP, Mor-Avi V, Afilalo J, Armstrong A, Ernande L, et al. Recommendations for cardiac chamber quantification by echocardiography in adults: an update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. Eur Heart J Cardiovasc Imaging 2015;16:233-70. https://doi.org/10.1093/ehjci/jev014
5. Deschle HA, Allende N, Miranda A, Lakowsky A, Sánchez Luceros D, Carbajales J, et al. Volumen de la aurícula izquierda indexada por superficie corporal en sujetos normales divididos por sexo y edad. Rev Argent Cardiol 2010;77:39-42.
6. Nacif MS, Barranhas AD, Turkbey E, Marchiori E, Kawel N, Mello RA, et al. Left atrial volume quantification using cardiac MRI in atrial fibrillation: comparison of the Simpson's method with biplane area-length, ellipse, and three-dimensional methods. Diagn Interv Radiol 2013;19:213-20. https://doi.org/10.5152/dir.2012.002
7. Maceira AM, Cosin-Sales J, Roughton M, Prasad SK, Pennell DJ. Reference left atrial dimensions and volumes by steady state free precession cardiovascular magnetic resonance. J Cardiovasc Magn Reson 2010;12:65. https://doi.org/10.1186/1532-429X-12-65
8. Funk S, Kermer J, Doganguezel S, Schwenke C, von Knobelsdorff-Brenkenhoff F, Schulz-Menger J. Quantification of the left atrium applying cardiovascular magnetic resonance in clinical routine. Scand Cardiovasc J 2018;52:85-92. https://doi.org/10.1080/14017431.2017.1423107
9. Rohner A, Brinkert M, Kawel N, Buechel RR, Leibundgut G, Grize L, et al. Functional assessment of the left atrium by real-time three-dimensional echocardiography using a novel dedicated analysis tool: initial validation studies in comparison with computed tomography. Eur J Echocardiogr 2011;12:497-505. https://doi.org/10.1093/ejechocard/jer066
10. Hudsmith LE, Petersen SE, Francis JM, Robson MD, Neubauer S. Normal human left and right ventricular and left atrial dimensions using steady state free precession magnetic resonance imaging. J Cardiovasc Magn Reson 2005;7:775-82. https://doi.org/10.1080/10976640500295516
11. Maceira AM, Cosin-Sales J, Roughton M, Prasad SK, Pennell DJ. Reference left atrial dimensions and volumes by steady state free precession cardiovascular magnetic resonance. J Cardiovasc Magn Reson 2010;12:65. https://doi.org/10.1186/1532-429X-12-65
12. Rodevand P, Bjornerheim R, Ljosland M, Maehle J, Smith HJ, Ihlen H. Left atrial volumes assessed by three- and two-dimensional echocardiography compared to MRI estimates. International Journal of Cardiac Imaging 1999;15:397-410. https://doi.org/10.1023/A:1006276513186
13. Vaziri SM, Larson MG, Benjamin EJ, Levy D. Echocardiographic predictors of nonrheumatic atrial fibrillation. The Framingham Heart Study. Circulation 1994;89:724-30. https://doi.org/10.1161/01.CIR.89.2.724
14. Tsang TS, Barnes ME, Bailey KR, Leibson CL, Montgomery SC, Takemoto Y, et al. Left atrial volume: important risk marker of incident atrial fibrillation in 1655 older men and women. Mayo Clin Proc 2001;76:467-75. https://doi.org/10.4065/76.5.467
15. Tsang TS, Barnes ME, Gersh BJ, Bailey KR, Seward JE. Left atrial volume as a morphophysiologic expression of LV diastolic dysfunction and predictor of cardiovascular risk burden. Am J Cardiol 2002;90:1284-9. https://doi.org/10.1016/S0002-9149(02)02864-3
16. Benjamin EJ, D'Agostino RB, Belanger AJ, Wolf PA, Levy D. Left atrial size and the risk of stroke and death. Circulation 1995;92:835-41. https://doi.org/10.1161/01.CIR.92.4.835
17. Barnes ME, Miyasaka Y, Seward JB, Gersh BJ, Rosales AG, Bailey KR, et al. Left atrial volume in the prediction of first ischemic stroke in an elderly cohort without atrial fibrillation. Mayo Clin Proc 2004;79:1008-14. https://doi.org/10.4065/79.8.1008
18. Tsang TS, Gersh BJ, Appleton CP, Tajik AJ, Barnes ME, Bailey KR, et al. Left ventricular diastolic dysfunction as a predictor of the first diagnosed nonvalvular atrial fibrillation in 840 elderly men and women. J Am Coll Cardiol 2002;40:1636-44. https://doi.org/10.1016/S0735-1097(02)02373-2
19. Tsang TS, Barnes ME, Gersh BJ, Bailey KR, Seward JB. Risks for atrial fibrillation and congestive heart failure in patients >= 65 years of age with abnormal left ventricular diastolic relaxation. Am J Cardiol 2004;93:54-8. https://doi.org/10.1016/j.amjcard.2003.09.012
20. Sabharwal N, Cemin R, Rajan K, Hickman M, Lahiri A, Senior R. Usefulness of left atrial volume as a predictor of mortality in patients with ischemic cardiomyopathy. Am J Cardiol 2004;94:760-3. https://doi.org/10.1016/j.amjcard.2004.05.060
HTML generado desde un xml-jats a través de la plantilla jats-rac.xsl por RevisCiencia. El motor utilizado es Apache Software Foundation (Xalan XSLTC).
