Belén Davico1, Maximiliano Martín1, Ezequiel Lozano Chiappe1, Rodrigo Esparza Iraola2 MTSAC, Marina Marchesini2 MTSAC, María Pérez2, Leonardo Gómez Rosso1, Laura Boero1, Gustavo Giunta2 MTSAC, Fernando Brites1
1 Laboratorio de Lípidos y Aterosclerosis, Departamento de Bioquímica Clínica, Facultad de Farmacia y Bioquímica, UBA. Buenos Aires, Argentina.
2 Servicio de Cardiología Clínica, Fundación Favaloro. Buenos Aires, Argentina.
Dirección para correspondencia: Belén Davico. Correo electrónico: belendavico@hotmail.com
Rev Argent Cardiol 2024;92:126-132. http://dx.doi.org/10.7775/rac.es.v92.i2.20754
RESUMEN
Introducción: El síndrome post COVID (SPC), que se caracteriza por síntomas que se extienden superando las 4 semanas post-infección, podría desencadenar aumento en el riesgo cardiovascular. Las lipoproteínas de alta densidad (HDL) presentan funciones antiaterogénicas, como su capacidad para promover el transporte inverso del colesterol (TIC) y su actividad antioxidante, en la que es clave la enzima paraoxonasa 1 (PON 1).
Objetivo: Evaluar funcionalidad de HDL en pacientes con SPC comparados con pacientes asintomáticos (PA) y controles.
Material y métodos: Se incluyeron 9 individuos con SPC, 18 PA y 10 controles. Se midieron el hemograma, el perfil lipoproteico básico, las apolipoproteínas A-I y B, y marcadores inflamatorios por métodos automatizados. La actividad de PON 1 se evaluó empleando un método espectrofotométrico y los 3 pasos del TIC, eflujo de colesterol (ECC), y actividades de lecitina:colesterol aciltransferasa (LCAT) y proteína transportadora de colesterol esterificado (CETP), por métodos radiométricos.
Resultados: No se observaron diferencias en sexo, edad, ni parámetros generales. El grupo PA presentó mayor actividad PON que los controles (94±76 vs. 183±111 vs. 148±58 nmol/mL.min, en controles, PA y SPC, respectivamente; p=0,049). No se observaron diferencias en el TIC. El ECC (r=-0,45; p=0,049) y CETP (r=-0,38; p=0,028) correlacionaron negativamente con el índice neutrófilos/linfocitos. LCAT correlacionó inversamente con la ferritina (r=-0,34; p=0,046).
Conclusiones: El incremento de PON 1 en el grupo PA representaría un mecanismo de defensa frente al estrés oxidativo post-infección. Todos los pasos del TIC mostraron una correlación negativa con marcadores inflamatorios. Nuestros resultados podrían explicar, en parte, el vínculo entre COVID y ateroesclerosis.
Palabras clave: Síndrome post COVID - HDL - Lipoproteínas - Estrés oxidativo
ABSTRACT
Background: Post-COVID syndrome (PCS), characterized by symptoms that persist for more than 4 weeks after initial infection, could increase cardiovascular risk. High-density lipoproteins (HDL) have antiatherogenic functions, such as the ability to promote reverse cholesterol transport (RCT) and antioxidant activity. In this regard, paraoxonase 1 (PON 1) plays a key role.
Objective: The aim of this study was to evaluate HDL functions in patients with PCS and compare them with asymptomatic patients (AP) and controls.
Methods: The study included 9 patients with PCS, 18 AP and 10 controls. Complete blood count, basic lipoprotein profile, apolipoproteins A-I and B, and inflammatory markers were measured using automated methods. PON 1 activity was evaluated by a spectrophotometric assay, and the 3 steps of RCT, cellular cholesterol (efflux CCE), lecithin-cholesterol acyltransferase (LCAT) activity and cholesteryl ester transfer protein (CETP) activity were evaluated by radiometric assays.
Results: There were no differences in sex, age, or general parameters. The AP group had higher PON activity than the control group (94±76 vs. 183±111 vs. 148±58 nmol/mL.min, in controls, AP and PCS, respectively; p=0.049). There were no differences in RCT. Cellular cholesterol efflux (r=-0.45; p=0.049) and CETP (r=- 0.38; p=0.028) had a negative correlation with neutrophil-to-lymphocyte ratio. LCAT had an inverse correlation with ferritin (r=-0.34; p=0.046).
Conclusions: Increased antioxidant activity of PON 1 would represent a defensive mechanism against oxidative stress after infection. All the RCT steps had a negative correlation with inflammatory markers. Our findings may explain, at least in part, the link between COVID-19 and atherosclerosis.
Key words: Post COVID Syndrome - Cholesterol HDL - Lipoproteins - Oxidative stress
Recibido: 6/11/2023
Aceptado: 27/02/2024
INTRODUCCIÓN
La infección por el virus Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) produce la enfermedad Coronavirus Disease, descripta en diciembre de 2019 (COVID-19). (1) El síndrome post COVID (SPC) es una enfermedad multisistémica, que se caracteriza por signos y síntomas que se inician durante la infección aguda o posterior a esta y se extienden más allá de las 4 semanas desde el inicio del cuadro infeccioso. (2) Las manifestaciones más frecuentes son fatiga, disnea, dolor torácico, tos, dolor articular, mialgias, cefalea, y palpitaciones. (3) El SPC puede llevar a un deterioro importante en la calidad de vida de las personas que lo padecen. (4) Se estima que al menos un 10% de las infecciones provocan el síndrome y que actualmente no menos de 65 millones de personas lo padecen en el mundo. (5)
El ingreso del virus SARS-CoV-2 al huésped depende de la interacción de la proteína spike del virus con la enzima convertidora de angiotensina 2 (ECA2) que actúa como receptor. (6) Consecuentemente, la ECA2 se encuentra menos disponible para catalizar la conversión de angiotensina II a angiotensina 1-7 y, por lo tanto, aumentan los niveles de angiotensina II. Esta última deberá unirse alternativamente al receptor de angiotensina II tipo 1 (RAT1), lo cual estimula la actividad de las nicotinamida adenina dinucleótido fosfato (NADPH) oxidasas. Estas catalizan la reducción de oxígeno a anión superóxido, iniciando la producción de otras especies reactivas del oxígeno (ROS). (7,8). Este es el principal mecanismo que provoca el aumento de estrés oxidativo en pacientes con COVID-19.
A su vez, dicho aumento se ve favorecido por el contexto proinflamatorio, ya que cuando el virus es reconocido, se liberan citoquinas que actúan reclutando macrófagos y neutrófilos. Estos son responsables de la producción de ROS y otros compuestos oxidantes, además de contribuir a la síntesis de citoquinas. La liberación de citoquinas es prolongada y desmedida, por lo cual se la conoce como tormenta de citoquinas y se encuentra estrechamente relacionada con la gravedad de la enfermedad. ((9),10) La misma puede ocasionar daño tisular y síntomas que se extienden más allá del cuadro agudo de la infección y pueden perdurar en el tiempo, siendo responsables, al menos en parte, del desarrollo del SPC. El aumento del estrés oxidativo trae como consecuencia la alteración de funciones mitocondriales, además de afectar la proliferación celular, el remodelamiento de la matriz extracelular y los mecanismos de defensa a nivel pulmonar. (11) En este contexto, cobra relevancia el rol de los antioxidantes, que incluso se han propuesto como terapia para el SPC. (12,13)
Algunos pacientes, mientras cursaban la enfermedad COVID-19 mostraron menores niveles de colesterol transportado por las lipoproteínas de alta densidad (HDL), única fracción lipoproteica con propiedades antiaterogénicas. Este descenso se encontró relacionado con la gravedad de la enfermedad y una tormenta de citoquinas más exacerbada. (14,15) Además, los niveles del colesterol transportado por las HDL (C-HDL) se asociaron significativamente con una eliminación del virus más prolongada. (1617) Esto destaca el potencial rol antiviral de las HDL que, además de promover el transporte inverso del colesterol, cumplen funciones antitrombóticas, antiapoptóticas, antiinflamatorias y antioxidantes. Esta última se le atribuye debido a su capacidad para inhibir la oxidación de las lipoproteínas de baja densidad (LDL) y es ejercida principalmente por la enzima paraoxonasa (PON) 1, unida a las HDL. (18) Por lo antes mencionado, la evaluación de la funcionalidad de las HDL cobra relevancia en un contexto de elevado estrés oxidativo y de inflamación con alto riesgo de enfermedad cardiovascular como el SPC.
El objetivo del presente estudio fue evaluar las principales funciones cardioprotectoras de las HDL, que incluyen su actividad antioxidante y su capacidad para promover el transporte inverso del colesterol conformado por tres pasos: a) el eflujo de colesterol celular, b) la esterificación del colesterol libre por la enzima lecitina:colesterol aciltransferasa (LCAT), y c) el intercambio de colesterol esterificado por triglicéridos entre las HDL y las lipoproteínas que contienen apoproteína B por la proteína transportadora de colesterol esterificado (CETP), de importancia terapéutica. (19) El deterioro en algunas de las funciones de las HDL podría estar relacionado con una eliminación enlentecida del virus SARS-CoV-2 del organismo y la evolución de la infección hacia el SPC.
MATERIAL Y MÉTODOS
Diseño y sujetos
Estudio observacional de corte transversal realizado en forma colaborativa entre el Hospital Universitario Fundación Favaloro y el Laboratorio de Lípidos y Aterosclerosis de la Facultad de Farmacia y Bioquímica, UBA, entre junio de 2021 y febrero de 2022. Se utilizaron los siguientes criterios de inclusión: hombres y mujeres entre 20 y 60 años, que hubieran padecido infección por COVID-19 confirmada por proteína C reactiva (PCR) entre 4 y 12 semanas previas a la inclusión, que aceptasen la firma del consentimiento informado. Este período de tiempo corresponde al denominado COVID persistente sintomático definido por las Guías del National Institute for Health and Care Excellence (NICE) 2020. (2) Según la presencia de síntomas persistentes, se definió un grupo portador de SPC (SPC, n = 9) que se comparó con un grupo de pacientes que habían padecido la enfermedad y evolucionaron asintomáticos (PA, n = 18). Además, se incorporó un grupo control sin diagnóstico de COVID-19 en el último año (Control, n = 10). Se excluyeron los pacientes que presentaron síntomas previos a la infección por COVID-19, índice de masa corporal (IMC) mayor de 35 kg/m2, presencia de comorbilidades (enfermedad renal crónica, diabetes mellitus tipo 1 o tipo 2, hepatopatías crónicas, enfermedades inflamatorias crónicas, cardiopatías estructurales o funcionales, neumopatías), aquellos que estuvieran bajo tratamiento con inhibidores de la ECA, antagonistas del receptor de la angiotensina II, estatinas o corticoides, y mujeres embarazadas. El estudio fue aprobado por el Comité de Bioética de la Fundación Favaloro de acuerdo con la declaración de Helsinki y posteriores enmiendas a la misma.
Evaluación de las características clínicas y antropométricas
Se efectuó una anamnesis exhaustiva y un examen clínico a todos los individuos seleccionados. Se evaluó el peso y la talla para luego calcular el IMC. También, se midió la presión arterial (PA) en 3 oportunidades con un esfigmomanómetro certificado (Welch-Allyn, EEUU). Se consideró válido el promedio de las dos últimas determinaciones. Para objetivar la persistencia de síntomas y evaluar la capacidad funcional, se realizó una prueba de marcha de 6 minutos y se estableció el grado de esfuerzo por la escala de Borg. (2021)
Muestras
Se extrajo sangre de la vena antecubital luego de 12 horas de ayuno. Las muestras se recogieron en tubos con gel acelerador de la coagulación y en tubos con Na2EDTA, los cuales se centrifugaron a 1500 rpm, durante 15 minutos. Se separó el suero y/o plasma, según correspondiese, y se almacenaron alícuotas a 4° y -70° C.
Determinación de parámetros bioquímicos generales y específicos
Se determinaron las concentraciones plasmáticas de urea y creatinina, así como el hemograma completo por métodos estandarizados.
Caracterización del estado inflamatorio general
Se determinó la concentración de PCR ultrasensible (PCRus) y de ferritina por ensayos inmunoturbidimétricos en un autoanalizador COBAS C 501 (Roche S.A.Q. e I., Suiza). Además, se realizó el cálculo del cociente neutrófilos/linfocitos como indicador del estado inflamatorio. (22)
Determinación del perfil de lípidos, lipoproteínas y apolipoproteínas
Los niveles plasmáticos de triglicéridos, colesterol total y C-HDL se determinaron por métodos estandarizados. Se calculó el nivel de C-LDL empleando las fórmulas de Friedewald o de Sampson según los niveles plasmáticos de triglicéridos. Se realizó el dosaje de apo B y apo A-I por inmunoturbidimetría en un autoanalizador COBAS C 501 (Roche, Basilea, Suiza).
Medición de la actividad de la paraoxonasa 1
La actividad de la enzima PON 1 fue evaluada a través de un ensayo cinético espectrofotométrico desarrollado empleando dos sustratos: paraoxón (actividad paraoxonasa propiamente dicha, PON) y fenilacetato (actividad arilesterasa, ARE). Ambas actividades se midieron siguiendo un método previamente descripto con mínimas modificaciones. (23) Los fenotipos para la variante genética Q192R del gen de PON 1 se estimaron mediante el método del doble sustrato. (24)
Evaluación de la capacidad de las HDL para promover el eflujo de colesterol celular
Se aislaron las HDL con reactivo precipitante polietilenglicol 6000 al 45% y buffer Tris-HCl 0,2 M (pH=8,2). La capacidad de las HDL aisladas para promover el eflujo de colesterol celular fue determinada empleando la línea celular de monocitos humanos THP-1. (25)
Medición de la actividad de la lecitina:colesterol aciltransferasa
La determinación de la actividad de la enzima LCAT se llevó a cabo mediante un método radiométrico desarrollado siguiendo una versión modificada del protocolo de Aguilar- Espinoza y cols. (26)
Medición de la actividad de la proteína transportadora de colesterol esterificado
Se determinó la actividad de la CETP siguiendo un método radiométrico desarrollado previamente descripto con pequeñas modificaciones. (27)
Análisis estadístico
El cálculo muestral se llevó a cabo considerando poder del 80% y un error α de 0,05 utilizando el software Open Epi (MIT, EEUU). Se escogió como variable dependiente a la actividad de la PON y se utilizaron datos previos no publicados del grupo en poblaciones similares. Se estimó un número mínimo de 8 individuos por grupo. Se presentaron las variables cuantitativas como media y desviación estándar, o mediana y rango intercuartílico (Q1-Q3) según la distribución observada. Se evaluó el supuesto de normalidad de la distribución poblacional de cada variable de manera descriptiva (comparación de medias y medianas), gráfica (histograma y gráfico cuantil - cuantil) y con test de bondad de ajuste (test de Kolmogorov - Smirnov y test de Shapiro - Wilk). Para comparar las variables continuas se utilizó ANOVA o prueba de Kruskal Wallis según la distribución de los datos. La correlación se analizó mediante los coeficientes de Pearson (variables paramétricas) o Spearman (variables no paramétricas). Las diferencias en variables categóricas fueron evaluadas mediante el test de Chi cuadrado (c2). Se utilizaron los programas estadísticos Infostat (Universidad Nacional de Córdoba, Córdoba, Argentina) y SPSS, versión 26.0 (Chicago, Illinois, EEUU.). Se consideraron estadísticamente significativas las probabilidades menores a 0,05 para tests de dos colas.
RESULTADOS
En los 3 grupos evaluados en el presente estudio, la distribución de géneros, la edad, la talla, el peso, el IMC, y la PA fueron similares (Tabla 1). Los pacientes del grupo SPC presentaron como síntomas principales disnea (69%), palpitaciones (54%) y astenia (46%). Coincidentemente, en el grupo SPC se observó un incremento de la escala de Borg en el test de marcha de 6 minutos (1,6±1,0 vs. 1,2±1,0 vs. 3,5±1,9; control, PA y SPC, respectivamente; p = 0,017). No se encontraron diferencias significativas en ninguno de los parámetros bioquímicos generales medidos, ni en los parámetros del hemograma analizados. (Tabla 1)
En relación con el perfil lipoproteico, no se observaron diferencias significativas en los niveles plasmá ticos de colesterol total, C-LDL, C-HDL, triglicéridos, ni tampoco de apo A-I o B. (Tabla 2) A su vez, ninguno de los indicadores de inflamación analizados (PCRus, ferritina y cociente neutrófilos/linfocitos) mostró diferencias significativas entre los tres grupos. (Tabla 3)
Al analizar los tres pasos del transporte inverso de colesterol, ninguno de ellos mostró diferencias significativas (Figura 1), pero los tres presentaron asociación con otros parámetros: el eflujo de colesterol celular correlacionó negativamente con el índice neutrófilos/ linfocitos (r = -0,45; p=0,049), la actividad LCAT inversamente con el reactante de fase aguda ferritina (r = -0,34; p=0,046), y la actividad CETP positivamente con los niveles de triglicéridos r=0,47; p=0,006 y negativamente con el índice neutrófilos/linfocitos (r = -0,38; p=0,028).
El grupo PA presentó mayor actividad PON que los controles (94±76 vs. 183±111 vs. 148±58 nmol/ mL.min, en controles, PA y SPC, respectivamente; p=0,049) sin observarse diferencias significativas en la actividad ARE entre los tres grupos (Figura 2). Además, todos los grupos presentaron una distribución fenotípica similar de la variante genética Q192R de la PON 1, lo que permitió la comparación entre grupos.
DISCUSIÓN
Los resultados expuestos muestran que el SPC no se asocia a modificaciones del transporte inverso del colesterol en los grupos analizados. Sin embargo, se observa un cambio en la función antioxidante de las HDL representada por una mayor actividad PON en pacientes que resolvieron la sintomatología en comparación con controles sanos. Cabe destacar la importancia de esta función durante las infecciones virales, ya que tanto el desempeño como la supervivencia de las células del sistema inmune depende del control del sistema oxidativo, particularmente de los niveles de ROS, (28) los cuales se ven aumentados en el SPC. Por ello el aumento en la actividad PON se podría explicar como un mecanismo de defensa frente al aumento del estrés oxidativo. De hecho, este aumento como mecanismo de defensa ya ha sido descripto en otras condiciones asociadas a la presencia de estrés oxidativo como el ejercicio físico. (29,30)
Además de la actividad PON, también se analizó la actividad ARE, la cual no es afectada por variantes genéticas, siendo considerada marcador de la concentración de PON 1. (24) Por tal motivo, el hallazgo de un aumento de la actividad PON, junto con una actividad ARE conservada, estaría sugiriendo un incremento específico de la actividad intrínseca de la enzima sin modificaciones de su concentración. Esta respuesta, que se observa en pacientes con sintomatología resuelta y no en pacientes con SPC, podría explicar, al menos en parte, la persistencia de sintomatología en este último grupo. De hecho, en trabajos previos se le ha atribuido un rol antiviral a las HDL, particularmente en COVID-19. (17) Más aún, la actividad antioxidante de las HDL, atribuible a la enzima PON 1, así como la capacidad antiaterogénica general de estas lipoproteínas, tendría influencia en la supresión de la replicación de este virus. (17) En concordancia, en un estudio previo, se mostró que la variante alélica de mayor actividad para Q192R de la PON 1 se asociaba a menor gravedad de la enfermedad COVID-19. (31)
Es importante destacar que no se observó un incremento de los marcadores inflamatorios medidos en nuestra población. Sin embargo, existe una correlación negativa de cada uno de los pasos del transporte inverso del colesterol con alguno de estos marcadores. Esto confirmaría el impacto previamente reportado que puede tener la inflamación persistente en la funcionalidad de las HDL y en el desarrollo de enfermedad cardiovascular aterosclerótica. (32,33) De hecho, en un trabajo previo, mostramos la asociación negativa que existe entre la presencia de inflamación específica vascular y el transporte inverso de colesterol en niños y adolescentes con obesidad. (34).
Por otro lado, la persistencia de síntomas en el grupo SPC se asoció a un incremento en la escala de Borg reportada para la prueba de marcha de 6 minutos. Esta prueba se ha utilizado extensamente para medir la capacidad funcional ante el ejercicio, (35) que se ha encontrado alterada en los pacientes luego de la infección aguda por COVID-19. (36) La disociación entre la clínica y los marcadores inflamatorios podría explicarse por la heterogeneidad que estos últimos muestran en diversos estudios. Como se explicó anteriormente, la inflamación persistente podría jugar un rol importante en el desarrollo de SPC. (9,10) Sin embargo, la evidencia al respecto no es conclusiva. En un estudio reciente, se observó que la inflamación persistente estaba presente en aproximadamente un 60% de los pacientes con SPC. (37) Más aún, diversos factores como la severidad de la infección aguda, la edad, o el IMC serían determinantes sobre la persistencia de inflamación. (37) Por otra parte, en un metaanálisis que analizo 113 marcadores inflamatorios en SPC, se reportó que marcadores como la PCRus o la ferritina no se encontraban elevados aún en presencia de inflamación persistente. (38) El estatus inflamatorio de los pacientes con SPC estaría definido por marcadores de inflamación de bajo grado como los interferones. (37,38) De esta manera, la diversidad presente en los pacientes con SPC podría explicar la falta de diferencias en los marcadores inflamatorios presentes en nuestro estudio. Sin embargo, tampoco puede descartarse la presencia de inflamación de bajo grado, lo cual podría explicar en parte la asociación negativa entre los parámetros inflamatorios y la funcionalidad de HDL observada en los pacientes afectados.
Tabla 1. Parámetros antropométricos y bioquímicos generales
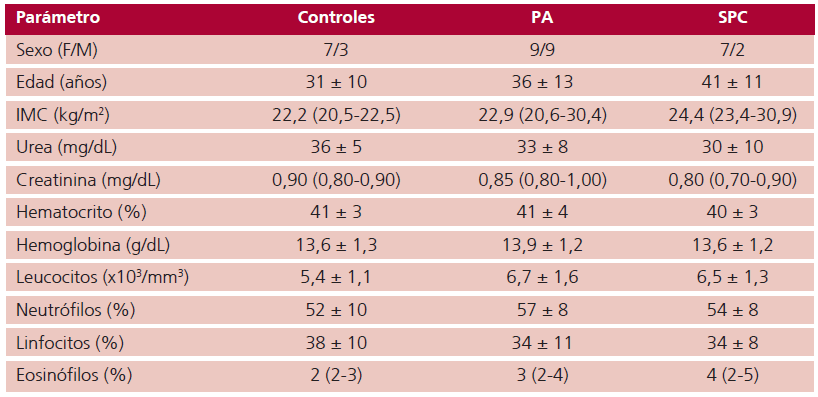
F: femenino; IMC: índice de masa corporal; M: masculino; PA: pacientes asintomáticos; SPC: pacientes con síndrome post COVID.
Las variables se expresan como media ± DE o mediana y rango intercuartílico (Q1-Q3) según su distribución
Tabla 2. Perfil de lípidos, lipoproteínas y apolipoproteínas
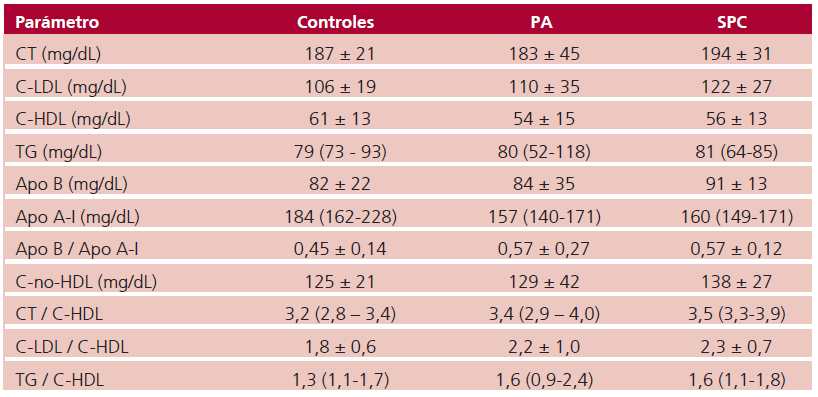
Apo: apolipoproteína; C-HDL: olesterol de lipoproteínas de alta densidad; C-LDL: colesterol de lipoproteínas de baja densidad; CT: colesterol total; PA: pacientes asintomáticos; SPC: pacientes con síndrome post COVID; TG: triglicéridos Las variables se expresan como media ± DE o mediana y rango intercuartílico (Q1-Q3) según su distribución
Tabla 3. Indicadores de inflamación
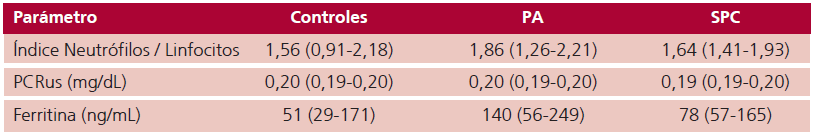
PA: pacientes asintomáticos; PCRus: proteína C reactiva ultrasensible; SPC: pacientes con síndrome post COVID. Las variables se expresan como mediana y rango intercuartílico (Q1-Q3) según su distribución
Fig. 1. Evaluación de los tres pasos del transporte inverso del colesterol. Panel A: Eflujo de colesterol celular. Panel B: Actividad LCAT. Panel C: Actividad CETP.

CETP: proteína transportadora de colesterol esterificado; LCAT: lecitina: colesterol aciltransferasa; PA: pacientes asintomáticos; SPC: pacientes con síndrome post COVID.
Fig. 2. Actividades de la enzima paraoxonasa 1. Panel A: actividad PON. Panel B: actividad ARE.
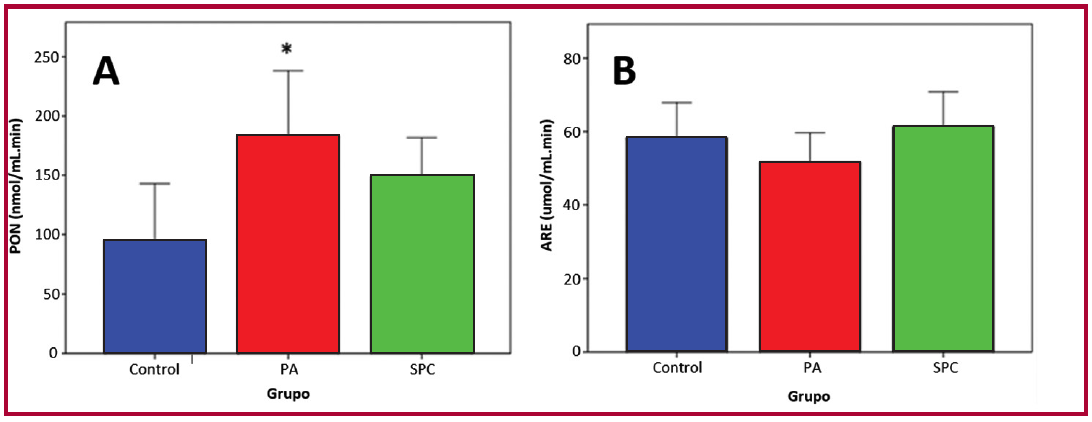
ARE: arilesterasa; PA: pacientes asintomáticos; PON: paraoxonasa; SPC: pacientes con síndrome post COVID. * p = 0,049 entre PA y Controles
CONCLUSIONES
El incremento de la actividad antioxidante de PON 1 representaría un mecanismo de defensa frente al estrés oxidativo que solo alcanza significancia estadística en el grupo PA. A su vez, la asociación negativa entre los marcadores de inflamación y cada uno de los pasos del transporte inverso del colesterol sugiere la presencia de un efecto perjudicial de bajo grado del proceso inflamatorio sobre esta función crucial de las HDL. Nuestros resultados podrían explicar, al menos en parte, el vínculo entre SPC y la ateroesclerosis.
Declaración de conflicto de intereses
Los autores declaran que no tienen conflicto de intereses.
(Véanse formularios de conflicto de intereses de los autores en la Web).
Financiamiento
Proyecto PIP N° 11220200102363 y proyecto UBACyT N° 20020190100075BA.
https://creativecommons.org/licenses/by-nc-sa/4.0/

©Revista Argentina de Cardiología
BIBLIOGRAFÍA
- https://www.who.int/es/news/item/27-04-2020-who-timeline-covid-19
- COVID-19 rapid guideline: managing the long-term effects of COVID-19. London: National Institute for Health and Care Excellence (NICE); 2020 Dec 18.
- Oronsky B, Larson C, Hammond TC, Oronsky A, Kesari S, Lybeck M, et al. A Review of Persistent Post-COVID Syndrome (PPCS). Clin Rev Allergy Immunol. 2023;64:66-74. https://doi.org/10.1007/s12016-021-08848-3
- Ayoubkhani D, Khunti K, Nafilyan V, Maddox T, Humberstone B, Diamond I, et al. Post-covid syndrome in individuals admitted to hospital with covid-19: retrospective cohort study. BMJ. 2021;372:n693. https://doi.org/10.1136/bmj.n693
- Davis HE, McCorkell L, Vogel JM, Topol EJ. Long COVID: major findings, mechanisms and recommendations. Nat Rev Microbiol. 2023;21:133-46. https://doi.org/10.1038/s41579-022-00846-2
- Beyerstedt S, Casaro EB, Rangel ÉB. COVID-19: angiotensin-converting enzyme 2 (ACE2) expression and tissue susceptibility to SARS-CoV-2 infection. Eur J Clin Microbiol Infect Dis. 2021;40:905- 19. https://doi.org/10.1007/s10096-020-04138-6
- Suhail S, Zajac J, Fossum C, Lowater H, McCracken C, Severson N, et al. Role of Oxidative Stress on SARS-CoV (SARS) and SARS-CoV-2 (COVID-19) Infection: A Review. Protein J. 2020;39:644-56. https://doi.org/10.1007/s10930-020-09935-8
- Contreras-Briceño F, Espinosa-Ramírez M, Rozenberg D, Reid WD. Eccentric Training in Pulmonary Rehabilitation of Post-COVID-19 Patients: An Alternative for Improving the Functional Capacity, Inflammation, and Oxidative Stress. Biology (Basel). 2022;11:1446. https://doi.org/10.3390/biology11101446
- Sorokin AV, Karathanasis SK, Yang ZH, Freeman L, Kotani K, Remaley AT. COVID-19-Associated dyslipidemia: Implications for mechanism of impaired resolution and novel therapeutic approaches. FASEB J. 2020;34:9843-53. https://doi.org/10.1096/fj.202001451
- Tang L, Yin Z, Hu Y, Mei H. Controlling Cytokine Storm Is Vital in COVID-19. Front Immunol. 2020;11:570993. https://doi.org/10.3389/fimmu.2020.570993.
- Siekacz K, Kumor-Kisielewska A, Miłkowska-Dymanowska J, Pietrusińska M, Bartczak K, Majewski S, et al. Oxidative Biomarkers Associated with the Pulmonary Manifestation of Post-COVID-19 Complications. J Clin Med. 2023;12:4253. https://doi.org/10.3390/jcm12134253
- Vollbracht C, Kraft K. Oxidative Stress and Hyper-Inflammation as Major Drivers of Severe COVID-19 and Long COVID: Implications for the Benefit of High-Dose Intravenous Vitamin C. Front Pharmacol. 2022;13:899198. https://doi.org/10.3389/fphar.2022.899198
- Jarrott B, Head R, Pringle KG, Lumbers ER, Martin JH. “LONG COVID”-A hypothesis for understanding the biological basis and pharmacological treatment strategy. Pharmacol Res Perspect. 2022;10:e00911. https://doi.org/10.1002/prp2.911
- Hu X, Chen D, Wu L, He G, Ye W. Declined serum high density lipoprotein cholesterol is associated with the severity of COVID-19 infection. Clin Chim Acta. 2020;510:105-10. https://doi.org/10.1016/j.cca.2020.07.015
- Wang G, Zhang Q, Zhao X, Dong H, Wu C, Wu F, et al. Low high-density lipoprotein level is correlated with the severity of COVID-19 patients: an observational study. Lipids Health Dis. 2020;19:204. https://doi.org/10.1186/s12944-020-01382-9
- Ding X, Zhang J, Liu L, Yuan X, Zang X, Lu F, et al. High-density lipoprotein cholesterol as a factor affecting virus clearance in covid-19 patients. Respir Med. 2020;175:106218. https://doi.org/10.1016/j.rmed.2020.106218
- Cho KH, Kim JR, Lee IC, Kwon HJ. Native High-Density Lipoproteins (HDL) with Higher Paraoxonase Exerts a Potent Antiviral Effect against SARS-CoV-2 (COVID-19), While Glycated HDL Lost the Antiviral Activity. Antioxidants (Basel). 2021;10:209. https://doi.org/10.3390/antiox10020209
- Brites F, Martin M, Guillas I, Kontush A. Antioxidative activity of high-density lipoprotein (HDL): Mechanistic insights into potential clinical benefit. BBA Clin. 2017;8:66-77. https://doi.org/10.1016/j.bbacli.2017.07.002
- Nurmohamed NS, Ditmarsch M, Kastelein JJP. Cholesteryl ester transfer protein inhibitors: from high-density lipoprotein cholesterol to low-density lipoprotein cholesterol lowering agents? Cardiovasc Res. 2022;118:2919-31. https://doi.org/10.1093/cvr/cvab350.
- Enright PL. The six-minute walk test. Respir Care 2003;48:783–5.
- Borg GA. Psychophysical bases of perceived exertion. Med Sci Sports Exerc 1982;14:377–81.
- Buonacera A, Stancanelli B, Colaci M, Malatino L. Neutrophil to Lymphocyte Ratio: An Emerging Marker of the Relationships between the Immune System and Diseases. Int J Mol Sci. 2022;23:3636. https://doi.org/10.3390/ijms23073636
- Furlong CE, Richter RJ, Seidel SL, Costa LG, Motulsky AG. Spectrophotometric assays for the enzymatic hydrolysis of the active metabolites of chlorpyrifos and parathion by plasma paraoxonase/arylesterase. Anal Biochem. 1989;180:242-7. https://doi.org/10.1016/0003-2697(89)90424-7
- Nevin DN, Zambon A, Furlong CE, Richter RJ, Humbert R, Hokanson JE, et al. Paraoxonase genotypes, lipoprotein lipase activity, and HDL. Arterioscler Thromb Vasc Biol. 1996;16:1243-9. https://doi.org/10.1161/01.atv.16.10.1243
- Martin M, Condori AI, Davico B, Gómez Rosso L, Gaete L, Tetzlaff W, et al. Impaired Reverse Cholesterol Transport is Associated with Changes in Fatty Acid Profile in Children and Adolescents with Abdominal Obesity. J Nutr. 2024;154:12-25. https://doi.org/10.1016/j.tjnut.2023.08.037
- Aguilar-Espinosa SL, Mendoza-Espinosa P, Delgado-Coello B, Mas-Oliva J. Lecithin cholesterol acyltransferase (LCAT) activity in the presence of Apo-AI-derived peptides exposed to disorder-order conformational transitions. Biochem Biophys Res Commun. 2013;441:469-75.
- Lagrost L, Gandjini H, Athias A, Guyard-Dangremont V, Lallemant C, Gambert P. Influence of plasma cholesteryl ester transfer activity on the LDL and HDL distribution profiles in normolipidemic subjects. Arterioscler Thromb. 1993;13:815-25. https://doi.org/10.1161/01.atv.13.6.815
- Morris G, Gevezova M, Sarafian V, Maes M. Redox regulation of the immune response. Cell Mol Immunol. 2022;19:1079-101. https://doi.org/10.1038/s41423-022-00902-0
- Otocka-Kmiecik A, Orłowska-Majdak M, Stawski R, Szkudlarek U, Kosielski P, Padula G, et al. Repetitions of Strenuous Exercise Consistently Increase Paraoxonase 1 Concentration and Activity in Plasma of Average-Trained Men. Oxid Med Cell Longev. 2021;2021:2775025. https://doi.org/10.1155/2021/2775025
- Brites F, Zago V, Verona J, Muzzio ML, Wikinski R, Schreier L. HDL capacity to inhibit LDL oxidation in well-trained triathletes. Life Sci. 2006;78:3074-81. https://doi.org/10.1016/j.lfs.2005.12.015
- Ghoreshi ZA, Abbasi-Jorjandi M, Asadikaram G, Sharif-Zak M, Seyedi F, Khaksari Haddad M, et al. Paraoxonase 1 rs662 polymorphism, its related variables, and COVID-19 intensity: Considering gender and post-COVID complications. Exp Biol Med (Maywood). 2023;248:2351-62. https://doi.org/10.1177/15353702221128563
- Tall AR, Yvan-Charvet L. Cholesterol, inflammation and innate immunity. Nat Rev Immunol. 2015;15:104-16. https://doi.org/10.1038/nri3793
- McGillicuddy FC, de la Llera Moya M, Hinkle CC, Joshi MR, Chiquoine EH, Billheimer JT, et al. Inflammation impairs reverse cholesterol transport in vivo. Circulation. 2009;119:1135-45. https://doi.org/10.1161/CIRCULATIONAHA.108.810721
- Martin M, Gaete L, Tetzlaff W, Ferraro F, Lozano Chiappe E, Botta EE, Osta V, et al. Vascular inflammation and impaired reverse cholesterol transport and lipid metabolism in obese children and adolescents. Nutr Metab Cardiovasc Dis. 2022;32:258-68. https://doi.org/10.1016/j.numecd.2021.09.025
- ATS Committee on Proficiency Standards for Clinical Pulmonary Function Laboratories. ATS statement: guidelines for the six-minute walk test. Am J Respir Crit Care Med. 2002;166:111-7. https://doi.org/10.1164/ajrccm.166.1.at1102
- Qorolli M, Beqaj S, Ibrahimi-Kaçuri D, Murtezani A, Krasniqi V, Mačak Hadžiomerović A. Functional status and quality of life in post-COVID-19 patients two to three weeks after hospitalization: A cross-sectional study. Health Sci Rep. 2023;6:e1510. https://doi.org/10.1002/hsr2.1510
- Talla A, Vasaikar SV, Szeto GL, Lemos MP, Czartoski JL, MacMillan H, et al. Persistent serum protein signatures define an inflammatory subcategory of long COVID. Nat Commun. 2023;14:3417. https://doi.org/10.1038/s41467-023-38682-4
- Lai YJ, Liu SH, Manachevakul S, Lee TA, Kuo CT, Bello D. Biomarkers in long COVID-19: A systematic review. Front Med (Lausanne). 2023;10:1085988. https://doi.org/10.3389/fmed.2023.1085988.