INTRODUCCIÓN
El consumo mundial de dietas ricas en carbohidratos y grasas constituye un factor determinante en el desarrollo del síndrome metabólico (SM), definido por la concurrencia de al menos tres alteraciones metabólicas –hiperglucemia, hipertrigliceridemia, resistencia a la insulina, hipertensión arterial (HTA), inflamación sistémica o aumento del perímetro de cintura– que comprometen diversos órganos, en particular el riñón, esencial en la homeostasis hidroelectrolítica y el control de la presión arterial. (1,2) Las dietas hipercalóricas inducen disfunción renal estructural y funcional e incrementan el riesgo de HTA, una enfermedad crónica y asintomática responsable de aproximadamente el 50% de la mortalidad cardiovascular global. (3,4) Según un estudio poblacional de la Organización Mundial de la Salud publicado en The Lancet en 2021, que incluyó 104 millones de participantes, la prevalencia de HTA fue de 59 % en mujeres (55-62 años) y 49 % en varones (46-52 años), con tratamiento en solo 47% y 38 %, respectivamente. (5) Más recientemente, en 2023 el informe de la OMS “Global Report on Hypertension: The Race Against a Silent Killer” señaló una prevalencia mundial del 34 % en varones y del 32 % en mujeres, diferencia que tiende a desaparecer con el avance de la edad. (6). En Argentina, el estudio RENATA 2 (2017) reportó una incidencia de 36,3 % en adultos de 26-60 años, mayor en varones. (7)
En la regulación renal de la presión arterial destacan el sistema dopaminérgico renal (SDR) y el sistema renina-angiotensina (SRA). El SDR, localizado en el túbulo contorneado proximal, promueve natriuresis, diuresis y efectos antiinflamatorios actuando sobre receptores D1 y D2, contrarrestando la acción de insulina y angiotensina II (Ang II). (8) Por el contrario, la sobreactivación del SRA estimula la reabsorción tubular de sodio y agua e incrementa la inflamación y el estrés oxidativo. Ambos sistemas mantienen un antagonismo funcional, ya que la angiotensina II inhibe la síntesis y actividad dopaminérgica. (9) En este marco, el cociente L-dopa/dopamina ha sido propuesto como biomarcador temprano de daño renal en modelos animales de HTA inducida por fructosa. (10)
El tratamiento farmacológico de la HTA incluye antagonistas del receptor AT1 (AT1R), entre ellos el losartán (L), un bloqueante competitivo, potente y selectivo que inhibe de forma específica los efectos de la Ang II. (11) Aunque su eficacia antihipertensiva es conocida, su capacidad de modular el equilibrio SDR– SRA en el SM inducido por dietas grasas (DG) como parte de su acción nefroprotectora no ha sido del todo aclarada. En este contexto, se propuso evaluar si la DG altera dicho equilibrio como mecanismo de HTA, y si el tratamiento temprano con L previene estas alteraciones en un modelo experimental de SM inducido por DG durante 8 semanas, analizando además la utilidad del índice L-dopa/dopamina como biomarcador temprano de disfunción renal.
MATERIAL Y MÉTODOS
A) Animales, diseño experimental y dieta.
Ratas macho Sprague-Dawley (6 semanas de edad, 180-200 g; Bioterio Central, FFyB-UBA) se mantuvieron en condiciones controladas (22 ± 2°C, 50-70% humedad, 12 h luz/oscuridad), y se estudiaron durante 8 semanas, distribuidas en cuatro grupos (n=4-6):
- C: dieta estándar y agua ad-libitum (SD; Asociación Cooperativas Argentinas; 20 % proteínas, 3 % grasa, 2 % fibra, 6 % minerales, 69 % almidón, vitaminas; 3,3 kcal/g);
- DG: SD + 50 % p/p grasa y agua ad-libitum (Faty, Quick-food S.A., Argentina; 9 kcal/g, 99 % grasa total, 77 % saturada, 19 % trans);
- CL: C + losartán (L), 30 mg/kg/día, agua. Losartan potásico, 100% en base seca, Droguería Saporiti S.A.C.I.F.I.A, Buenos Aires, Argentina);
- DGL: DG + CL.
B) Peso corporal, ingesta y calorías.
El peso corporal se registró diariamente. La ingesta de alimento y bebida se midió cada 48 h. Se calcularon: I) alimento (g/día) = ofrecido – remanente; II) bebida (mL/día) = ofrecido – remanente; III) calorías: C y CL = SD (g) × 3,3 kcal/g; DG y DGL = SD (g) × 3,3 kcal/g + grasa (g) × 9 kcal/g.
C) Presión arterial sistólica (PAS).
Se midió al inicio y antes del sacrificio por pletismografía de cola con esfigmomanómetro fotoeléctrico (Grass D.C. 7DAC) y osciloscopio (Grass D.C. 79D, Grass Instruments Co., USA).
D) Recolección de orina y sangre.
Tres días antes del sacrificio los animales se alojaron en jaulas metabólicas por 48h. Recolección de orina: I) la fracción urinaria de las primeras 6 h fue recuperada en solución acuosa de ácido clorhídrico con una concentración 6 Normal (HCl 6 N), alicuotada en HCl 1 N y −80 °C para determinación de L-dopa y dopamina por cromatografía líquida de alta eficacia (HPLC); II) la fracción urinaria de las siguientes 18 h se conservó a −20 °C para determinar sodio, creatinina y albúmina (Spectrum CCX, Abbott Diagnostics, USA). La diuresis se determinó por volumen total orinado en 24 h. El día del sacrificio, tras un ayuno de 6 h, se obtuvo sangre por punción retroorbitaria bajo anestesia (ketamina 80 mg/kg + xilazina 12 mg/kg, PRO-SER SA).
E) Obtención de tejidos.
Se realizó el sacrificio con los animales anestesiados, en cámara con CO2. Los riñones se decapsularon, pesaron y distribuyeron al azar para histología, microscopía electrónica de transmisión (MET), y Western blot.
F) Determinaciones.
F-1) Metabolismo plasmático: Glucemia con Accu-Chek Performa Nano (Roche Diagnostics, Alemania). Trigliceridemia con kit TG Color GPO/PAP AA (Wiener Lab., Argentina). Insulina por ELISA (Mercodia Rat Insulin ELISA, Suecia). Se calcularon el producto triglicérido glucosa (TyG) (12) y el índice de Evaluación del Modelo Homeostático de la Resistencia a la Insulina (HOMA-IR). (13)
F-2) Función renal: Se midió sodio y creatinina en plasma y orina (Spectrum CCX); tasa de filtración glomerular (TFG) estimada por clearance de creatinina; función tubular evaluada por excreción urinaria de sodio (UNa+.V) y excreción fraccional de sodio (FENa+).
F-3) Catecolaminas urinarias: L-dopa y dopamina de midieron por HPLC en fase reversa (columna Zorbax RxC18; DuPont, USA; detección amperométrica, ESA, USA). Estándar interno: 3,4-dihidroxibencilamina (Sigma-Aldrich, Cat. No. 858781). Estándares externos: L-dopa (Cat. No. 13248) y dopamina (Cat. No. 21992) ambos de Cayman Chemical. Límite de detección: 20 pg/muestra.
F-4) Albuminuria: Se midió con equipo Cobas (ALBT2 Tina-quant Albumin Gen.2; Roche Diagnostics, Suiza); Se determinó la relación Albúmina/Creatinina urinaria, considerando microalbuminuria entre 30-300 mg/g. (14)
F-5) Expresión proteica renal determinada por Western blot: el transportador de aminoácidos y hormona tiroidea LAT2, las proteínas transportadoras de membrana OCT2 y OCTN1,2,3, los receptores dopaminérgicos D1DRy D2DR, el receptor de Ang II AT1R, la sodio-potasio ATPasa Na+K+ATPasa, el factor de crecimiento transformante beta 1 TGF-beta1 y el factor nuclear kappa B1 NFkB1. Control de carga: beta-tubulina. Análisis por densitometría óptica (ImageJ). Debido a que varios de los anticuerpos tienen un peso molecular similar entre sí, se utilizó la técnica de stripping de membrana con ácido acético al 5% luego del revelado del anticuerpo primario a fin de marcar la expresión del control de carga. (Tabla 1)
F-6) Histología renal: Cortes de 8 micrones de espesor teñidos con hematoxilina-eosina, y Sirius Red (15). Fibrosis cortical cuantificada en 20 campos/animal (ImageJ) utilizando un microscopio Nikon Type 104c para obtención de las imágenes. La fibrosis cortical se expresa como: porcentaje de fibrosis (%) = [Σ colágeno intersticial cortical / (Área total – Σ vasos)] × 100.
F-7) Ultraestructura renal; Fragmentos corticales renales de 1 mm3 se destinaron para MET y se observaron con MET Zeiss EM 109T con cámara digital Gatan ES1000W.
Tabla 1
Anticuerpos utilizados para Western blot
| Proteína | Anticuerpo | Dilución | Peso molecular | Proveedor y N° de catálogo |
|---|---|---|---|---|
| D1DR | Policlonal de conejo anti-D1DR | 1:1000 | 50 kDa | Proteintech, número de catálogo 17934-1-AP |
| D2DR | Policlonal de conejo anti-D2DR | 1:600 | 51 kDa | Proteintech, número de catálogo 55084-1-AP |
| OCTN 1,2,3 | Policlonal de conejo anti-OCTN 1,2,3 | 1:2000 | 90 kDa | Santa Cruz Biotechnology, Inc., número de catálogo sc-33534 |
| OCT2 | Policlonal de cabra anti-OCT2 | 1:800 | 50 kDa | Santa Cruz Biotechnology, Inc., número de catálogo sc-19814 |
| LAT2 | Policlonal de cabra anti-LAT2 | 1:800 | 50 kDa | Santa Cruz Biotechnology, Inc., número de catálogo sc-27581 |
| AT1R | Policlonal de conejo anti-AT1R | 1:1000 | 50 kDa | Proteintech, número de catálogo 25343-1-AP |
| Na+K+ATPasa | Policlonal de conejo anti-alfa-1 Na+K+ATPasa | 1:10000 | 105 kDa | Abcam, número de catálogo ab74945 |
| NFkB1 | Policlonal de conejo anti-NFkB1 | 1:1000 | 50 kDa y 105 kDa | Proteintech, número de catálogo 14220-1-AP |
| TGF-beta1 | Policlonal de conejo anti-TGF-beta1 | 1:500 | 44 kDa | Proteintech, número de catálogo 21898-1-AP |
| Beta-tubulina | Policlonal de conejo anti-beta-tubulina | 1:3000 | 50 kDa | Abcam, número de catálogo ab6046 |
Análisis estadístico
Se empleó InfoStat. Test t y ANOVA una vía con Tukey; correlaciones por Pearson y regresión lineal. Los resultados se expresaron como media ± error estándar de la media (ESM), significancia p < 0,05. Gráficos en GraphPad Prism v10.2.3.
Consideraciones éticas
Procedimientos aprobados por CICUAL-UBA (Res. CD N° 1881/1999, director Dr. M. R. Choi), conforme a normas internacionales de ética en experimentación animal.
RESULTADOS
La Tabla 2 muestra que la DG indujo un aumento significativo del peso corporal respecto a C, prevenido por L en DGL. La ingesta de alimento disminuyó en DG frente a C, efecto revertido por L, mientras que la ingesta calórica se incrementó en DG sin diferencias entre DG y DGL. La ingesta de agua no varió entre grupos. Los parámetros plasmáticos mostraron incrementos significativos en DG respecto a C, con reducciones en triglicéridos e insulina en DGL; TyG y HOMA-IR no difirieron entre grupos.
Tabla 2
Peso corporal, ingesta de alimento, bebida y calorías. Parámetros metabólicos plasmáticos.
| Parámetro | C | DG | CL | DGL |
|---|---|---|---|---|
| Peso corporal (g) | 415,7 ± 8,7 | 473,8 ± 14,1* | 389,7 ± 3,8 | 359,13 ± 7,93* |
| Ingesta de alimento (g/24 hs) | 20,9 ± 3,6 | 13,8 ± 1,3† | 28,4 ± 3,5 | 18,6 ± 1,7* |
| Ingesta de agua (mL/24 hs) | 12,5 ± 3,9 | 12,4 ± 0,7 | 20,5 ± 2,7 | 19,1 ± 1,3 |
| Ingesta calórica (kcal/24 hs) | 60,5 ± 10,8 | 103,6 ± 11,5* | 72,4 ± 11,4 | 119,3 ± 11,1 |
| Triglicéridos (mg/dL) | 59,68 ± 6,13 | 119,25 ± 4,17* | 53,20 ± 4,41 | 82,97 ± 6,93* |
| Glucemia (mg/dL) | 117,5 ± 7,5 | 152,2 ± 4,6† | 100,3,3 ± 29,6 | 173,7 ± 14,0* |
| Índice TyG | 8,0 ± 0,2 | 10,5 ± 0,1* | 8,1 ± 0,3 | 10,2 ± 0,2 |
| Insulina (ng/mL) | 1,20 ± 0,10 | 4,20 ± 0,50* | 1,3 ± 0,2 | 2,8 ± 0,4† |
| HOMA-IR | 0,7 ± 0,1 | 3,3 ± 0,5* | 1,5 ± 0,7 | 3,2 ± 0,5 |
Los resultados están expresados como la Media ± ESM. La significancia está expresada como: *p<0,05 C vs DG; †p<0,01 C vs DG; ‡p<0,05 DGL vs DG; §p<0,01 DGL vs DG; C: dieta estándar y agua ad-libitum (SD); CL: C + losartán (L); DG: SD + 50% p/p grasa y agua ad-libitum; DGL: DG + CL; ESM: error estándar de la media HOMA-IR: Evaluación del Modelo Homeostático de la Resistencia a la Insulina; TyG: producto triglicéridos-glucosa
En la Tabla 3, se evidencia cómo la DG elevó la PAS y el índice urinario L-dopa/dopamina respecto a C, efectos atenuados por L en DGL; CL mostró reducción adicional de PAS respecto a C. No se observaron cambios en la relación albúmina/creatinina urinaria ni en TFG. La diuresis, la FENa+ y la UNa+.V disminuyeron en DG, y fueron prevenidas por L en DGL.
Tabla 3
Presion arterial sistolica. Indice urinario L-dopa/dopamina. Parametros plasmaticos y urinarios evaluados de funcion renal
| Parámetro | C | DG | CL | DGL |
|---|---|---|---|---|
| PAS (mmHg) | 120,7 ± 2,3 | 134,8 ± 2,3† | 106,4 ± 2,5 ¶ | 109,5 ± 2,0§ |
| Índice L-dopa/dopamina | 1,1 ± 0,1 | 2,9 ± 0,2† | 1,8 ± 0,1 | 1,8 ± 0,1§ |
| Albumina/Creatinina urinaria (mg/g) | 17,42 ± 1,98 | 12,93 ± 0,66 | 15,31 ± 1,52 | 8,45 ± 1,13 |
| Diuresis (mL/24 hs) | 16,4 ± 2,2 | 3,5 ± 0,3† | 17,28 ± 1,38 | 6,23 ± 0,93‡ |
| TFG (mL/min) | 1,65 ± 0,27 | 1,38 ± 0,11 | 1,77 ± 0,20 | 1,42 ± 0,09 |
| FENa+ (%) | 0,50 ± 0,06 | 0,16 ± 0,02† | 0,51 ± 0,02 | 0,32 ± 0,05‡ |
| UNA+ V (mEq/24 hs) | 1,78 ± 0,18 | 0,45 ± 0,05† | 1,95 ± 0,01 | 0,78 ± 0,10‡ |
Los resultados están expresados como la Media ± SEM. La significancia está expresada como: *p<0,05 C vs DG; †p<0,01 C vs DG; ‡p<0,05 DGL vs DG; §p<0,01 DGL vs DG; ¶p<0,01 CL vs C; ESM: error estándar de la media; FENa: excreción fraccional de sodio; PAS: presión arterial sistólica; UNAV: excreción urinaria de sodio ; TFG: tasa de filtrado glomerular
La tinción con hematoxilina-eosina evidenció vacuolas citoplasmáticas en células tubulares corticales en DG versus C, sin alteraciones en CL respecto a C; con DGL se presentaron vacuolas menores respecto a DG (Figura 1 A a D). La ultraestructura podocitaria mostró acortamiento y fusión de pedicelos en DG, prevenido por L en DGL, sin diferencias entre CL y C (Figura 1 E a H).
Fig. 1.
Estructura y ultraestructura de la corteza renal
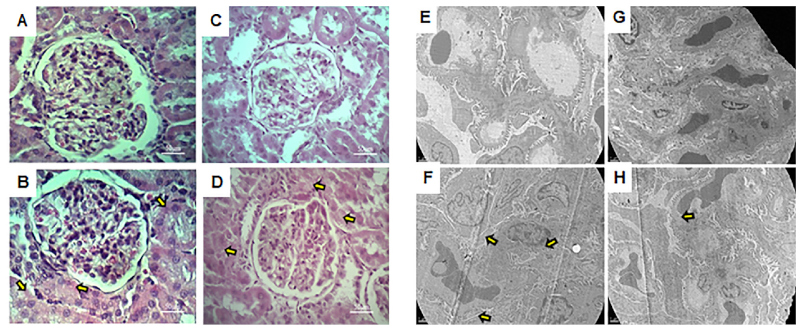
Fotos A, B, C, y D: Microscopia óptica con tinción de hematoxilina y eosina, aumento total: 400X. Fotos E, F, G, y H: Microscopia electrónica de transmisión, aumento total: 7000X. Nomenclatura: A-E: grupo C. B-F: grupo DG. C-G: grupo CL. D-H: grupo DGL. En A, B, C y D las flechas amarillas apuntan a las vacuolas citoplasmáticas de las células tubulares. En E, F, G y H, las flechas amarillas señalan a los pedicelos de los podocitos con morfología alterada.
La DG sobreexpresó AT1R y redujo la proteína transportadora de membrana OCTN1,2,3, respecto al C, mientras que L previno dicha disminución. También L previno la sobreexpresión del receptor dopaminérgico D1DR en DGL respecto de DG y, D2DR disminuido en DG, no se modificó con L. LAT2 y OCT2 no variaron entre grupos. La Na+K+ATPasa se incrementó en DG, pero L la mantuvo en valores normales en DGL respecto de DG (Figura 2).
Fig. 2.
Expresión de proteínas del SDR y SRA en corteza renal por Western blot.
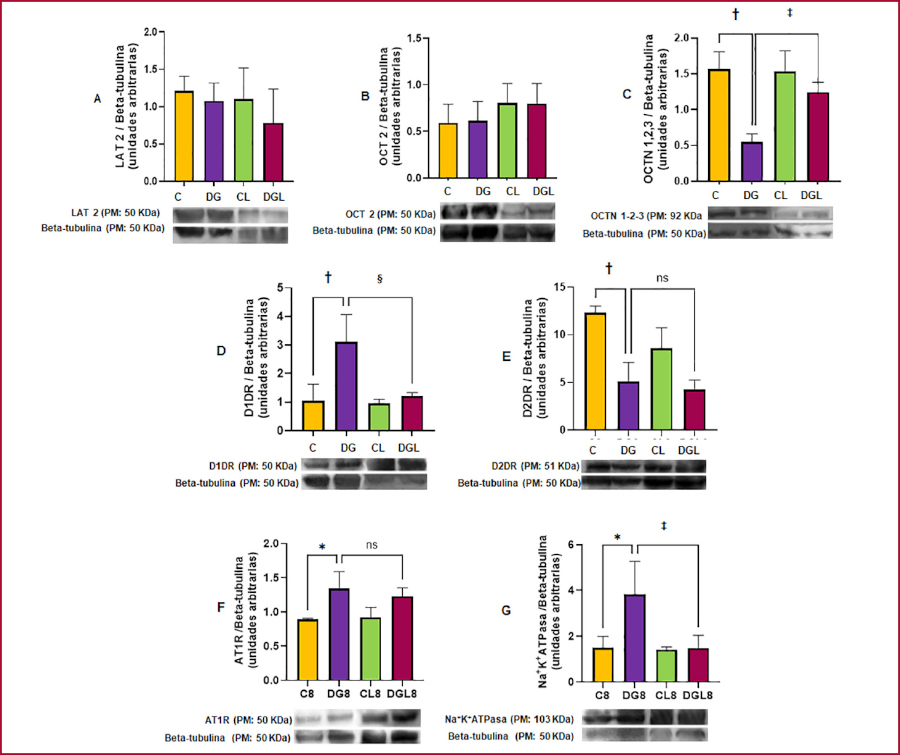
A: LAT2. B: OCT 2. C: OCTN 1,2,3. D: D1DR. E: D2DR. F: AT1R. G: Na'K'ATPasa. Los resultados están expresados como la media ± ESM. La significancia está expresada como: *p<0,05 C vs DG; †p<0,01 C vs DG; ‡p<0,05 DGL vs DG; §p<0,01 DGL vs DG, C: control; CL: C + losartán; DG: dieta grasa; DGL: DG + CL; ESM: error estándar de la media; SDR: sistema dopaminérgico renal; SRA: sistema angiotensina. Resto de las abreviaturas ver el texto.
El índice L-dopa/dopamina correlacionó positivamente con PAS, insulinemia y D1DR, e inversamente con la UNa+.V y OCTN1,2,3. L previno dichas alteraciones en DGL comparado con DG (Figura 3).
Fig. 3.
Correlaciones funcionales con el índice L-dopa/dopamina
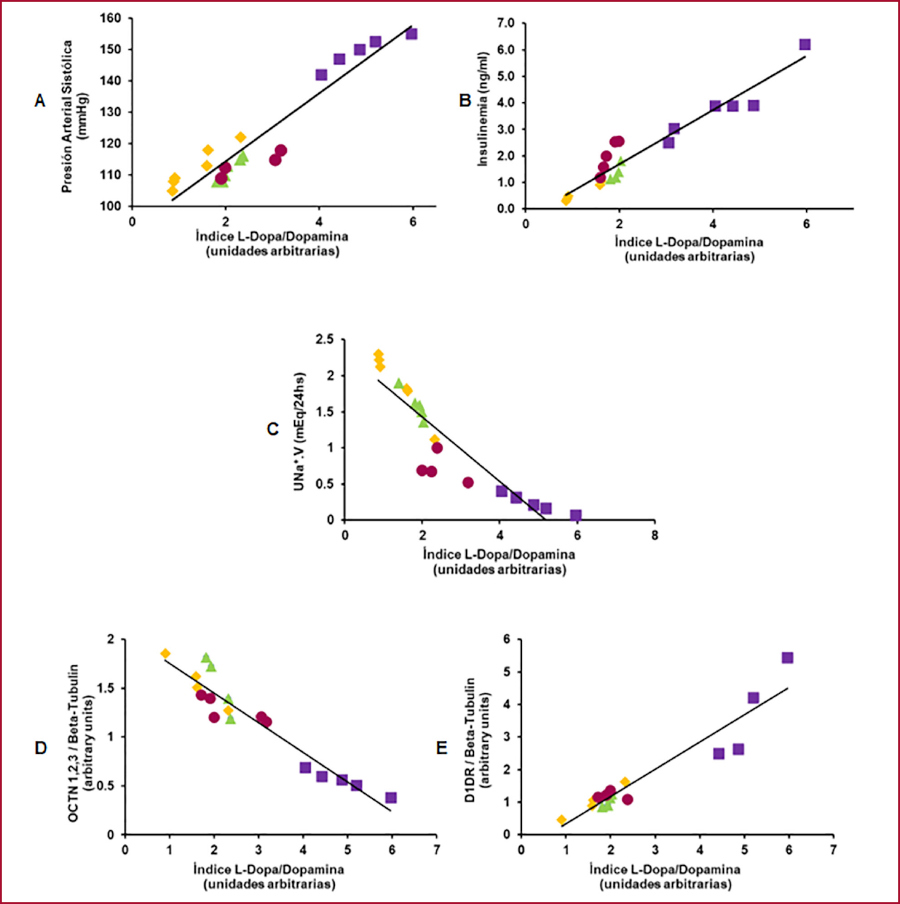
A: Regresión lineal PAS versus índice L-dopa/DA; r = 0,95, R2 = 0,90, p<0,01; B: Regresión lineal Insulínemia versus índice L-dopa/DA; r = 0,96, R2 = 0,91, p<0,01. C: Regresión lineal de UNA'.V versus índice L-dopa/DA; r = 0,91, R2 = 0,83, p<0,01; D: Regresión lineal OCTN 1,2,3 versus índice L-dopa/dopamina; r = 0,95, R2 = 0,91, *p<0,01; E: Regresión lineal D1DR versus índice L-dopa/dopamina; r = 0,95, R2 = 0,89, *p<0,05 Código de grupos y colores: C: Amarillo. DG: Violeta. CL: Verde. DGL: Bordó.
La DG aumentó significativamente la expresión de NFkB1 y TGF-beta1, efectos que fueron prevenidos por L en DGL. La fibrosis intersticial se incrementó en DG frente a C, y L lo previno significativamente en DGL respecto a DG, con focos residuales, sin cambios en CL respecto a C. El análisis semicuantitativo confirmó estos hallazgos (Figura 4).
Fig. 4.
Evaluación de marcadores de inflamación en la corteza renal por Western blot y determinación del porcentaje de fibrosis por histología con tinción de Sirius red.
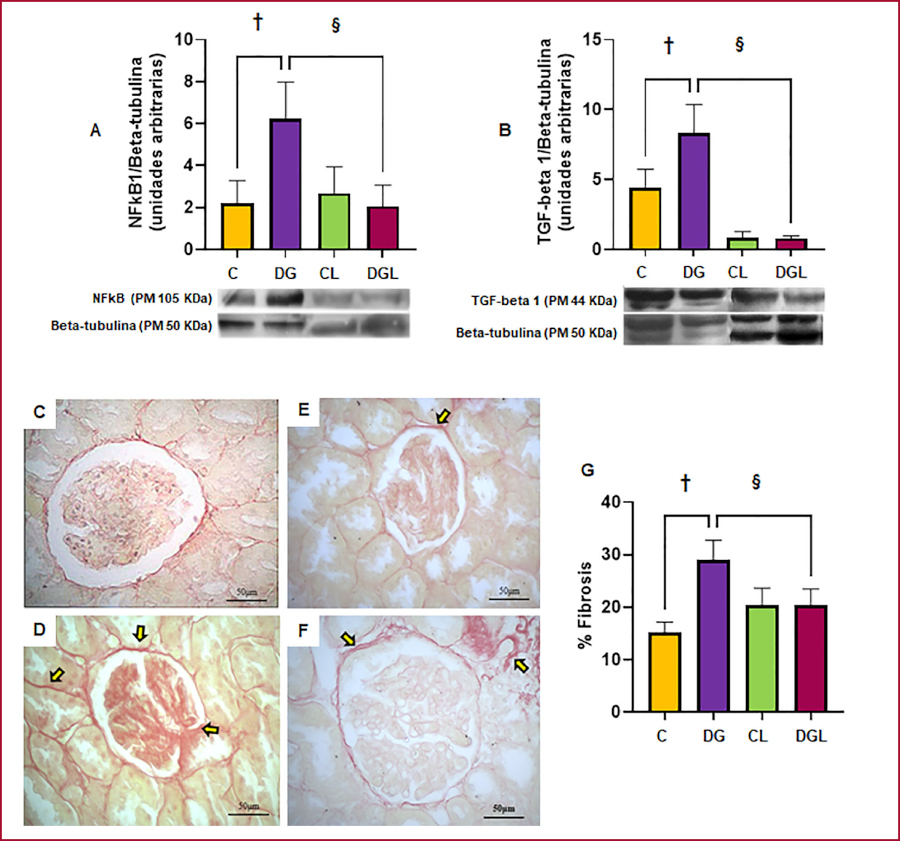
Gráficos: A: NFkB1. B: TGF-beta1. Los resultados están expresados como la Media ± ESM. La significancia está expresada como; 1p<0,01 C vs DG; 1p<0,01 DGL vs DG. Foto C: grupo C. Foto D: grupo DG. Foto E: grupo CL. Foto F: grupo DGL. Gráfico G: porcentaje de fibrosis. Las flechas amarillas apuntan a los sitios de incremento en la fibrosis intersticial. Aumento total: 400X Los resultados están expresados como la Media ± ESM. La significancia está expresada como: 1p<0,01 C vs DG; 1p<0,01 DGL vs DG.
DISCUSIÓN
El consumo de DG incrementó significativamente el peso corporal respecto del C, efecto que fue prevenido por L. Aunque la ingesta de alimento fue menor en DG, la densidad calórica de la dieta resultó en un 33 % más de calorías consumidas, lo que explica el aumento en el peso corporal, en concordancia con lo reportado por Pinhal et al. (16) Nuestros resultados coinciden con Smith et al. (17), quienes describieron un efecto reductor de L sobre peso corporal, sugiriendo un rol modulador del antagonismo AT1 en la obesidad inducida por DG. Asimismo, Hosseini et al. (18) sugirieron que el L puede mejorar la resistencia a la leptina y modular el peso corporal en condiciones de obesidad inducida por la dieta. La ingesta de agua no difirió entre grupos y la administración de L en agua de bebida, validada previamente, (19) evitó el sesgo asociado al gavage (alimentación forzada) crónico.
El perfil metabólico mostró resistencia a la insulina en DG respecto de C, con aumento de triglicéridos, glucemia, insulina, TyG y HOMA-IR, en concordancia con reportes previos en modelos de SM inducido por DG. (18) L atenuó parcialmente triglicéridos e insulina, sin modificar glucemia ni los índices, mientras que CL no difirió de C. Estos hallazgos coinciden con literatura que vincula las alteraciones metabólicas causadas por DG y los efectos beneficiosos de L, que propusieron que este efecto podría deberse a la reducción del estrés oxidativo vía activación de superóxido dismutasa (SOD), aunque el mecanismo preciso permanece incierto. (17,20)
La DG incrementó significativamente la PAS respecto de C, en concordancia con lo evidenciado por Jin et al. y Li et al. (21,22) quienes demostraron que la DG induce obesidad, resistencia a la insulina e hiperinsulinemia, acompañadas de activación del SRA, aumento de Ang II, aldosterona y expresión de AT1R, junto con inflamación y fibrosis renal. En nuestro modelo, la administración concomitante de L previno el aumento de PAS en DGL frente a DG, efecto atribuible a su acción antagonista sobre AT1R. (16) Además, L redujo significativamente la PAS en controles normotensos (CL), en línea con lo reportado por Lee et al. (19) Li et al. (22) describieron un efecto alostérico de L sobre AT1R, que potencia la actividad de D1DR contribuyendo a su acción antihipertensiva.
La TFG no mostró diferencias entre los grupos. Resultados similares fueron reportados por Roza et al. (23) en ratones tratados con DG a 8 y 12 semanas. Asimismo, otros grupos reportaron incrementos asociados a hiperfiltración glomerular en animales obesos. (24,25) Estos hallazgos sugieren que el efecto de las DG sobre el TFG es variable. El tratamiento con L tampoco modificó este parámetro entre los grupos evaluados.
La relación albúmina/creatinina urinaria, más confiable que los valores absolutos de los metabolitos por separado, no superó 30 mg/g en ningún grupo, descartando microalbuminuria. L no modificó este marcador, sugiriendo que las alteraciones derivan de la dieta y no del fármaco. En contraste, Sánchez-Navarro et al. (26) reportaron aumento significativo bajo DG de mayor duración, lo que indica que el tiempo de exposición podría ser determinante.
La DG redujo la diuresis versus C, como informó Sánchez-Navarro et al. (26), posiblemente por una menor actividad del SDR y mayor del SRA. (10) L previno esta reducción en DGL, sugiriendo restauración de la función del SDR por bloqueo de AT1R. (22) Asimismo, la FENa+ y la UNa+.V se redujeron en DG, prevenidas parcialmente por L en DGL, aunque sin alcanzar valores de CL, indicando la posible participación de mecanismos de reabsorción de sodio independientes de la Na+K+ATPasa como el intercambiador Na+/H+ o el canal de sodio epitelial ENaC. (27,28) Resultados previos muestran disparidad: Roza et al. (23) no observaron cambios, mientras que Pinhal et al. (16) reportaron disminuciones de FENa+ y UNa+.V en obesidad o DG prolongada. La DG se asocia así con las alteraciones observadas, y L ejerce un efecto preventivo parcial.
Histológicamente, la DG indujo vacuolas citoplasmáticas en los TCP, ausentes en C, parcialmente prevenidas por L en DGL, sin cambios en CL. Aunque las tinciones para lípidos fueron negativas, la literatura sugiere que podrían corresponder a vacuolas lipídicas, (4,29) o a degeneración hidrópica por disfunción de Na+K+ATPasa asociada a lipotoxicidad, (30) atenuada por L mediante reducción de inflamación y estrés oxidativo. (19) El estudio ultraestructural al MET mostró borramiento e interdigitación de pedicelos e hipertrofia podocitaria en DG, prevenidos parcialmente por L, lo que concuerda con el rol nefroprotector de la dopamina (31) y el efecto dañino de Ang II sobre AT1R. (32)
El SM inducido por DG se asocia con HTA a través de la activación del SRA, en particular por la acción de Ang II sobre AT1R, que estimula la bomba Na+K+ATPasa, favoreciendo la retención de sodio y reduciendo su excreción. (1,22) De manera concomitante, la DG inhibe la actividad del SDR, potenciando el efecto anti-natriurético. Existe una reciprocidad negativa entre AT1R y D1DR en células de tubo contorneado proximal (TCP), donde la activación de uno induce la internalización y abolición de la señalización del otro, actuando como una unidad de opuestos junto con la Na+K+ATPasa como diana común. (33) En humanos normotensos, se ha demostrado una interacción negativa entre SDR y SRA en la regulación del transporte renal de sodio, dependiente de la ingesta de este ión. (34) La DG incrementó la expresión renal de AT1R respecto de C, en concordancia con modelos de SM y activación del SRA. (21) L no previno su sobreexpresión en DGL, aunque mostró tendencia a reducción, sugiriendo que tiempos mayores podrían ser necesarios para evidenciar el efecto. En cambio, L normalizó el índice L-dopa/dopamina, incrementado en DG vs. C, (35) evidenciando mayor disponibilidad de dopamina tubular y excreción urinaria, asociada a restauración de transportadores OCTN1,2,3. LAT2 y OCT2 no se modificaron, en contraste con la sobrecarga de fructosa. (35) La DG aumentó D1DR, prevenido por L, y redujo D2DR, sin cambios por L, reflejando alteración dopaminérgica renal (36). La DG aumentó significativamente la Na+K+ATPasa cortical respecto de C, hallazgo coincidente con Deji et al. (9,37). L previno este incremento en DGL, sin modificar valores basales (CL vs. C), efecto explicado por su acción alostérica sobre AT1R–D1DR. (21)
El índice L-dopa/dopamina se correlacionó positivamente con PAS e insulina, y negativamente con UNa+.V y OCTN1,2,3, lo que vincula directamente al SDR con la regulación de presión arterial y el balance de sodio, en interacción con resistencia a la insulina. (38) L normalizó estas correlaciones mediante bloqueo de AT1R e inhibición de Na+K+ATPasa. En conjunto, los resultados destacan el desequilibrio SDR/SRA inducido por DG y el potencial de L para prevenir la disfunción renal y hemodinámica asociada.
En cuanto a la inflamación, el SDR ejerce efectos antiinflamatorios, mientras que el SRA los potencia. (10,39) La dopamina renal, vía D1DR y D2DR, atenúa los efectos de Ang II reduciendo inflamación y fibrosis (16). En contraste, la DG indujo un ambiente proinflamatorio con sobreexpresión de NFkB1 y TGF-beta1, incremento de fibrosis intersticial y activación de vías oxidativas. (3,11,39). L previno estos cambios al bloquear Ang II y permitir la acción protectora del SDR reduciendo la fibrosis, el estrés oxidativo. (40)
En conclusión, el tratamiento preventivo y continuo con L atenuo significativamente la actividad del SRA y reactivó el SDR. La inhibición de AT1R por losartán redujo la acción de la Na+K+ATPasa y normalizó la expresión de D1DR, al tiempo que restableció los niveles de los transportadores OCTN1,2,3, favoreciendo el acceso de dopamina a la luz tubular. En consecuencia, aumentó la excreción urinaria de dopamina, se normalizó el índice L-dopa/dopamina y se potenció la interacción con D1DR, promoviendo la natriuresis y el restablecimiento del equilibrio SDR-SRA. Además, L mejoró la fibrosis intersticial, generó un entorno renal antiinflamatorio y preservó la estructura de los TCPs y la ultraestructura podocitaria.
LIMITACIONES
Dentro de las limitaciones del presente estudio podría mencionarse que la expresión de la bomba Na+K+ATPasa se determinó en forma total, sin discriminar entre la forma fosforilada o activa de la no fosforilada o inactiva. Asimismo, no se determinó la actividad de este transportador, basados en antecedentes propios del grupo de trabajo donde se demostró en un modelo de sobrecarga de fructosa y tratamiento con L, que no presentaba variaciones entre los diferentes grupos experimentales.
Por otra parte, no se pudo llevar a cabo la técnica de inmunohistoquímica tanto de los transportadores como de los receptores del SDR, lo cual hubiera brindado información acerca de la ubicación celular de las distintas proteínas, que se relacionaría directamente con la funcionalidad de dichas proteínas.
Como complemento de la MET, hubiera sido deseable determinar la expresión de nefrina y de podocalixina como marcadores estructurales de la integridad de la barrera de filtración glomerular, como así también, la determinación de la expresión de IL-6 como marcador agudo de inflamación complementario al NFkB1.
Está previsto realizar estas determinaciones a futuro a fin de completar el perfil correspondiente.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
(Véase formularios de conflictos de interés de los autores en la Web).
Financiamiento
El financiamiento provino de subsidios de investigación: 2014-2016: Proyecto BA105 / 2014–2017: Proyecto 20020130100019BA / 2018–2020 (prorrogado hasta 2022): Proyecto 20020170100621BA.
