La insuficiencia cardíaca aguda (ICA) representa uno de los principales motivos de hospitalización en todo el mundo, con elevada morbimortalidad posalta. (1) A pesar de los avances terapéuticos, la persistencia de signos de congestión al momento del egreso es frecuente y continúa siendo el predictor más importante y modificable de rehospitalización precoz, eventos adversos y mortalidad. (2,3) Esta congestión, muchas veces subclínica, pasa inadvertida al examen físico tradicional, lo que subraya la necesidad de herramientas más sensibles y reproducibles.
Los métodos tradicionales de evaluación para definir el momento del alta, como los cambios de peso o el examen físico, se han mostrado insuficientes para determinar una descongestión adecuada, como lo reflejan las elevadas tasas de rehospitalización dentro de los 30 días del alta. (4) En la práctica, la percepción de “estabilidad clínica” no siempre equivale a una verdadera descongestión, lo que refuerza la necesidad de incorporar mediciones objetivas y reproducibles.
Históricamente, la evaluación clínica ha sido el pilar de las decisiones terapéuticas. Sin embargo, múltiples estudios han demostrado su escasa sensibilidad y capacidad para predecir eventos. La congestión subclínica al momento del alta hospitalaria puede estar presente hasta en el 40% de los pacientes, incluso en aquellos que se consideran clínicamente “compensados”. (5) Esta disociación entre la clínica y la congestión real dio origen al concepto de congestión subclínica y puso en duda la confiabilidad del examen físico como único criterio para definir el alta hospitalaria.
Alcanzar una descongestión adecuada constituye el objetivo terapéutico central durante la hospitalización por insuficiencia cardíaca aguda. Más allá del alivio sintomático, la euvolemia proporciona la base fisiológica que permite tolerar e intensificar las terapias modificadoras del pronóstico. Sin embargo, definir y cuantificar la congestión continúa siendo desafiante, ya que puede manifestarse como congestión intravascular, tisular o ambas, cada una con diferente perfil diagnóstico y terapéutico. (6)
Frente a esta limitación, se han desarrollado herramientas complementarias. Los biomarcadores como el NT-proBNP (fragmento aminoterminal del péptido natriurético tipo B), si bien útiles para diagnóstico y pronóstico, presentan limitaciones como guías terapéuticas durante la fase aguda. Ensayos clínicos como GUIDE-IT y PRIMA II demostraron que la estrategia de tratamiento guiada exclusivamente por niveles de NT-proBNP no logró reducir la mortalidad o las rehospitalizaciones. (7,8) Otros biomarcadores –como el CA-125 (antígeno de cáncer 125), el sST2 (la forma soluble del receptor ST2, supresión de la tumorigénesis tipo 2) o la bio-ADM (adrenomedulina biólogicamente activa)– han sido propuestos como marcadores dinámicos de sobrecarga de volumen, especialmente en el entorno ambulatorio, aunque su uso clínico e implementación aún son limitados. (9,10)
En los últimos años, el foco se ha desplazado hacia herramientas no invasivas. La ecografía pulmonar (LUS) permite detectar líneas B indicativas de congestión pulmonar con sensibilidad superior a la radiografía de tórax. (11) De forma complementaria, la ecografía de la vena cava inferior (VCI) y la evaluación Doppler de venas hepáticas, porta y renales mediante el protocolo VExUS permiten objetivar la congestión sistémica intravascular. (12-14) Más recientemente, el monitoreo remoto dieléctrico (ReDS) mostró resultados alentadores para el manejo de la descongestión en pacientes hospitalizados en un ensayo clínico. (15) Estos métodos, accesibles y reproducibles, han demostrado valor pronóstico en múltiples cohortes.
En este contexto, nuestro grupo desarrolló el estudio CAVAL US-AHF (CAVA and Lung UltraSound-guided therapy in Acute Heart Failure), (16,17) un ensayo clínico aleatorizado, unicéntrico, realizado en Argentina, que incluyó pacientes hospitalizados por ICA. Todos los pacientes recibieron una evaluación protocolizada de LUS y VCI al ingreso, durante la internación y al alta, realizada por médicos entrenados que no participaban en las decisiones terapéuticas. Las imágenes fueron analizadas e informadas a los médicos tratantes por un core lab externo ciego a la asignación y al paciente. La congestión se clasificó en tres categorías (A, B o C) según los hallazgos ecográficos reportados previamente en la literatura que se asociaban a mayor riesgo de hospitalización o mortalidad luego del alta. Los pacientes fueron asignados al azar y estratificados por edad y fracción de eyección del ventrículo izquierdo a dos grupos: a) grupo control, con manejo estándar basado en clínica, síntomas y laboratorio, y b) grupo intervención (CAVAL US), con atención estándar más ajuste terapéutico guiado por protocolo LUS + VCI. El algoritmo de intervención consideró clínica, número de líneas B (en 8 zonas) y parámetros de la VCI (diámetro y colapsabilidad). Los médicos del grupo intervención accedían a los hallazgos ecográficos, mientras que los del grupo control permanecían cegados.
Previo al alta hospitalaria, se aplicó un checklist sistemático para asegurar el cumplimiento del tratamiento basado en guías, vacunación, educación y planificación del seguimiento. Todos los pacientes recibieron consejería estructurada con entrega de material educativo y un esquema escrito de tratamiento farmacológico. En ambos grupos se programaron controles ambulatorios a los 7-10 días del alta y posteriormente al menos una vez al mes.
El punto final primario de congestión subclínica al alta (>5 líneas B y/o VCI dilatada) se observó en 13,3% del grupo CAVAL US versus 66,6% en el grupo control (p<0,001), una reducción relativa del 80%. Asimismo, se redujo el punto final combinado a 90 días (reinternación, consulta no programada o muerte: 13,3% vs. 36,7%; p=0,038). Esta intervención además fue segura y no implicó mayor duración de hospitalización.
Recientemente, la Heart Failure Association (HFA) de la European Society of Cardiology (ESC) propuso un algoritmo multiparamétrico para evaluar la descongestión al alta, que incluye tres criterios: <5 líneas B en LUS, VCI <21 mm con colapsabilidad >50%, y reducción >30% del NT-proBNP respecto al ingreso. (3) Estos criterios fueron establecidos acorde a estudios pronósticos de los últimos años y consenso de expertos. Sobre esta base, realizamos un substudio recientemente publicado en European Journal of Heart Failure. (18) Según los criterios propuestos por la HFA-ESC, los pacientes fueron clasificados en dos grupos: descongestión óptima (VCI <21 mm y colapsabilidad >50%, <5 líneas B en LUS de 8 zonas, y reducción >30% del NT-proBNP) y no óptima (falla en cumplir cualquiera de los tres). El punto final primario fue el compuesto de rehospitalización por IC, consulta urgente por empeoramiento o muerte a 90 días post alta. El 45% alcanzó los tres criterios de descongestión óptima. Ninguno de ellos presentó eventos durante el seguimiento a 90 días, mientras que el 42,4% de los pacientes con descongestión no óptima alcanzó el punto final primario (p<0,001). No hubo diferencias significativas entre grupos en la dosis de furosemida al alta, fracción de eyección ni uso de tratamiento médico guiado por guías, lo que sugiere que la congestión residual puede persistir independientemente de la evaluación clínica o la intensidad terapéutica. Este análisis aporta evidencia prospectiva que valida el valor pronóstico del algoritmo multiparamétrico de la HFA-ESC y refuerza la aplicabilidad de una estrategia de descongestión guiada y objetiva en un escenario de práctica clínica cotidiana.
La incorporación de herramientas complementarias no representa una sofisticación innecesaria, sino una evolución hacia una medicina más precisa y reproducible. La congestión subclínica es frecuente y su persistencia tras el alta continúa siendo uno de los principales determinantes de eventos adversos. En este contexto, la integración de la ecografía pulmonar y de vena cava inferior con biomarcadores accesibles ofrece una estrategia objetiva, factible y de alto impacto clínico, especialmente en sistemas de salud con limitaciones de recursos.
La descongestión efectiva no se logra solo con diuréticos. La retención de sodio refleja una activación neurohormonal e inflamatoria que exige la introducción temprana y completa del tratamiento modificador del pronóstico –ARNI (inhibidores de la neprilisina y receptor de la angiotensina), los betabloqueantes, ARM (antagonistas de los receptores mineralocorticoides) y los i SGLT2 (inhibidores del cotransporte sodio glucosa 2–. (19) El ensayo STRONG-HF demostró que una titulación intensiva de ARNI, betabloqueantes y ARM en las primeras semanas post-alta no solo fue segura, sino que redujo significativamente la mortalidad y las rehospitalizaciones (20) En un subanálisis de este ensayo la titulación intensiva del bloqueo neurohormonal se asoció con una descongestión más eficiente y sostenida a 90 días, junto con una reducción significativa del riesgo del punto final primario. (21)
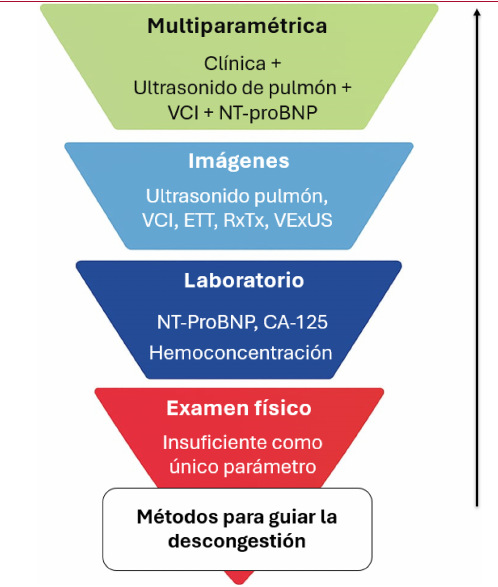
La descongestión guiada en insuficiencia cardíaca aguda debe ser precisa, integral y reproducible. La integración de múltiples herramientas objetivas sumado a criterios clínicos ofrece una sinergia diagnóstica para alcanzar ese objetivo. Como ilustra la Figura 1, cada uno de estos pilares aporta información complementaria para evaluar la congestión de forma multiparametrica. La Tabla 1 propone un decálogo clínico que resume los principios de esta nueva práctica, integrando evidencia y experiencia.
Alcanzar una descongestión completa antes del alta hospitalaria es un paso decisivo para reducir hospitalizaciones y mejorar resultados clínicos. La congestión residual al egreso sigue siendo uno de los predictores más sólidos de mortalidad y eventos adversos, por lo que su detección debería integrarse al estándar de atención. Sin embargo, la evaluación óptima de la descongestión y la manera de guiar el tratamiento aún no están completamente definidas ni estandarizadas.
Tabla 1
Decálogo de la congestión en ICA
| 1. La congestión es el predictor clave de eventos posalta. |
| 2. La congestión subclínica es frecuente y se asocia con mayor riesgo de eventos. |
| 3. El examen físico aislado no es suficiente. |
| 4. La evaluación de la congestión debe ser multiparamétrica. |
| 5. El algoritmo HFA-ESC ofrece un marco objetivo. |
| 6. Los diuréticos son necesarios, pero no suficientes. |
| 7. El tratamiento médico dirigido por guías (TMDG) es parte esencial de la descongestión. |
| 8. Descongestionar no es lo mismo que “sacar agua”. |
| 9. La fase vulnerable es una ventana de oportunidad. |
| 10. Validar estrategias de descongestión en nuestro medio es posible y necesario. |
La literatura reciente coincide en que ningún parámetro aislado es suficiente. Por ello, se recomienda una valoración multiparamétrica que combine herramientas clínicas, ecográficas y de laboratorio, todas disponibles, reproducibles y de bajo costo relativo. En sistemas de salud como los de Latinoamérica, donde la presión por el alta precoz es frecuente y los recursos suelen ser limitados, la integración de ecografía pulmonar, evaluación de la vena cava inferior y biomarcadores representa una estrategia objetiva, segura y factible, capaz de mejorar la toma de decisiones y los resultados clínicos.
En este contexto, el estudio CAVAL US-AHF y su subestudio demuestran que es posible implementar modelos de atención basados en evidencia, simples y efectivos, que redefinen cómo evaluamos la congestión y el momento óptimo del alta. El verdadero cambio de paradigma radica en incorporar esta mirada integral como parte del estándar asistencial. Pasar de “tratar la descompensación” a “garantizar la descongestión completa” antes del alta representa una transición hacia una medicina más precisa, reproducible y orientada a resultados.
Declaración de conflicto de intereses
Los autores declaran que no tienen conflicto de intereses. (Véanse formularios de conflicto de intereses de los autores en la Web)
Financiamiento
Este trabajo no recibió financiamiento público ni privado.
BIBLIOGRAFÍA
1. Rubio-Gracia J, Demissei BG, ter Maaten JM, Cleland JG, O'Connor CM, Metra M, et al. Prevalence, predictors and clinical outcome of residual congestion in acute decompensated heart failure. Int J Cardiol. 2018;258:185-191. https://doi.org/10.1016/j.ijcard.2018.01.067
2. Gheorghiade M, Vaduganathan M, Fonarow GC, Bonow RO. Rehospitalization for heart failure: problems and perspectives. J Am Coll Cardiol. 2013;61:391-403. https://doi.org/10.1016/j.jacc.2012.09.038
3. Metra M, Adamo M, Tomasoni D, Mebazaa A, Bayes-Genis A, Abdelhamid M, et al. Pre-discharge and early post-discharge management of patients hospitalized for acute heart failure: a scientific statement by the Heart Failure Association of the ESC. Eur J Heart Fail. 2012;23:1201-1222. https://doi.org/10.1002/ejhf.2888
4. Felker GM, Whellan DJ. Inpatient management of heart failure: are we shooting at the right target? Ann Intern Med. 2017;166:223-224. https://doi.org/10.7326/M16-2667
5. Rivas-Lasarte M, Maestro A, Fernández-Martínez J, López-López L, Solé-González E, Vives-Borrás M, et al. Prevalence and prognostic impact of subclinical pulmonary congestion at discharge in patients with acute heart failure. ESC Heart Fail. 2020;7:2621-2628. https://doi.org/10.1002/ehf2.12842
6. George J, Wilson Tang WH. Evolving Decongestion Strategies in the Management of Acute Heart Failure. Curr Treat Options Cardiovasc Med. 2025;27:71. https://doi.org/10.1007/s11936-025-01125-y
7. Ibrahim NE, Januzzi JL. The future of biomarker-guided therapy for heart failure after the GUIDE-IT study. Curr Heart Fail Rep. 2018;15:37-43. https://doi.org/10.1007/s11897-018-0381-0
8. Stienen S, Salah K, Moons AH, Bakx AL, van Pol P, Kortz RA, et al. NT-proBNP-guided therapy in acute decompensated heart failure: PRIMA II randomized controlled trial. Circulation. 2018;137:1671-1683. https://doi.org/10.1161/CIRCULATIONAHA.117.029882
9. Núñez J, Núñez E, Sanchis J, Bodi V, Miñana G, Mainar L, et al. Antigen carbohydrate 125: an emerging prognostic risk biomarker in acute heart failure? Heart. 2007;93:716-721. https://doi.org/10.1136/hrt.2006.096016
10. Maisel AS, Mueller C, Adams K, Anker SD, Aspromonte N, Cleland JG, et al. State of the art: using biomarkers in heart failure clinical practice. Eur J Heart Fail. 2008;10:824-839. https://doi.org/10.1016/j.ejheart.2008.07.014
11. Platz E, Merz AA, Jhund PS, Vazir A, Campbell RT, McMurray JJ. Dynamic changes and prognostic value of pulmonary congestion by lung ultrasound in acute and chronic heart failure: a systematic review. Eur J Heart Fail. 2017;19:1154-1163. https://doi.org/10.1002/ejhf.839
12. Pellicori P, Platz E, Dauw J, Martens P, Verbrugge FH, Nijst P, et al. Ultrasound imaging of congestion in heart failure: examinations beyond the lung. Eur J Heart Fail. 2021;23:703-712. https://doi.org/10.1002/ejhf.2032
13. Llàcer P, Romero G, Trullàs JC, de la Espriella R, Cobo M, Quiroga B, et al. Consensus on the approach to hydrosaline overload in acute heart failure. SEMI/SEC/S.E.N. recommendations. Rev Esp Cardiol (Engl Ed). 2024;77:556-565. https://doi.org/10.1016/j.rec.2024.01.003
14. Anastasiou V, Peteinidou E, Moysidis DV, Daios S, Gogos C, Liatsos AC, et al. Multiorgan Congestion Assessment by Venous Excess Ultrasound Score in Acute Heart Failure. J Am Soc Echocardiogr. 2024;37:923-933. https://doi.org/10.1016/j.echo.2024.05.011
15. Alvarez-Garcia J, Lala A, Rivas-Lasarte M, De Rueda C, Brunjes D, Lozano-Jimenez S, et al. Remote Dielectric Sensing Before and After Discharge in Patients With AHF: The ReDS-SAFE HF Trial. JACC Heart Fail. 2024;12:695-706. https://doi.org/10.1016/j.jchf.2024.01.002
16. Burgos LM, Baro Vila RC, Ballari FN, Goyeneche A, Costabel JP, Muñoz F, et al. Inferior vena CAVA and lung UltraSound-guided therapy in acute heart failure: a randomized pilot study (CAVAL US-AHF Study). Am Heart J. 2024;277:47-57. https://doi.org/10.1016/j.ahj.2024.07.015
17. Burgos LM, Baro Vila R, Goyeneche A, Muñoz F, Spaceavento A, Fasan MA, et al. Design and rationale of the inferior vena CAVA and Lung UltraSound-guided therapy in Acute Heart Failure (CAVAL US-AHF Study): a randomised controlled trial. Open Heart. 2022;9:e002105. https://doi.org/10.1136/openhrt-2022-002105
18. Burgos LM, Baro Vila R, Goyeneche A, Costabel JP, Spaceavento A, Fasan MA, et al. Residual congestion defined by HFA-ESC multiparametric criteria and 90-day outcomes in worsening heart failure. Eur J Heart Fail. 2025;27:1866-1867. https://doi.org/10.1002/ejhf.70004
19. Burgos LM, Fairman E, Gould N. Insuficiencia cardíaca descompensada: los diuréticos son necesarios, pero no suficientes. Rev Argent Cardiol. 2025;93(6):402-404. https://doi.org/10.7775/rac.es.v84.i6.10084
20. Mebazaa A, Davison B, Chioncel O, Cohen-Solal A, Diaz R, Filippatos G, et al. Safety, tolerability and efficacy of up-titration of guideline-directed medical therapies for acute heart failure (STRONG-HF): a multinational, open-label, randomised trial. Lancet. 2022;400:1938-1952. https://doi.org/10.1016/S0140-6736(22)02076-1
21. Biegus J, Mebazaa A, Davison B, Cotter G, Edwards C, Čelutkienė J, et al. Effects of Rapid Uptitration of Neurohormonal Blockade on Effective, Sustainable Decongestion and Outcomes in STRONG-HF. J Am Coll Cardiol. 2024;84:323-336. https://doi.org/10.1016/j.jacc.2024.04.055
HTML generado desde un xml-jats a través de la plantilla jats-rac.xsl por RevisCiencia. El motor utilizado es Apache Software Foundation (Xalan XSLTC).