Afección coronaria en síndrome inflamatorio multisistémico post-COVID. Reporte de un caso
El síndrome inflamatorio multisistémico en niños asociado con enfermedad por coronavirus 2019 (SIM-C) se define por la presencia de fiebre persistente, inflamación y disfunción orgánica, con evidencia de infección pasada o reciente por coronavirus tipo 2 del síndrome respiratorio agudo grave, y exclusión de otra causa microbiana. Acarrea la superposición con otras enfermedades inflamatorias (enfermedad de Kawasaki y síndrome de shock tóxico). (1)
La Sociedad Argentina de Pediatría segmenta la presentación clínica del síndrome en dos fenotipos: a) enfermedad tipo Kawasaki (EK), completa o incompleta, y b) cuadro no específico, niños que presentan shock y/o fiebre y síntomas gastrointestinales, respiratorios o neurológicos, que no cumplen con los criterios para la EK. (2)
En distintos reportes internacionales el compromiso cardiovascular tuvo una alta incidencia. La clínica de shock se dio en el 43%, la afección miocárdica con elevación enzimática entre el 31% y el 50%, y la disfunción ventricular izquierda evaluada por ecocardiograma en el 42%. Las anomalías en las arterias coronarias se presentaron en el 18,5% de los casos. (1,2,3)
El tratamiento general es de sostén, mientras que el específico consiste en agentes inmunomoduladores. Para ambos subtipos, la inmunoglobulina endovenosa (Ig IV) es el tratamiento de primera línea. La segunda línea son los corticoides sistémicos; en los pacientes con fenotipo de EK menores de 12 meses o con afección coronaria, la primera y segunda líneas se administran conjuntamente. La tercera línea son los agentes biológicos. (1,5,6)
Nuestro objetivo es presentar un caso clínico con dilatación coronaria por síndrome inflamatorio multisistémico post COVID-19 tratado en el Hospital del Niño Jesús de Tucumán.
Paciente de 1 año, de 8,6 kg de peso y 77 cm de talla, previamente sano, con antecedente de COVID-19 positivo en un tío materno 14 días antes. Inicia con congestión de vías aéreas superiores e inyección conjuntival bilateral de una semana de evolución, que no ceden con tratamiento sintomático. Se agregan registros febriles, rash urticariforme en tronco, vómitos y diarrea, con mala tolerancia oral. Consulta en guardia, y se interna por deshidratación moderada.
Se solicita laboratorio; se observa reacción inflamatoria sistémica, PCR e inmunoglobulina (IgG e IgM) para SARS-CoV 2 negativos. En el ecocardiograma Doppler presenta derrame pericárdico de 5 mm, sin afección coronaria, con buena función ventricular. Se suma al cuadro queilitis, lengua aframbuesada, adenomegalia submaxilar izquierda, edema bipalpebral, edema en miembros superiores e inferiores sin signo de Godet. El rash se extiende a cara y abdomen, por lo que se asume como síndrome de Kawasaki like. Se administra gammaglobulina más metilprednisolona, ácido acetil salicílico (AAS) a dosis antiinflamatorias con buena respuesta. Luego de 72 h afebril desde finalizado el tratamiento, se decide el alta hospitalaria con corticoides y AAS.
A las 24 horas del alta presenta registro febril, regular estado general, acompañado de lengua aframbuesada, edema bipalpebral y conjuntivitis. Se interna. Por laboratorio se constatan parámetros de inflamación, IgG para SARS-CoV 2 positivo y al repetir ecocardiograma Doppler (Figura 1) presenta dilatación aneurismática de ambas coronarias con función ventricular conservada (Tabla 1, se detallan los valores de las coronarias con sus respectivos Z score, en los sucesivos controles ecocardiográficos). Se reasume el cuadro como SIM-C. Recibe tratamiento inmunomediado y antiagregante plaquetario con gammaglobulina (2 gr/kg/dosis), metilprednisolona (10 mg/kg/dosis, 3 pulsos), AAS 5 mg/kg/día. Presenta leve mejoría clínica y analítica. El control cardiológico a los 5 días revela similares características. Se lo clasifica como resistente al tratamiento y se indica Infliximab (5 mg/kg). Evoluciona favorablemente, con marcada mejoría clínica y cardiovascular; se otorga el alta luego de 16 días. Se programa control cardiológico y reumatológico más tratamiento antiagregante y antiinflamatorio.
Conclusión
El SIM-C se presentó como un estado inflamatorio florido en relación con una infección pasada por SARSCoV- 2. El paciente evoluciona con marcada afección coronaria sin disfunción ventricular, por lo que requirió tratamiento inmunomediado escalonado hasta tercera línea con buena respuesta durante la internación y en controles posteriores al alta.
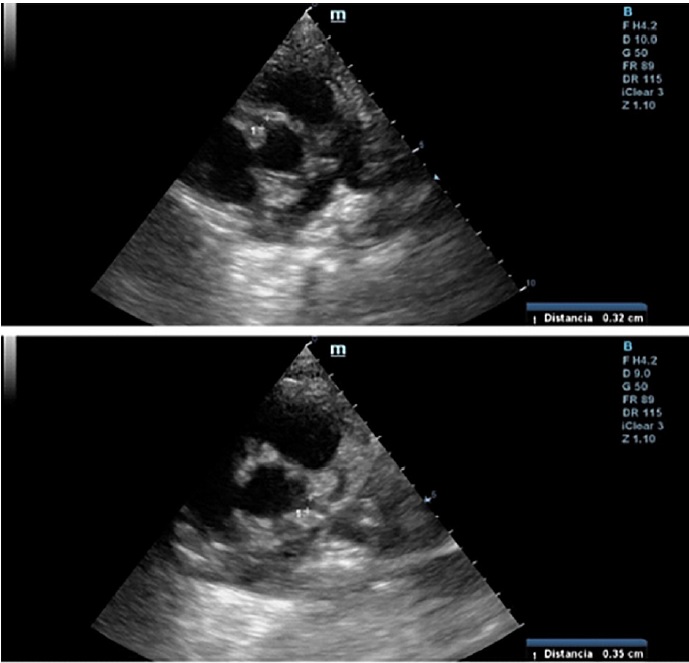
Fig. 1 Ecocardiograma Doppler 2D (eje corto de los vasos): se observa coronaria derecha en la parte superior, y coronaria izquierda en la inferior.
Tabla 1
|
Diámetro
de las coronarias (Z-Score) |
día 1 |
día 6 |
día 11 |
día 21 |
día 35 |
día 119 |
|
Coronaria derecha |
1,6
mm (+0,3) |
3,5
mm (+ 5,8) |
Proximal
2,4 mm (+2,6) Distal
3,5 mm (+7,2) |
2,2
mm (+2,7) |
2
mm (+1,5) |
1,9
mm (+1,2) |
|
Coronaria izquierda |
1,8
mm (+0,27) |
3,5
mm (+5,2) |
Proximal
3,5 mm (+5,2) Distal
3,9 mm (+8) |
2,4
mm (+1,9) |
1,8
mm (+0,27) |
2,4
mm (+2) |
Emilia Croigverg, Patricia Baselga, Susana Chicco Campos, Valeria Hasbani, Eliana Santillán
Declaración de conflicto de intereses
Los autores declaran que no tienen conflicto de intereses (Véanse formularios de conflicto de intereses de los autores en la web)
Consideraciones éticas
No aplica
BIBLIOGRAFÍA
- Sociedad Argentina de Pediatría. Consenso sobre el tratamiento del síndrome inflamatorio multisistémico asociado a COVID-19. Arch Argent Pediatr 2021;119:S198-S211. https://doi.org/10.5546/aap.2021.s198
- Taffarel P, Jorro Barón F, Rodríguez AP, Widmer J, Meregalli C. Síndrome inflamatorio multisistémico en niños, relacionado con COVID-19: actualización a propósito de la presentación de 2 pacientes críticos. Arch Argent Pediatr 2021;119: e26-e35. https://doi.org/10.5546/aap.2021.e26
- Sociedad Argentina de Pediatría y Sociedad Argentina de Cardiología. Enfermedad de Kawasaki: consenso interdisciplinario e intersociedades (guía práctica clínica). Arch Argent Pediatr. 2016.
- Asociación Española de Pediatría. Documento español de consenso sobre diagnóstico, estabilización y tratamiento del síndrome inflamatorio multisistémico pediátrico vinculado a SARS-CoV-2 (SIM-PedS). https://doi.org/10.1016/j.anpedi.2020.09.005
- Ministerio de Salud de la Nación. “Manejo inicial del síndrome inflamatorio multisistémico en niños y adolescentes relacionados temporalmente al COVID-19 (SIM-C)” Recomendaciones 31 de agosto de 2020. Disponible en: https://bancos.salud.gob.ar/sites/default/files/2020-09/covid19-manejo-inicial-del-sindrome-inflamatorio-multisistemico-en-ninios-y-adolescentes-relacionados-temporalmente-alcvod19-sim-c.pdf
- American College of Rheumatology Clinical Guidance for Multisystem Inflammatory Syndrome in Children Associated with SARSCoV- 2 and Hyperinflammation in Pediatric COVID-19: Version 3. Arthritis Rheumatol. 2022. https://doi.org/10.1002/art.42062
Rev Argent Cardiol 2023;91:374-375.
http://dx.doi.org/10.7775/rac.es.v91.i5.20673
Estenosis coronaria iatrogénica y aneurisma ventricular tras tratamiento quirúrgico como causa de miocardiopatia isquemico necrótica no aterosclerótica
El trauma torácico es responsable del 25% de las muertes por trauma. Se estima que entre el 15 y el 30% de los pacientes con traumatismo cardiotorácico penetrante requieren tratamiento quirúrgico. Dentro de las complicaciones, aunque poco frecuente, se encuentra la estenosis coronaria iatrogénica debido a sutura quirúrgica.
La estenosis coronaria iatrogénica es una complicación inusual que conlleva alta tasa de morbimortalidad. Puede observarse tras un procedimiento quirúrgico, como en la cirugía de reemplazo valvular o tras la reparación de un traumatismo cardiotorácico penetrante.
La presentación clínica dependerá de la arteria coronaria afectada, el grado de lesión, su localización y extensión, así como también de la reserva miocárdica preoperatoria. Puede evidenciarse, durante el procedimiento, infarto agudo de miocardio, arritmia ventricular o shock cardiogénico, y en estos casos, debe realizarse bypass coronario de urgencia. Sin embargo, la presentación clásica es la aparición de angina inestable, insuficiencia cardíaca congestiva, arritmias ventriculares y muerte súbita luego de varios meses del procedimiento.
Presentamos un paciente de sexo masculino de 30 años, con antecedentes de miocardiopatía dilatada isquémico-necrótica no ateroesclerótica, con fracción de eyección ventricular izquierda (FEVI) reducida (35%) y aneurisma ventricular (Figura 1) por lesión iatrogénica, extrínseca, tras la sutura de la arteria descendente anterior, luego de una herida de arma de fuego y cirugía de urgencia. Evoluciona posteriormente con varias internaciones por episodios recurrentes de taquicardia ventricular monomorfa sostenida (TVMS) (Figura 2a) por lo que se decide colocación de un dispositivo cardiodefibrilador implantable (CDI) y ablación del sustrato, con evolución favorable.
Se realiza lectura semestral del dispositivo CDI. No se han detectado nuevos eventos arrítmicos hasta el momento (dos años luego de la ablación).
La taquicardia ventricular monomorfa sostenida (TVMS) es una causa importante de muerte súbita y morbilidad en los pacientes con enfermedad coronaria. Se origina en un tejido cicatrizal; puede aparecer en la fase subaguda o incluso años después del evento isquémico. La extensión de la necrosis miocárdica y el grado de disfunción del ventrículo izquierdo son predictores del riesgo de arritmias, mayor en aquellos con FEVI reducida e isquemia extensa. (1)
La fisiopatología involucra un mecanismo de reentrada asociado a un evento isquémico, con cicatriz ya instalada o en desarrollo en más del 95% de los casos.
La fibrosis con haces de miocardio vivo entrelazados, crea el sustrato para un bloqueo de conducción fijo o funcional, con una conducción interrumpida y lenta que lleva al mecanismo desencadenante de la arritmia.
Los aneurismas ventriculares se observan en el ventrículo izquierdo en un 95% de los casos. Se definen por la presencia de cicatriz que genera deformidad de la cavidad, con una dilatación no contráctil y circunscripta del ventrículo. Puede asociarse a insuficiencia cardíaca congestiva grave, con gasto cardíaco bajo e incluso shock cardiogénico, embolismos sistémicos y taquicardia ventricular recidivante o combinación de los anteriores.
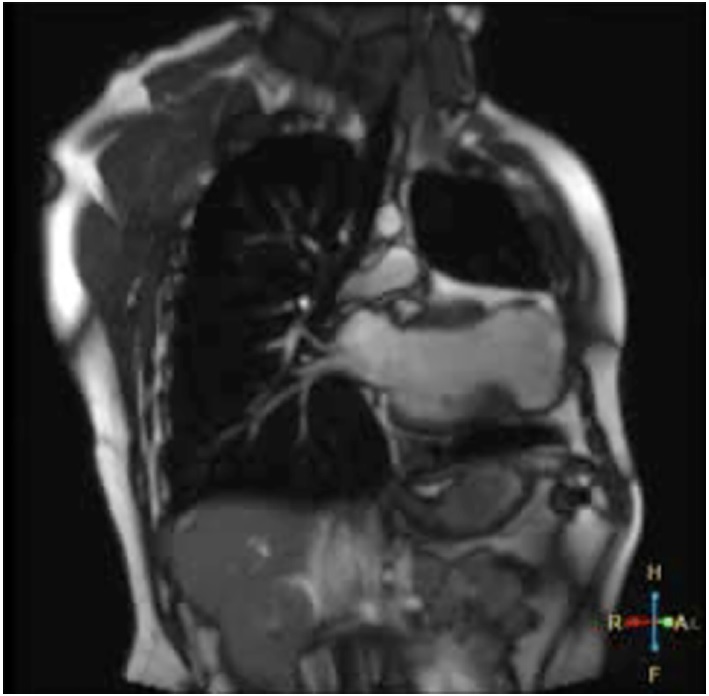
Fig. 1 Corte coronal de resonancia magnética en secuencia T2 donde se evidencia dilatación ventricular izquierda, la presencia de saco aneurismático apical, adelgazamiento miocárdico y señal de baja intensidad.
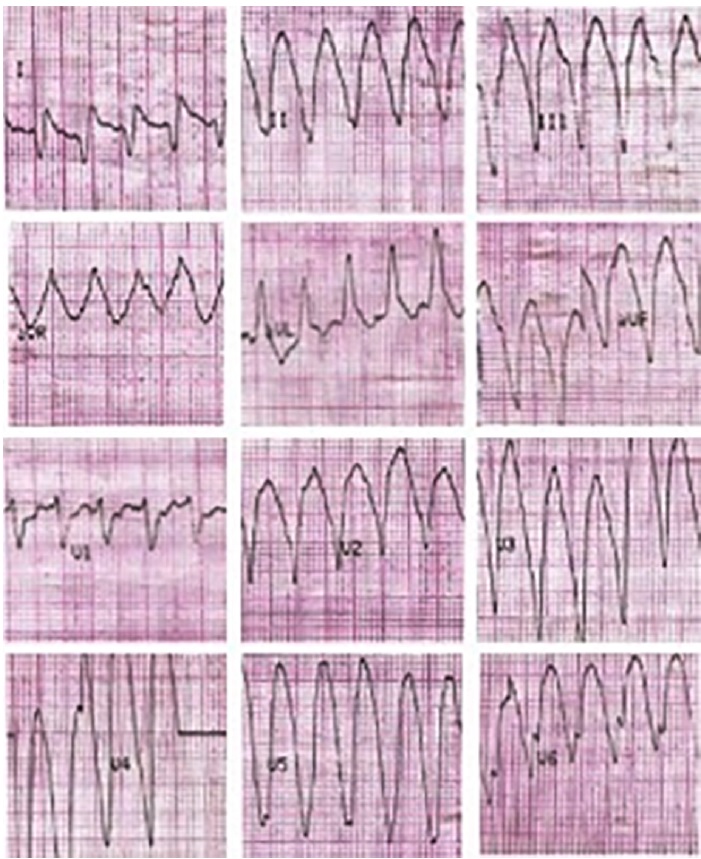
Fig. 2a Taquicardia ventricular monomorfa con complejo QRS ancho, regular, monomorfa a 190 lpm, con origen apical compatible con el aneurisma ventricular
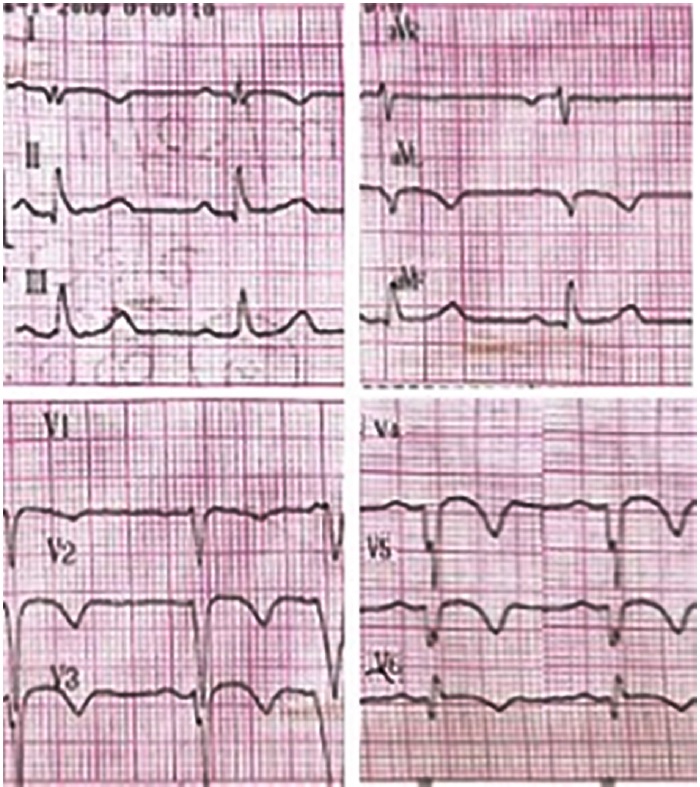
Fig. 2b Electrocardiograma posterior a la cardioversión eléctrica donde se observa ritmo sinusal a 65 lpm, con presencia de ondas Q y T negativas en cara anterolateral, compatible con secuela de necrosis y trastornos en la repolarización
La primera opción terapéutica ante la detección de un aneurisma ventricular iatrogénico es la revascularización que puede lograrse mediante angioplastia transluminal coronaria (ATC) o by pass aorto-coronario, dependiente del momento en que se detecta el daño. Si se detecta durante la cirugía y/o el vaso se encuentra totalmente obstruido por una sutura, se opta por el by pass; en cambio si la detección es luego del cierre de la esternotomía, la ATC es la mejor opción para restaurar el flujo y evitar una nueva esternotomía. En ocasiones puede optarse por un procedimiento híbrido. Es importante destacar igualmente que los resultados a largo plazo de cualquiera de estas intervenciones son desconocidos. (2)En la actualidad contamos con distintas alternativas terapéuticas para la prevención secundaria de la TV.
Actualmente el CDI se ha convertido en el tratamiento de elección en sujetos con arritmia ventricular asociada a enfermedad coronaria; es una recomendación IA en pacientes con FEVI ≤35% en CF II-III de la NYHA, o en CF I con FEVI ≤30%, en prevención primaria, y en sobrevivientes a un paro cardíaco por TV o fibrilación ventricular (FV) no atribuibles a casusas reversibles o transitorias en prevención secundaria. Estudios reportados basados en el uso de este dispositivo en prevención secundaria, evidencian una reducción significativa en la tasa de mortalidad, la cual se debe a la reducción de la muerte súbita cardiaca, y no a la disminución del número de eventos arrítmicos. (3)
Complementariamente se recomienda en estos casos, realizar terapia combinada con tratamiento farmacológico y/o ablación, siendo esta última de elección para aquellos con TVMS, debido a la menor tasa de recurrencia. (4)
El abordaje utilizado para la ablación de la taquicardia ventricular depende de varios factores, como la inducibilidad, la sostenibilidad y la tolerancia clínica a la TV. A su vez, la combinación de imágenes anatómicas de la cicatriz miocárdica mediante tomografía computada (TC) y resonancia magnética nuclear (RMN), entre otros, contribuyen a detectar el sitio arritmogénico. (5)
En los casos de TV no inducible o mal tolerada por inestabilidad hemodinámica o disfunción sistodiastólica ventricular, la ablación del sustrato puede realizarse mediante el uso de sistemas de navegación 3D. Con esta técnica, la energía de radiofrecuencia se administra en regiones con tejido cicatrizal que se correlacionan topográficamente con la región de origen del circuito de reentrada de la taquicardia, según sugiere el electrograma intracavitario, donde se registran potenciales anormales. Las áreas de voltaje extremadamente bajo se designan como cicatriz densa. Las lesiones por radiofrecuencia pueden generarse entonces en paralelo a la zona del borde de la cicatriz (donde la amplitud del electrograma bipolar, por técnica de marcapasos, suele estar entre 0,5 mV y 1,0 mV).
Cuando se puede inducir una TV semejante a la que presentó el paciente, la ablación se realiza en la zona en la que la arritmia fue generada, y una vez efectuada, se corrobora el éxito si no se logra inducir nuevamente. Si en cambio, no se logra reproducir, como ocurrió en este caso, la ablación se hace mediada por el sustrato anatómico y no es posible evaluar su efectividad. (6)
En general, la ablación es eficaz de forma aguda, y produce la abolición de una o más TVMS relacionadas con la cicatriz en hasta el 77-95% de los casos. Sin embargo, la recurrencia de la TV con la misma morfología, o más a menudo con una morfología diferente, puede ocurrir en el 12-50% de los pacientes, y puede ser necesaria la reintervención. En consecuencia, la ablación exitosa de la TV no elimina la necesidad de un tratamiento con CDI o antiarrítmicos orales.
Debido a la alta tasa de morbimortalidad y recurrencia de la TVMS en pacientes con cardiopatía isquémica, se debe optar por un tratamiento efectivo, en la mayoría de los casos terapia combinada. Es de elección el implante de un dispositivo CDI para disminuir la incidencia de muerte súbita y el uso de ablación de sustrato y/o antiarrítmicos orales para evitar la recurrencia.
Ana Inés María Vinuesa, Giuliana Tresenza, Guillermo LiniadoMTSAC
BIBLIOGRAFÍA
- Guandalini GS, Liang JJ, Marchlinski FE. Ventricular Tachycardia Ablation: Past, Present, and Future Perspectives. JACC Clin Electrophysiol. 2019;5:1363-83. https://doi.org/10.1016/j.jacep.2019.09.015
- Comanici M, Raja SG. Iatrogenic Coronary Artery Injuries during Non-cardiac Artery Adult Cardiac Surgery. AME Med J 2023;8-12
- Al-Khatib SM, Stevenson WG, Ackerman MJ, Bryant WJ, Callans DJ, Curtis AB, et al. 2017 AHA/ACC/HRS Guideline for Management of Patients With Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death: A Report of the American College of Cardiology/ American Heart Association Task Force on Clinical Practice Guidelines and the Heart Rhythm Society. J Am Coll Cardiol. 2018;72:e91- e220. https://doi.org/10.1016/j.jacc.2017.10.054
- Liu G, Xu X, Yi Q, Lv T. The efficacy of catheter ablation versus ICD for prevention of ventricular tachycardia in patients with ischemic heart disease: a systematic review and meta-analysis. J Interv Card Electrophysiol. 2021;61:435-43. https://doi.org/10.1007/s10840-020-00848-1
- Cuculich PS, Schill MR, Kashani R, Mutic S, Lang A, Cooper D, et al. Noninvasive Cardiac Radiation for Ablation of Ventricular Tachycardia. N Engl J Med. 2017;377:2325-36. https://doi.org/10.1056/NEJMoa1613773.
- Berruezo A, Fernández-Armenta J, Andreu D, Penela D, Herczku C, Evertz R, et al. Scar dechanneling: new method for scar-related left ventricular tachycardia substrate ablation. Circ Arrhythm Electrophysiol. 2015;8:326-36. https://doi.org/10.1161/CIRCEP.114.002386 a 65 lpm, con presencia de ondas Q y T negativas en cara anterolateral, compatible con secuela de necrosis y trastornos en la repolarización.
Rev Argent Cardiol 2023;91:375-378.
http://dx.doi.org/10.7775/rac.es.v91.i5.20674
Trombosis venosa profunda por variante inusual de síndrome de May-Thurner. Resolución mediante trombectomía mecánica percutánea sin uso de trombolíticos
El síndrome de May-Thurner (SMT) es una entidad que consiste en la compresión de la vena ilíaca común izquierda entre la columna vertebral y la arteria ilíaca común derecha. Se puede presentar como lesiones de vena ilíaca no trombóticas (LVINT), trombosis venosa profunda (TVP) o síndrome postrombótico (SPT), y típicamente afecta a mujeres jóvenes. Si bien se considera una entidad muy poco frecuente, se sabe que su incidencia está muy probablemente subestimada. (1)
Aunque más raro, las compresiones a otros niveles también han sido descriptas, como la de la vena ilíaca común derecha o una compresión izquierda por la arteria hipogástrica homolateral. (2,3)
Presentamos el caso de una mujer que se presentó con una TVP del miembro inferior izquierdo causada por una variante rara de SMT.
Mujer de 55 años, previamente sana, que consulta por cuadro de edema marcado de todo el miembro inferior izquierdo, con dolor incapacitante, coloración azulada-violácea del miembro y parestesias en el pie, que comenzó una semana previa a la consulta y que fue empeorando al punto de inhabilitar la marcha. Al examen físico era notable el edema desde el pie hasta la raíz del muslo, tenso, así como la ausencia de pulsos distales con solo señales monofásicas por Doppler sin alteración de la función motora. El eco Doppler reveló una TVP que involucraba las venas femoral común, femoral proximal y femoral profunda, y también la vena safena magna, por lo que se decidió iniciar de inmediato anticoagulación con heparina de bajo peso molecular. La angiotomografía mostró una extensa TVP desde la vena ilíaca externa izquierda proximal hasta la vena poplítea, al igual que una bifurcación aórtica retrocava, con compresión a nivel de la confluencia de las venas ilíacas externa e interna, entre el sacro y la arteria hipogástrica izquierda (Figura 1).
Se decidió llevar a la paciente a Hemodinamia para colocación de un filtro de vena cava inferior (VCI) por vía femoral derecha. Luego, con la paciente en decúbito ventral, se realizó una punción guiada por ecografía de la vena poplítea con colocación de un introductor 11 French por medio del cual se llevó a cabo una trombectomía mecánica de toda la oclusión con dispositivo Aspirex®S. Un claro sitio de compresión se notó al mismo nivel observado en la angiotomografía, que ocasionaba incluso una ruptura parcial de la vena con fuga de contraste sin descompensación hemodinámica. Se decidió colocar un stent venoso autoexpandible de 12 × 120 mm, y dilatación con balón, con un resultado final muy satisfactorio (Figura 2).
El edema resolvió a las pocas horas, con recuperación de los pulsos distales y franca resolución de los síntomas. La paciente fue externada luego de una angiotomografía que evidenció permeabilidad del stent y ausencia de complicaciones agudas, con anticoagulación oral y compresión 30-40 mmHg, programada para posterior extracción del filtro de VCI.
La compresión de la vena ilíaca común o externa por la arteria hipogástrica homolateral es rara; existen pocos casos descriptos en la literatura. Llamativamente, nuestra paciente presentaba ausencia de pulsos distales palpables con flujo arterial alterado por Doppler, lo cual no es lo más habitual en casos de TVP iliofemoral. Sin embargo, este cuadro también está descripto en los reportes de casos de esta misma variante. (2,3)
Creemos que esto puede estar explicado claramente por el intenso edema producto de una compresión exactamente a nivel de la confluencia entre las venas ilíacas externa e interna, lo cual comprometería aún más el drenaje venoso del miembro inferior.
La incidencia de SPT a 2 años llega hasta 75% en pacientes con TVP extensas, por lo que remover el trombo en forma precoz está demostrado y recomendado en la actualidad no solo para aliviar los síntomas en la fase aguda, sino también para prevenir el desarrollo de esta complicación, especialmente teniendo en cuenta que muchas veces se trata de pacientes jóvenes, y que el cuadro puede llegar a ser discapacitante y afectar seriamente la calidad de vida. (4)
De los estudios al respecto, CaVenT es quizás el que posea mayor peso debido a su período de seguimiento, si bien apunta al uso de líticos como estrategia para remover el trombo. Este mismo estudio arrojó tasas de permeabilidad muy bajas a mediano y largo plazo sin uso de stent (65,9%), por lo que hoy las recomendaciones hablan de intervenir los pacientes con TVP iliofemoral para remover el trombo por distintos mecanismos, y aconsejan el uso de stents para lidiar con los sitios de compresión o estenosis residual. (4,5)
El dispositivo Aspirex®S permite realizar una trombectomía mecánica en forma segura, y evitar el uso de trombolíticos y el consiguiente riesgo de hemorragia. Aún no hay estudios randomizados al respecto, pero los resultados provenientes de estudios observacionales son muy prometedores. (6)
Si bien no existe evidencia fuerte para el uso profiláctico de filtros de VCI, preferimos hacerlo dado que no solo se previene una complicación potencialmente mortal como la embolia pulmonar, sino también las consecuencias a largo plazo de embolias pulmonares subclínicas en pacientes jóvenes, como la hipertensión pulmonar.
En conclusión, describimos el caso de una mujer que se presentó con una TVP iliofemoral como consecuencia de una variante rara del SMT, con clínica incapacitante. El mismo fue resuelto en forma exitosa por vía endovascular, siguiendo las recomendaciones de las guías internacionales para el tratamiento de las TVP iliofemorales y sin el uso de trombolíticos. El trabajo multidisciplinario que involucre profesionales de hemodinamia, cirugía vascular y hematología es elemental para el reconocimiento de esta patología y poder hacer así un tratamiento precoz y adecuado, como también para el control y seguimiento de estos pacientes.
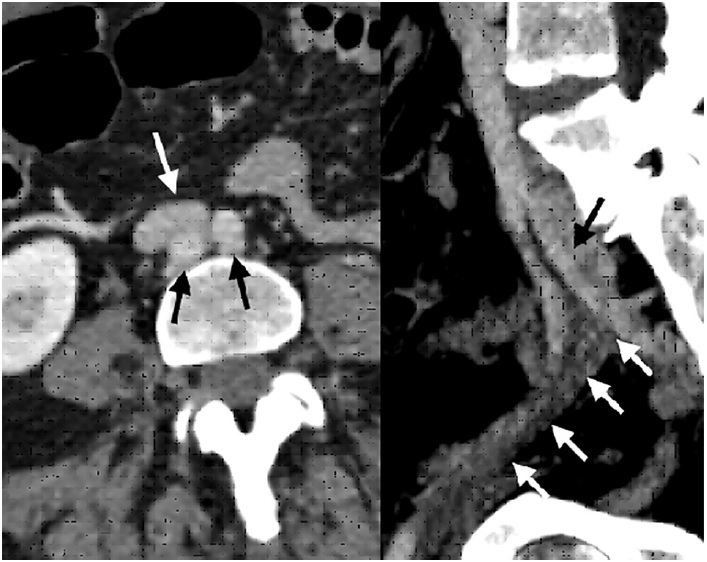
Fig. 1 Izquierda. Corte axial de angiotomografía que evidencia bifurcación aórtica (flechas negras), por detrás de la confluencia iliocava (flecha blanca). Derecha. Corte sagital que objetiva compresión por la arteria hipogástrica izquierda (flecha negra) que causa trombosis de la vena ilíaca externa (flechas blancas).
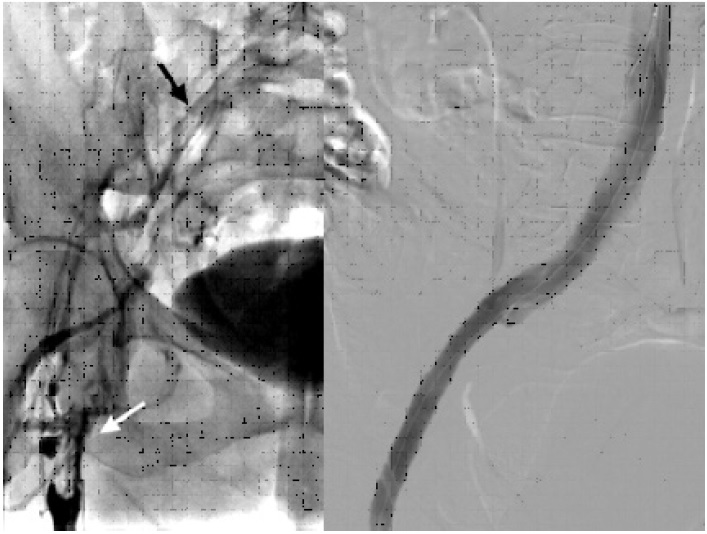
Fig. 2 Izquierda. Flebografía inicial que muestra trombosis la desde vena femoral proximal (flecha blanca), que recanaliza con hipoflujo a nivel de vena ilíaca común (flecha negra). Derecha. Flebografía final post colocación de stent mostrando permeabilidad absoluta del eje ilíaco.
Miguel Ferrer, Sebastián Romero, Fernando Álvarez, Ricardo Parra, Horacio Romero
Servicios de Cirugía Vascular y Hemodinamia.
Hospital Privado Regional del Sur. San Carlos de Bariloche, Argentina
Declaración de conflicto de intereses
Los autores declaran que no tienen conflicto de intereses (Véanse formularios de conflicto de intereses de los autores en la web)
BIBLIOGRAFÍA
- Mako K, Puskas A. May-Thurner syndrome - Are we aware enough? Vasa 2019;48:381-8. https://doi.org/10.1024/0301-1526/a000775
- Steinberg JB, Jacocks MA. May-Thurner Syndrome: a previously unreported variant. Ann Vasc Surg 1993;7:577-81. https://doi.org/10.1007/BF02000154
- Sharafi S, Farsad K. Variant May-Thurner syndrome: Compression of the left common iliac vein by the ipsilateral internal iliac artery. Radio Case Rep 2018;13:419-423. https://doi.org/10.1016/j.radcr.2018.01.001
- Kakkos SK, Gohel M, Baekgaard N, Bauersachs R, Bellmunt- Montoya S, Black SA, et al., European Society for Vascular Surgery (ESVS) 2021 Clinical Practice Guidelines on the Management of Venous Thrombosis. European Journal of Vascular and Endovascular Surgery. https://doi.org/10.1016/j.ejvs.2020.09.023
- Haig Y, Enden T, Sandset PM, CaVenT Study Group. Postthrombotic syndrome after catheter-directed thrombolysis for deep vein thrombosis (CaVenT): 5-year follow-up results of an open-label, randomized controlled trial. Lancet Haematol 2016,3:e64-71. https://doi.org/10.1016/S2352-3026(15)00248-3
- Loffroy R, Falvo N, Chevallier O. Single-Session Percutaneous Mechanical Thrombectomy Using the Aspirex ®S Device Plus Stenting for Acute Iliofemoral Deep Vein Thrombosis: Safety, Efficacy, and Mid-Term Outcomes. Diagnostics (Basel) 2020;10:544. https://doi.org/10.3390/diagnostics10080544
Rev Argent Cardiol 2023;91:378-379.
http://dx.doi.org/10.7775/rac.es.v91.i4.20671
https://creativecommons.org/licenses/by-nc-sa/4.0/
