José M. Bonorino1 MTSAC, Jorge A. Bilbao1 MTSAC, Nicolás A. Torres1, Mateo Iwanowski1, Emilia M. Spaini1, Agustina F. Gallegos1, Renzo Melchiori1, María E. Aris Cancela2, Horacio E. Fernández1 MTSAC, Sergio Baratta1 MTSAC
1 Instituto de Cardiología, Hospital Universitario Austral
2 Servicio de Hematología, hemostasia y trombosis, Hospital Universitario Austral
Dirección para correspondencia: José M. Bonorino. Av. Presidente Perón 1500, Pilar, Buenos Aires, Argentina. Código Postal: B1629ODT. Correo electrónico: jbonorin@cas.austral.edu.ar
Rev Argent Cardiol 2024;92:103-109. http://dx.doi.org/10.7775/rac.es.v92.i2.20744 Ver artículo relacionado: Rev Argent Cardiol 2024;92:101-102. http://dx.doi.org/10.7775/rac.es.v92.i2.20755
RESUMEN
Introducción: El Índice de Severidad del Embolismo Pulmonar (PESI) se utiliza para categorizar el riesgo de mortalidad en el tromboembolismo pulmonar agudo (TEP). Por definición, los pacientes con cáncer siempre presentarán un puntaje PESI simplificado alto y serán considerados de mayor riesgo. Existe información limitada respecto de si los pacientes con PESI intermedio o alto (≥86 puntos) y cáncer activo, tienen mayor riesgo de presentar una evolución desfavorable respecto de aquellos sin cáncer.
Objetivos: Determinar si, en pacientes con TEP y un puntaje PESI ≥86 puntos, la presencia de cáncer activo se asocia a una evolución desfavorable respecto de aquellos sin cáncer.
Material y métodos: Análisis retrospectivo en pacientes con TEP y un puntaje PESI ≥86, entre los años 2008 y 2022. Se evaluó la ocurrencia de muerte intrahospitalaria (MIH), uso de drogas vasopresoras (DV) y necesidad de asistencia respiratoria mecánica (ARM) en los pacientes con vs. sin cáncer.
Resultados: Se analizaron 209 pacientes. La población con cáncer, respecto de aquella sin cáncer, resultó ser más joven (65 vs. 70 años; p=0,006), presentó valores de PESI simplificado altos con mayor frecuencia (100 % vs. 84 %; p<0,001), tuvo menor requerimiento de ARM (9 % vs. 34 %; p=0,005) y menor uso de DV (11 % vs. 23 %; p=0,019), aunque no se observaron diferencias en las tasas de MIH (12,7 % vs. 8 %; p=NS).
Conclusiones: Los pacientes con TEP y un puntaje PESI ≥86 con cáncer no presentaron mayor MIH e incluso tuvieron menor requerimiento de ARM y DV. En la población estudiada, los pacientes con TEP y cáncer no tuvieron mayor riesgo de presentar una evolución desfavorable.
Palabras clave: Embolia pulmonar - Cáncer - Mortalidad hospitalaria - Puntuaciones de riesgo - PESI - Pulmonary Embolism Severity Index - PESI simplificado
ABSTRACT
Background: The Pulmonary Embolism Severity Index (PESI) is used to categorize the risk of death in acute pulmonary embolism (PE). By definition, cancer patients will always have a high simplified PESI score and will be considered at high risk. There is limited information regarding whether patients with an intermediate or high PESI score (≥86 points) and cancer are at greater risk of an unfavorable progression versus those without cancer.
Objectives: To determine whether the presence of active cancer in patients with a PESI score ≥86 points is associated with an unfavorable progression versus those without cancer.
Methods: A retrospective analysis in patients with PE and a PESI score ≥86, between 2008 and 2022. The occurrence of in-hospital mortality (IHM) the use of vasopressor drugs (VDs), and the need for mechanical ventilatory support (MVS) were evaluated in patients with vs. without cancer.
Results: 209 patients were analyzed. The population with cancer was younger than patients without cancer (65 vs 70 years; p=0.006), showed high simplified PESI values more frequently (100% vs 84%; p<0.001), had lower MVS requirement (9% vs 34%; p=0.005), and used fewer VDs (11% vs 23%; p=0.019). However, no difference was observed in IHM rates (12.7% vs 8%; p=NS).
Conclusions: Patients with PE and a PESI score ≥86 who have cancer did not show higher IHM and also had lower MVS and VDs requirement. Therefore, in the studied population, patients with PE and cancer had no greater risk of having an unfavorable progression.
Key words: Images - Cardiovascular prevention - Artificial intelligence - Machine learning.
Recibido: 30/09/2023
Aceptado: 05/03/2024
INTRODUCCIÓN
El tromboembolismo agudo de pulmón (TEP) es la segunda causa de muerte en los pacientes oncológicos, luego de las ocasionadas por el propio cáncer, (1) y se estima que hasta un 20 % de los pacientes con cáncer presentará un TEP. (23)
La Argentina tiene una incidencia intermedia a alta de cáncer, que, junto con las enfermedades cardiovasculares, concentran más del 40 % de las defunciones según los últimos registros epidemiológicos. (4)
La presencia de TEP asociado al cáncer (TEP-CA) tiene en varios registros mayor mortalidad, independientemente de las características del cáncer (5-7) y de los síntomas asociados. (8,9)
El Índice de Severidad del Embolismo Pulmonar (PESI) es un modelo pronóstico útil para estimar la mortalidad intrahospitalaria y a 30 días. Las complicaciones o eventos fatales de los pacientes de bajo o muy bajo riesgo (<86 puntos) es menor de 1,9 % y 1,1 % respectivamente. (10)
Con la versión simplificada del PESI (PESIs) se verificó que en aquellos individuos con un puntaje de PESIs <1, la mortalidad a 30 días fue 1,1 % (riesgo bajo) mientras que con un puntaje ≥1 fue 8,9 % (riesgo alto). (11) Ambos puntajes han sido validados en la Argentina con buena correlación con la mortalidad. (12)
Las guías actuales recomiendan la utilización indistinta de cualquiera de los puntajes (PESI o PESIs) para estratificar el riesgo. (13-15) Aquellos con puntajes de PESI o PESIs bajos, son candidatos para recibir únicamente anticoagulación, y un eventual egreso hospitalario temprano. (16)
Los pacientes con TEP-CA presentarán indefectiblemente un valor de PESIs alto, ya que el antecedente oncológico es considerado una variable de riesgo en su definición original y por lo tanto serán considerados de mayor riesgo al utilizar esta clasificación.
Existe información limitada, respecto de si los pacientes con TEP-CA y un PESI intermedio o alto (≥86 puntos) tienen mayor riesgo de presentar una evolución desfavorable respecto de aquellos sin cáncer. También se desconoce si aquellos pacientes con TEP-CA, podrían tener un mejor pronóstico con un PESI <86 puntos.
MATERIAL Y MÉTODOS
Análisis retrospectivo de una cohorte prospectiva unicéntrica, efectuado en un Hospital Universitario Argentino, sobre pacientes hospitalizados por TEP entre los años 2008-2022 que tuvieran un puntaje PESI ≥86 puntos. El objetivo de este estudio es determinar si en pacientes con TEP y puntaje PESI ≥86 puntos la presencia de cáncer activo se asocia a una evolución desfavorable respecto de aquellos sin cáncer.
Se evaluó la incidencia de mortalidad intrahospitalaria (MIH), uso de drogas vasopresoras (DV) y necesidad de asistencia respiratoria mecánica (ARM) en pacientes con y sin TEP-CA. Asimismo, se evaluó la MIH y la incidencia de sangrado BARC (17) en pacientes con TEP-CA y puntaje PESI <86 puntos.
Se definió cáncer activo a la presencia de neoplasia maligna sólida o hematológica que hubiera recibido en el último año tratamiento quimioterápico y/o radiante, o sin tratamiento activo, pero con cuidados paliativos. Se incluyeron los pacientes con cáncer avanzado, al igual que las neoplasias cerebrales, tuvieran o no contraindicación para recibir anticoagulación o terapia de reperfusión. No se consideró cáncer activo a las neoplasias de piel, excepto al melanoma. Se definió dilatación del ventrículo derecho (VD) a una relación entre el diámetro del VD/ diámetro del ventrículo izquierdo >0,9 en la vista de cuatro cámaras; y se consideró como falla del VD, a la dilatación del VD junto con al menos uno de los siguientes: hipoquinesia de la pared libre, excursión sistólica del plano del anillo tricuspídeo (TAPSE) menor que 16mm, y/o abombamiento del septum interventricular.
Condiciones éticas
Los datos fueron tomados de la historia clínica y se almacenaron en una base de datos encriptada y autorizada por el Comité de Ética e Investigación Institucional. Se obtuvieron todos los consentimientos informados para el uso anónimo de datos y el protocolo fue aprobado por nuestro Comité de Bioética Institucional, con número de resolución 19-041.
Análisis estadístico
Para la descripción de las variables cuantitativas se utilizaron la media y la desviación estándar o la mediana y el rango intercuartílico (RIC) 25-75 según que la distribución fuera normal o no. Las variables cualitativas se presentaron como tablas de frecuencia y porcentajes. Para la comparación de variables cuantitativas se utilizaron el test de t o el test de Wilcoxon para muestras independientes o pareadas según el caso. Para la comparación de variables dicotómicas se usaron la prueba de χ2 o la de McNemar. Se realizó un análisis multivariado de regresión logística para evaluar la estabilidad de los resultados sobre MIH, ARM y uso de DV, con ajuste por edad, sexo, hipertensión arterial (HTA), diabetes y cáncer activo. Se consideró significativo un valor de p a 2 colas <0,05. El análisis se realizó con Stata/ SE v13.0 (StataCorp, Estados Unidos).
RESULTADOS
Sobre 456 pacientes internados con diagnóstico de TEP incluidos en nuestro registro, se analizaron 209 que presentaron un puntaje PESI ≥86. De esta población, 126 (60,3 %) presentaban cáncer activo y 83 (39,7 %) no tenían cáncer (Figura 1). Respecto de la población con cáncer, el 23 % correspondió a TEP incidentales y el 12,6 % presentaba limitación del esfuerzo terapéutico. Se registró una prevalencia elevada de tumores sólidos: cáncer de pulmón (17,4 %), gastrointestinal (17,4 %), mama (11,1 %), biliopancreático (10,3 %), ginecológico (9,5 %), renovesical (8,7 %), prostático (7,1 %), sistema nervioso central (4,7 %) y otros tumores malignos (6,3 %); y una menor prevalencia de neoplasias malignas oncohematológicas (7,1 %). (Figura 2). Las características basales, marcadores pronósticos y terapia de reperfusión indicada en cada población con y sin cáncer se muestran en la Tabla 1. La población con TEP-CA resultó más joven que aquella sin cáncer (65 vs. 70 años; p=0,006). Los pacientes con TEP-CA presentaron una menor prevalencia de HTA (48% vs 72%, p<0,001), pero más diabetes (19% vs. 8%, p=0,045), respectivamente. Por definición, la totalidad de los pacientes con TEP-CA tuvieron un puntaje PESIs alto y su prevalencia resultó mayor respecto de los pacientes sin cáncer (100 % vs. 84 %; p<0,001). Existió una tasa de utilización de anticoagulación elevada tanto en pacientes con TEP-CA como en la población sin cáncer (97,6 % vs. 97,5 %; p=NS). La población con TEP-CA respecto de aquella sin cáncer presentó menor dilatación del VD (16,6 % vs. 50,1 %; p<0,001) y menor disfunción del VD (13,4 % vs. 37,3 %; p<0,001).
En la población de pacientes con TEP-CA se indicó con menor frecuencia algún tipo de terapia de reperfusión (9,3 % vs 33,6 %; p<0,001), con una menor indicación de fibrinolíticos (Tabla 1). No se observaron diferencias en las tasas de sangrado mayor (BARC ≥3) entre los pacientes con TEP-CA vs. sin cáncer (2,3 % vs. 4,8 %; p=NS); no existieron sangrados fatales (BARC tipo 5) y se registró un sangrado quirúrgico (BARC tipo 4) en cada grupo.
Los pacientes con TEP-CA no mostraron diferencias en las tasas de MIH respecto de los pacientes sin cáncer (12,7 % vs. 8,4 %; p = NS), aunque tuvieron menor requerimiento de ARM (9,5 % vs. 24 %; p = 0,005) y uso de DV (11 % vs. 23 %; p = 0,019) (Tabla 2). La ausencia de cáncer activo correlacionó con mayor riesgo de ARM, pero no de mayor mortalidad hospitalaria, en análisis multivariado ajustado por edad, género, HTA y diabetes (Tabla 3). El modelo estadístico tuvo una buena calibración gráfica y estadística con área bajo la curva ROC de 0,70 (IC95% 0,65-0,73) y una prueba de Hosmer-Lemeshow con un valor de p = 0,521.
Ninguno de los pacientes con puntaje PESI <86 puntos, con cáncer (n = 24) o sin cáncer (n=151) falleció durante la internación. En pacientes con cáncer, un puntaje PESI <86 vs. ≥86 puntos no demostró utilidad para predecir MIH (0 % vs. 12 %; p = NS). Ningún paciente con TEP-CA y PESI<86 presentó sangrado ni tuvo disfunción ventricular derecha, y solo 8,3 % tuvieron dilatación leve del VD.
Fig. 1. Diagrama de flujo. Pacientes internados con tromboembolismo pulmonar agudo con un puntaje PESI ≥86 puntos, con cáncer activo vs. sin cáncer activo
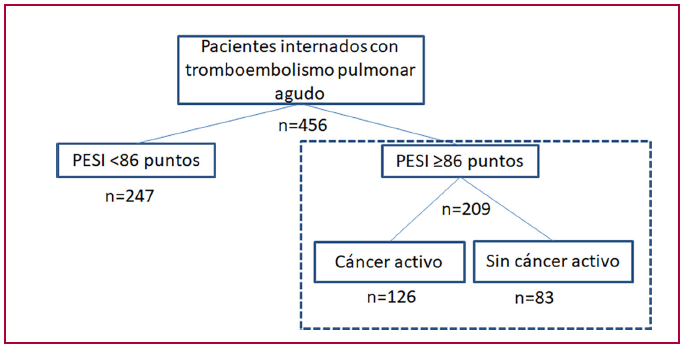
Fig. 2. Pacientes con tromboembolismo pulmonar agudo y cáncer activo (n=126). Tipos de neoplasia maligna
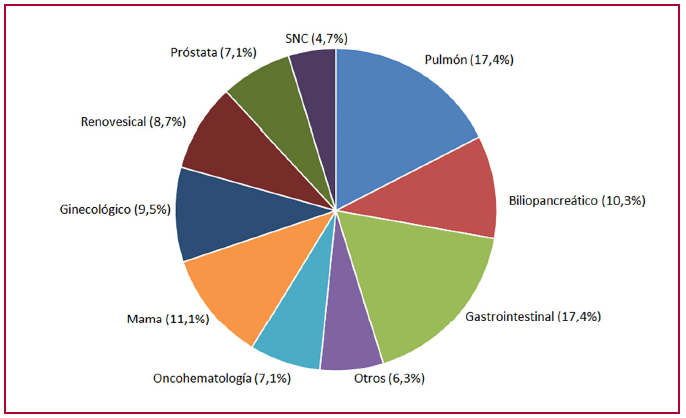
SNC = sistema nervioso central.
Tabla 1. Características clínicas, marcadores pronósticos y terapia de reperfusión indicada en pacientes con tromboembolismo pulmonar (TEP) y PESI ≥86
|
Características clínicas, marcadores pronósticos y terapia de reperfusión indicada |
Con Cáncer n = 126 (60,3%) |
Sin Cáncer n = 83 (39,7%) |
Valor de p |
|
Edad (años, media ) |
65 |
70 |
0,006 |
|
Sexo femenino |
62
(49%) |
38 (45%) |
0,672 |
|
Hipertensión Arterial |
61
(48%) |
60 (72%) |
<0,001 |
|
Diabetes |
24 (19%) |
7
(8%) |
0,045 |
|
EPOC |
6 (5%) |
7
(8%) |
0,381 |
|
Tabaquismo |
54
(43%) |
31 (37%) |
0,473 |
|
Dislipidemia |
46
(36%) |
27
(32%) |
0,656 |
|
Recibió tratamiento anticoagulante |
123
(97,6%) |
81
(97,5%) |
1 |
|
Puntaje PESI |
|||
|
PESI ³86 puntos |
126
(100%) |
83 (100%) |
1 |
|
PESIs ³1 punto |
126
(100%) |
70
(84%) |
<0,001 |
|
Compromiso ventricular derecho |
|||
|
Dilatación ventricular derecha |
21
(16,6%) |
42 (50,1%) |
<0,001 |
|
Falla ventricular derecha |
17
(13,4%) |
31 (37,3%) |
<0,001 |
|
Biomarcadores de injuria miocárdica |
|||
|
Troponina T >14 pg./ml |
63
(50%) |
53
(63%) |
0,064 |
|
Estrategia de reperfusión en la internación |
|||
|
Solo anticoagulación |
114
(90,4%) |
56 (67,4%) |
<0,001 |
|
Terapia de reperfusión
guiada por catéter |
8
(6,3%) |
11 (13,2%) |
0,138 |
|
Trombectomía quirúrgica |
1
(0,7%) |
3 (3,6%) |
0,303 |
|
Fibrinolíticos |
3
(2,3%) |
14 (16,8%) |
<0,001 |
EPOC: enfermedad pulmonar obstructiva crónica; PESIs: Índice de Severidad en el TEP Simplificado. Falla ventricular derecha (VD): dilatación VD junto con al menos uno de los siguientes: hipoquinesia de la pared libre, TAPSE menor de 16 mm, abombamiento del septum interventricular.
Tabla 2. Incidencia de eventos adversos hospitalarios en pacientes con puntaje PESI ≥≥86, con vs. sin cáncer
|
Eventos Adversos Hospitalarios |
Con Cáncer n = 126 (60,3%) |
Sin Cáncer n = 83 (39,7%) |
Valor de p |
|
Asistencia Respiratoria Mecánica |
12 (9,5%) |
20 (24%) |
0,005 |
|
Uso de Vasopresores |
14 (11%) |
19 (23%) |
0,019 |
|
Mortalidad Intrahospitalaria |
16 (12,7%) |
7
(8%) |
0,232 |
Tabla 3. Análisis multivariado para la predicción de eventos adversos hospitalarios.
|
Eventos Adversos Hospitalarios |
Odds Ratio (IC95%) |
Error estándar |
Valor de p |
|
Asistencia Respiratoria Mecánica |
|||
|
Edad (años) |
0,99 (0,96-1,02) |
0,01 |
0,759 |
|
Hipertensión Arterial |
0,99 (0,38-2,53) |
0,47 |
0,986 |
|
Diabetes |
1,34 (0,43-4,18) |
0,77 |
0,605 |
|
Sexo masculino |
1,98 (0,88-4,49) |
0,82 |
0,098 |
|
Cáncer Activo |
0,30 (0,14-0,65) |
0,11 |
0,002 |
|
Uso de drogas
vasopresoras |
|||
|
Edad (años) |
0,99 (0,96-1,02) |
0,01 |
0,721 |
|
Sexo masculino |
1,11 (0,51-2,37) |
0,43 |
0,786 |
|
Diabetes |
2,13 (0,79-5,74) |
1,07 |
0,132 |
|
Cáncer Activo |
0,39 (0,19-0,80) |
0,14 |
0,010 |
|
Muerte Intrahospitalaria |
|||
|
Edad (años) |
1,01 (0,97-1,05) |
0,01 |
0,405 |
|
Hipertensión Arterial |
0,35 (0,13-0,95) |
0,17 |
0,040 |
|
Diabetes |
1,99 (0,63-6,30) |
1,17 |
0,237 |
|
Sexo masculino |
1,46 (0,60-3,54) |
0,65 |
0,402 |
|
Cáncer Activo |
0,90 (0,42-1,93) |
0,35 |
0,800 |
DISCUSIÓN
La valoración del puntaje PESI forma parte de la estratificación inicial de los pacientes con TEP, tengan o no cáncer activo. En este sentido, se asume que los pacientes con TEP-CA serían de mayor riesgo que aquellos sin cáncer activo. Aquellos que presentan un puntaje PESI alto, dilatación del VD y elevación de troponinas son considerados pacientes con riesgo intermedio-alto de presentar una evolución desfavorable, y conforman el nicho de pacientes, junto con aquellos que presentan inestabilidad hemodinámica, en quienes se considerará la utilización de alguna terapia de reperfusión. De aquí se desprende la importancia de determinar si la sola presencia de cáncer activo podría impactar en el pronóstico de los pacientes con TEP. Existen diversos modelos que buscan identificar los pacientes con TEP-CA que tengan riesgo bajo de complicaciones y en quienes se podría ofrecer una alternativa terapéutica que pueda evitar o reducir el tiempo de internación. (18)
Al igual que lo observado en otros registros, (19,20) la MIH de los pacientes con TEP con valores de PESI ≥86 puntos fue elevada, aunque no observamos diferencias entre la población sin cáncer vs. con TEP-CA (8 % vs. 12,7 %, p=NS). A diferencia de lo observado en otros estudios, (21,22) donde los pacientes con TEP-CA son de mayor edad que aquellos sin cáncer, en nuestro estudio la población con TEP-CA resultó ser más joven. El análisis multivariado para MIH, con ajuste por edad, género, HTA y diabetes, no logró demostrar que el cáncer fuera un marcador independiente de pronóstico adverso; sin embargo, debe destacarse que los pacientes con cáncer tuvieron menor prevalencia de HTA, lo que pudo haber influido en el resultado. Por otra parte, es probable que el mayor riesgo de requerir ARM y DV en pacientes sin cáncer esté relacionado con la mayor prevalencia en esta población de predictores de pronóstico adverso, con mayor dilatación y disfunción del VD. Asimismo, las terapias de reperfusión se indicaron con mayor frecuencia en la población sin cáncer, lo cual sugiere que esta población era más grave. Estos hallazgos sugieren que el PESI tiene fundamentalmente valor predictivo negativo para pronóstico adverso; un valor de PESI elevado requeriría la presencia concomitante de dilatación y/o disfunción del VD y elevación de troponinas para predecir MIH.
Si bien en este trabajo no se evaluaron otros modelos predictivos útiles en TEP-CA, existe una diversidad de scores pronósticos con potencial utilidad. El modelo predictivo POMPE-C tendría adecuada precisión pronóstica para mortalidad a 30 días y un mejor rendimiento que el PESI. En el trabajo de Kline y col., el área bajo la curva ROC para POMPE-C fue 0,84 (IC95 % 0,82-0,88). Ningún paciente con un POMPE-C ≤5 % murió en un plazo de 30 días mientras que el 77 % con un POMPE-C >50 %, falleció en el seguimiento a 30 días. (23) El RIETE-VTE y el puntaje modificado de Ottawa son modelos de riesgo que tendrían utilidad para identificar pacientes con TEP-CA con riesgo bajo de MIH. En un estudio de Pfaundler y cols., ningún paciente clasificado como de riesgo bajo por los modelos RIETE-VTE o el puntaje modificado de Ottawa falleció
dentro de los 30 días. (24) El modelo HESTIA verificó que un puntaje total de cero coincidiría con una muy baja tasa de eventos adversos, aunque el mismo no ha sido suficientemente validado en pacientes con cáncer activo. (25) Roy y cols. compararon el modelo HESTIA y el PESIs para determinar cuál de ellos podría tener mayor precisión para detectar pacientes que pudieran realizar tratamiento ambulatorio. En el brazo del modelo HESTIA, el punto final primario a 90 días ocurrió en el 2,96 % vs. 1,40 %; p = NS. Ambos puntajes tuvieron similar eficacia y seguridad. (26)
El pronóstico de los pacientes con TEP-CA podría estar más determinado por el estado avanzado de la enfermedad oncológica y la condición general del paciente que por los puntajes de riesgo como el PESI. Li y cols. verificaron que en una población con TEP-CA, los pacientes que fallecieron dentro de los 30 días tuvieron una mayor proporción de cáncer metastásico y un Eastern Cooperative Oncology Group performance status ≥2. En dicho estudio observaron que la incidencia de muerte y eventos adversos se asoció con modelos más específicos para pacientes con TEP-CA (RIETE y POMPE-C) que con modelos más generales (PESI y HESTIA) o el puntaje de Ottawa modificado. Excepto para el puntaje HESTIA, que demostró una sensibilidad de 73,5 %, los cuatro puntajes restantes tuvieron una alta sensibilidad (>94 %) para mortalidad a 30 días. Todos estos modelos mostraron excelente valor predictivo negativo (>92 %) para mortalidad a 30 días, especialmente para los puntajes RIETE y POMPE-C (98,6 y 96,5 %, respectivamente). (18) Otros modelos como el EPIPHANY y el COMMAND VTE también tendrían utilidad en pacientes con TEP-CA, aunque los mismos no han sido validados suficientemente. (27,28)
Entre las múltiples limitaciones de este estudio, destacamos su naturaleza unicéntrica, por lo que la prevalencia de ciertos tipos de tumores podría ser diferente al de otras instituciones. No hubo seguimiento a 30 días, se incluyeron TEP incidentales, no se incluyeron pacientes ambulatorios; y no se consideraron la dilatación ni la disfunción del VD para el análisis multivariado.
El presente trabajo muestra que, en nuestro medio, los pacientes con PESI ≥86 puntos y cáncer tienen MIH alta, aunque no tendrían más mortalidad que los pacientes sin cáncer. Asimismo sugiere que el PESIs podría sobreestimar el riesgo en los pacientes con TEP-CA ya que ningún paciente con PESI <86 puntos con o sin cáncer falleció durante la internación. Son necesarios más estudios para verificar los hallazgos encontrados y evaluar la utilidad del PESI y otros modelos pronósticos en pacientes con TEP-CA.
CONCLUSIONES
En la población estudiada, los pacientes con TEP-CA con puntaje PESI intermedio o alto, no tuvieron mayor riesgo de presentar una evolución desfavorable. En esta población con cáncer, no se observó mayor mortalidad e incluso tuvieron menor requerimiento de ARM y DV.
Declaración de conflicto de intereses
Los autores declaran que no tienen conflicto de intereses.
(Véanse formularios de conflicto de intereses de los autores en la Web).
Financiamiento
No se recibió financiamiento para la realización del presente trabajo
Fuentes de apoyo: CEDECAFO, Instituto de Cardiología Hospital Universitario Austral.
https://creativecommons.org/licenses/by-nc-sa/4.0/

©Revista Argentina de Cardiología
BIBLIOGRAFÍA
- Khorana AA, Francis CW, Culakova E, Kuderer NM, Lyman GH. Thromboembolism is a leading cause of death in cancer patients receiving outpatient chemotherapy. J Thromb Haemost. 2007;5:632-4. https://doi.org/10.1111/j.1538-7836.2007.02374.x
- Lyman GH. Venous thromboembolism in the patient with cancer: focus on burden of disease and benefits of thromboprophylaxis. Cancer. 2011;117:1334-49. https://doi.org/10.1002/cncr.25714
- Mulder FI, Horváth-Puhó E, van Es N, van Laarhoven HWM, Pedersen L, Moik F, et al. Venous thromboembolism in cancer patients: a population-based cohort study. Blood. 2021;137:1959-69. https://doi.org/10.1182/blood.2020007338
- https://www.argentina.gob.ar/salud/instituto-nacional-del-cancer/estadisticas/mortalidad
- Brunson AM, Keegan THM, Mahajan A, White RH, Wun T. Cancer associated venous thromboembolism: incidence and impact on survival. Thromb Res.2018;164:178-9. https://doi.org/10.1016/j.thromres.2018.02.012
- Chew HK, Wun T, Harvey D, Zhou H, White RH. Incidence of venous thromboembolism and its effect on survival among patients with common cancers. Arch Intern Med.2006;166:458-64. https://doi.org/10.1001/archinte.166.4.458
- Sørensen HT, Mellemkjær L, Olsen JH, Baron JA. Prognosis of cancers associated with venous thromboembolism. N Engl J Med.2000;343:1846-50. https://doi.org/10.1056/nejm200012213432504
- Dentali F, Ageno W, Giorgi Pierfranceschi M, Imberti D, Malato A, Nitti C, et al. Prognostic relevance of an asymptomatic venous thromboembolism in patients with cancer. J Thromb Haemost. 2011;9:1081-3. https://doi.org/10.1111/j.1538-7836.2011.04259.x
- den Exter PL, Hooijer J, Dekkers OM, Huisman MV. Risk of recurrent venous thromboembolism and mortality in patients with cancer incidentally diagnosed with pulmonary embolism: a comparison with symptomatic patients. J Clin Oncol. 2011;29:2405-9. https://doi.org/10.1200/JCO.2010.34.0984
- Aujesky D, Obrosky DS, Stone RA, Auble TE, Perrier A, Cornuz J, et al. Derivation and validation of a prognostic model for pulmonary embolism. Am J Respir Crit Care Med.2005;172:1041-6. https://doi.org/10.1164/rccm.200506-862OC
- Jiménez D, Aujesky D, Moores L, Gómez V, Lobo JL, Uresandi F, et al; RIETE Investigators. Simplification of the pulmonary embolism severity index for prognostication in patients with acute symptomatic pulmonary embolism. Arch Intern Med.2010;170:1383-9. https://doi.org/10.1001/archinternmed.2010.199
- Burgos LM, Scatularo CE, Cigalini IM, Jauregui JC, Bernal MI, Bonorino JM, et al. External validation of prognostic scores for in-hospital and 30-day mortality in patients with pulmonary embolism in Argentina. MEDICINA (B AIRES).2020;80:462-72
- Konstantinides S, Meyer G, Becattini C, Bueno H, Geersing G, Harjola V y col. Guıía ESC 2019 para el diagnóstico y tratamiento de la embolia pulmonar aguda. Rev Esp Cardiol. 2020;73:497.e1-497. e58. https://doi.org/10.1016/j.recesp.2019.12.030
- Ubaldini J, Bilbao J, Spenatto M, Bonorino J et al. Consenso de enfermedad tromboembólica aguda. SAC 2016. Rev Argent Cardiol 2016;84:74-91.
- Flores LA, Ubaldini J, Kenar MR, Bilbao J, Bonorino J, Ceresetto J, et al. Guías de Manejo y Tratamiento de la Enfermedad Tromboembólica Aguda. Rev Arg de Ter Int. [Internet]. 7 de octubre de 2019 [citado 18 de septiembre de 2023];36(2). Disponible en: https://revista.sati.org.ar/index.php/MI/article/view/642
- Roy PM, Penaloza A, Hugli O, Klok FA, Arnoux A, Elias A, et al; HOME-PE Study Group. Triaging acute pulmonary embolism for home treatment by Hestia or simplified PESI criteria: the HOME-PE randomized trial. Eur Heart J. 2021;42:3146-57. https://doi.org/10.1093/eurheartj/ehab373
- Mehran R, Rao SV, Bhatt DL, Gibson CM, Caixeta A, Eikelboom J, et al. Standardized bleeding definitions for cardiovascular clinical trials: a consensus report from the Bleeding Academic Research Consortium. Circulation. 2011;123:2736-47. https://doi.org/10.1161/CIRCULATIONAHA.110.009449
- Li X, Hu Y, Lin P, Zhang J, Tang Y, Yi Q, et al. Comparison of Different Clinical Prognostic Scores in Patients with Pulmonary Embolism and Active Cancer. Thromb Haemost. 2021;121:834-44. https://doi.org/10.1055/a-1355-3549
- Pollack CV, Schreiber D, Goldhaber SZ, Slattery D, Fanikos J, O'Neil BJ, et al. Clinical characteristics, management, and outcomes of patients diagnosed with acute pulmonary embolism in the emergency department: initial report of EMPEROR (Multicenter Emergency Medicine Pulmonary Embolism in the Real World Registry). J Am Coll Cardiol. 2011;57:700-6. https://doi.org/10.1016/j.jacc.2010.05.071
- Cigalini I, Igolnikof D, Scatularo C, et al. Tromboembolismo pulmonar agudo en la Argentina. Registro CONAREC XX. Rev Argent Cardiol 2019;87:137-45.
- Cohen AT, Katholing A, Rietbrock S, Bamber L, Martinez C. Epidemiology of first and recurrent venous thromboembolism in patients with active cancer. A population-based cohort study. Thromb Haemost. 2017;117:57-65. https://doi.org/10.1160/TH15-08-0686
- Cai B, Bedayat A, George E, Hunsaker AR, Dill KE, Rybicki FJ, et al. Malignancy and Acute Pulmonary Embolism: Risk Stratification Including the Right to Left Ventricle Diameter Ratio in 1596 Subjects. J. Thorac. Imaging. 2013;28:196-201. https://doi.org/10.1097/RTI.0b013e3182870bf9
- Kline JA, Roy PM, Than MP, Hernandez J, Courtney DM, Jones AE, et al. Derivation and validation of a multivariate model to predict mortality from pulmonary embolism with cancer: The POMPE-C tool. Thromb Res.2012;129:e194-9. https://doi.org/10.1016/j.thromres.2012.03.015
- Pfaundler N, Limacher A, Stalder O, Méan M, Rodondi N, Baumgartner C, et al. Prognosis in patients with cancer-associated venous thromboembolism: Comparison of the RIETE-VTE and modified Ottawa score. J Thromb Haemost.2020;18:1154-61. https://doi.org/10.1111/jth.14783
- Zondag W, Mos IC, Creemers-Schild D, Hoogerbrugge AD, Dekkers OM, Dolsma J, et al; Hestia Study Investigators. Outpatient treatment in patients with acute pulmonary embolism: the Hestia Study. J Thromb Haemost.2011;9:1500-7. https://doi.org/10.1111/j.1538-7836.2011.04388.x
- Roy PM, Penaloza A, Hugli O, Klok FA, Arnoux A, Elias A, et al; HOME-PE Study Group. Triaging acute pulmonary embolism for home treatment by Hestia or simplified PESI criteria: the HOME-PE randomized trial. Eur Heart J. 2021;42:3146-57. https://doi.org/10.1093/eurheartj/ehab373
- Font C, Carmona-Bayonas A, Beato C, Reig Ò, Sáez A, Jiménez- Fonseca P, et al; Asociación para la Investigación de la Enfermedad Tromboembólica de la región de Murcia. Clinical features and short-term outcomes of cancer patients with suspected and unsuspected pulmonary embolism: the EPIPHANY study. Eur Respir J. 2017;49:1600282. https://doi.org/10.1183/13993003.00282-2016
- Yamashita Y, Morimoto T, Amano H, Takase T, Hiramori S, Kim K, et al; COMMAND VTE Registry Investigators. Usefulness of Simplified Pulmonary Embolism Severity Index Score for Identification of Patients With Low-Risk Pulmonary Embolism and Active Cancer: From the COMMAND VTE Registry. Chest. 2020;157:636-44. https://doi.org/10.1016/j.chest.2019.08.2206s