INTRODUCCIÓN
La aurícula izquierda (AI) es una estructura de fundamental importancia para la fisiología y la hemodinámica cardíaca. Sin embargo, por muchos años fue considerada únicamente como una cavidad con la función pasiva de conducir el flujo de sangre desde las venas pulmonares hasta el ventrículo izquierdo.
Existen múltiples métodos diagnósticos para detectar las alteraciones anatómicas y funcionales de la AI, pero su utilidad en la práctica cardiológica habitual no ha sido difundida, ni su implicancia en el desarrollo, progresión y complicaciones en múltiples patologías, entre las que destacan la insuficiencia cardíaca (IC), la fibrilación auricular (FA) y el accidente cerebrovascular.
Para la redacción de esta revisión se realizó una búsqueda exhaustiva y una revisión bibliográfica amplia acerca de la definición, fisiopatología, diagnóstico e implicancias diagnósticas actuales de la miopatía auricular en pacientes con insuficiencia cardíaca con fracción de eyección preservada. Se utilizaron las siguientes fuentes de información médica: bases de datos bibliográficos (MEDLINE), bases de medicina basada en la evidencia (Cochrane Library, Uptodate), revistas de la especialidad, guías de práctica clínica (Sociedad Europea de Cardiología, American College of Cardiology/American Heart Association), la biblioteca central del Hospital Italiano de Buenos Aires y la Revista Argentina de Cardiología.
Para la búsqueda se utilizaron las siguientes palabras y términos: “Miopatía auricular”, “Cardiomiopatía auricular”, “ICFEP” e “Insuficiencia cardíaca con fracción de eyección preservada” y sus equivalentes en inglés.
Definición
El término miopatía auricular surgió inicialmente en 1972 a raíz de un estudio publicado por Nagle et al. ( 1 ) en el que describieron un síndrome familiar que afectaba predominantemente la aurícula, asociado a trastornos de la conducción auriculoventricular. Una aproximación a su definición surgió en el año 2018, cuando la European Heart Rhythm Association en conjunto con la Heart Rhythm Society, Asia Pacific Heart Rhythm Society y la Sociedad Latinoamericana de Estimulación Cardíaca y Electrofisiología desarrollaron un consenso en el que definen a la miopatía auricular como “Cualquier complejo de cambios estructurales, arquitectónicos, contráctiles o electrofisiológicos que afecten a las aurículas y que puedan producir manifestaciones clínicamente relevantes”. ( 2 )
Fisiopatología
La AI cumple cinco funciones primordiales. Primero, funciona como una cavidad que recibe la sangre proveniente de las venas pulmonares. Segundo, posee una función contráctil que ayuda al llenado del ventrículo izquierdo al final de la diástole. Tercero, actúa como un conducto que permite el llenado pasivo del ventrículo izquierdo por diferencias de presiones. Cuarto, tiene la capacidad de detectar los cambios de volumen sanguíneo mediante barorreceptores, lo cual permite regular la liberación de péptidos natriuréticos y de ese modo regular la diuresis. Por último, posee mecanorreceptores que aumentan la tasa de descargas al nódulo sinusal, facilitando la taquicardia cuando aumenta el retorno venoso. ( 3 , 4 )
En cuanto a la fisiopatología de la miopatía auricular, se toman en consideración múltiples factores que pueden llevar al deterioro estructural y funcional de la AI. Shen et al. ( 5 ) proponen un modelo de estadificación de la progresión de la miopatía auricular que comienza con una aurícula normal, sobre la cual el efecto de factores como la edad, la inflamación, el agrandamiento auricular y el estrés oxidativo entre otros llevan a un estadio A, que se caracteriza por un alto riesgo de desarrollar miopatía auricular. Dichos factores de riesgo progresan produciendo fibrosis, remodelado estructural y alteraciones electrofisiológicas (estadio B), caracterizado por una miopatía auricular asintomática pero detectable por estudios de imágenes. En el estadio C se presentan las manifestaciones clínicas de una miopatía auricular reversible, y en el estadio D se produce una alteración irreversible de la aurícula.
Etiología
Múltiples etiologías se han asociado con el desarrollo de disfunción auricular. Entre las más frecuentes se encuentran: ( 6 )
-
Alteraciones del ritmo o la conducción: llevan a alteraciones estructurales y eléctricas de la aurícula. Pueden ser arritmias como la FA, o trastornos de la conducción que provocan un mal acoplamiento eléctrico auriculoventricular, como el bloqueo completo de rama izquierda o el bloqueo interatrial avanzado.
-
Cardiomiopatía auricular: Corresponde a un grupo de entidades que se caracterizan por la fibrosis auricular. Entre las más frecuentes están la fibrosis auricular idiopática, la isquemia auricular y la afectación auricular secundaria a miocarditis.
-
Remodelado auricular: Son entidades que producen alteraciones estructurales, electrofisiológicas y celulares en el tejido miocárdico auricular secundario a un aumento de la presión o de volumen de la AI. Entre las causas más frecuentes están la FA y las alteraciones del ventrículo izquierdo o de las válvulas auriculoventriculares.
Diagnóstico
Actualmente no existen criterios diagnósticos específicos para la miopatía auricular. Dentro de los estudios que aportan a la aproximación diagnóstica se cuentan el electrocardiograma (ECG), el ecocardiograma y la resonancia magnética. Se considera que para realizar un diagnóstico certero de miopatía auricular es necesario un estudio histológico del miocardio auricular. ( 7 )
En cuanto a los cambios electrocardiográficos que orientan a la identificación de miopatía auricular, destaca el bloqueo interatrial, que puede ser parcial, cuando la duración de la onda P es igual a o mayor de 120 ms, o avanzado, cuando la prolongación de la onda P se acompaña de cambios morfológicos en las derivaciones inferiores (ondas P bifásicas en DII, DIII y aVF). Existen además otros cambios que tienen implicación pronóstica en la miopatía auricular como la fuerza terminal de la onda P en V1 (>40 000 µV/ms) y el score MVP (Morphology-Voltage-P). ( 8 )
El score MVP se puede obtener a través de un ECG y se basa en 3 variables que son la morfología de la onda P en derivaciones inferiores (la morfología de bloqueo interatrial parcial equivale a 1 punto, y la de alto grado a 2 puntos), el voltaje en D1 (entre 0,20 y 0,10 mV equivale a un punto, y menos que 0,10 mV a 2) y la duración de la onda P (entre 120 y 140 ms equivale a un punto y mayor de 140 milisegundos equivale a 2). El score fue diseñado inicialmente para determinar a aquellos pacientes con alto riesgo de desarrollar FA: 0 a 2 puntos representa un riesgo bajo, 3 a 4 puntos un riesgo intermedio y 5 a 6 puntos un riesgo alto. Sin embargo, las variables que analiza, cómo el bloqueo interatrial y el voltaje de la onda P, son considerados marcadores de miopatía auricular. ( 9 )
La FA, como entidad, puede ser de utilidad para la aproximación diagnóstica a la miopatía auricular. La aparición de ondas f en el ECG puede ser un indicador de cambios electrofisiológicos y estructurales del miocardio auricular. Todavía existe debate acerca de que si la FA es un marcador de miopatía auricular o si, la arritmia per se cómo entidad patológica lleva al desarrollo de fibrosis auricular. ( 7 )
En cuanto a los parámetros ecocardiográficos que habitualmente se utilizan para la valoración de la estructura auricular se pueden mencionar la longitud anteroposterior de la AI, el área y el volumen de la AI (total e indexado a superficie corporal). ( 10 ) Para la valoración de la función de la AI se utilizan técnicas como el Doppler y el speckle tracking. ( 11 )
Mediante la ecocardiografía convencional es posible realizar diferentes cálculos basados en mediciones volumétricas para estimar la función de la AI. De tal modo que se pueden calcular: ( 12 - 14 )
-
Fracción de vaciamiento total de la AI = [(Volumen máximo de la AI - Volumen mínimo de la AI)/Volumen máximo de la AI] × 100. Representa la función de reservorio.
-
Índice de expansión de la AI = [(Volumen máximo de la AI - Volumen mínimo de la AI)/Volumen mínimo de la AI] × 100. Representa también la función de reservorio.
-
Fracción de vaciamiento pasivo de la AI = [(Volumen máximo de la AI - Volumen de la AI antes de la onda P en el ECG)/Volumen máximo de la AI] × 100. Representa la función de conducción.
-
Fracción de vaciamiento activo de la AI = [(Volumen de la AI antes de la onda P en el ECG - Volumen mínimo de la AI)/Volumen de la AI antes de la onda P en el ECG] × 100. Representa la función de contracción.
Adicionalmente a los parámetros anatómicos medidos por ecocardiografía convencional, mediante el uso del Doppler se pueden obtener datos indirectos acerca de la función de la AI, tales como la onda A pico y mediante Doppler tisular la onda A'; sin embargo, tienen la desventaja de ser dependientes de las condiciones de carga y la edad. ( 13 , 15 )
En la revisión de F. Triposkiadis et al. ( 16 ) se proponen 4 estadios de la disfunción de AI en pacientes con IC de acuerdo a parámetros ecocardiográficos.
-
Etapa 1: existe una prolongación de la relajación del ventrículo izquierdo que provoca una alteración en el vaciamiento pasivo de la AI. En el ecocardiograma se manifiesta con volúmenes y presiones de la AI conservados, con un aumento de la onda A en el Doppler.
-
Etapa 2: existe un aumento de la presión de la AI asociado a una disminución de la compliance ventricular. En el Doppler se evidencia un aumento de la onda E en relación a la onda A (pseudonormalización).
-
Etapa 3: existe una marcada dilatación de la AI, y la mayoría del llenado ventricular se desarrolla en la protodiástole. En el Doppler se evidencia un aumento más marcado de la onda E en relación a la onda A.
-
Etapa 4: se caracteriza fundamentalmente por un aumento del riesgo de desarrollar FA, con la consiguiente pérdida de la función de bomba de la AI. En el Doppler se evidencian ondas E en ausencia de ondas A.
Mediante el strain longitudinal de la AI se pueden medir tres fases del ciclo cardíaco: ( 17 )
-
Strain de reservorio: representa la contracción isovolumétrica del ventrículo izquierdo, eyección y relajación isovolumétrica. Se calcula restando el valor de pico de curva del strain menos el valor de fin de diástole. Se representa con un valor positivo.
-
Strain de conducción: representa el tiempo desde la apertura de la válvula mitral hasta el inicio de la contracción auricular en pacientes en ritmo sinusal (en pacientes con FA se considera hasta el cierre de la válvula mitral). Se calcula restando el valor del strain al inicio de la contracción auricular menos el valor pico de la curva de strain. Se representa con un valor negativo.
-
Strain de contracción: representa la contracción auricular en pacientes con ritmo sinusal y se calcula restando el valor del strain al final de la diástole menos el valor al inicio de la contracción auricular.
Pathan et al. ( 18 ) realizaron una revisión sistemática y metaanálisis para determinar los valores normales para el strain de la AI. Incluyeron 40 estudios (2542 pacientes) con información acerca de la función de reservorio; 14 estudios (805 pacientes) con información acerca de la función de conducción y 18 estudios (1005 pacientes) con información acerca de la función contráctil. Realizaron análisis para descartar fuentes de heterogeneidad, y definieron los siguientes puntos de corte para la normalidad: strain de reservorio: 39,4 % (IC95% 38,0 %-40,8 %), strain de conducción: 23,0 % (IC 95% 20,7 %-25,2 %) y strain de contracción 17,4 % (IC 95% 16,0 %-19,0 %).
Se ha descrito una correlación aceptable entre los parámetros de strain auricular medidos por ecocardiografía y mediciones invasivas de las presiones intracavitarias. En un estudio de Lundberg et al. ( 19 ) en el que fueron incluidos 164 pacientes que se sometieron a cateterismo cardíaco derecho por sospecha de IC, o disnea de causa no clara, se concluyó que la medición del strain longitudinal global de la AI es una herramienta útil y aplicable para la identificación de presiones elevadas de la AI y la estimación de las presiones de llenado del ventrículo izquierdo. Incluso se ha asociado al desarrollo de síntomas en pacientes en estadios tempranos de la IC, como en el estudio publicado por Maffeis et al. ( 20 ) en el que incluyeron a 185 pacientes en estadios A y B de IC con fracción de eyección preservada; la alteración de parámetros ecocardiográficos como el volumen indexado de la AI, el strain longitudinal pico y el strain de contracción tuvieron una asociación estadísticamente significativa con la presencia de síntomas en ambos estadios.
Los pacientes con IC con fracción de eyección preservada frecuentemente presentan diferentes grados de insuficiencia mitral secundaria como consecuencia de la dilatación de la AI o del ventrículo izquierdo. En el estudio publicado por Tamargo et al. ( 21 ) se incluyeron 280 pacientes que se realizaron un cateterismo cardíaco invasivo para evaluación de disnea de esfuerzo; la prevalencia de disfunción auricular, definida como un strain de reservorio menor de 24,5 %, fue dos veces mayor en aquellos pacientes con insuficiencia mitral en comparación con los pacientes con válvula mitral competente.
La resonancia magnética es una herramienta de fundamental importancia para el estudio de la anatomía y función auricular. La presencia de realce tardío de gadolinio a nivel de la AI se ha asociado a un riesgo elevado de desarrollar IC y al desarrollo de accidente cerebrovascular en este grupo de pacientes. En el estudio publicado por Zhou et al. ( 22 ) en el que incluyeron a 153 pacientes dialíticos de los cuales 96 presentaban IC con fracción de eyección preservada y 52 pacientes controles saludables, se realizó a todos análisis del strain de la AI mediante resonancia magnética; la medición del strain auricular aumentó la precisión diagnóstica por sobre los parámetros convencionales de la geometría auricular e índices ecocardiográficos para la identificación de pacientes con IC con fracción de eyección preservada.
En la Figura 1 se presenta un esquema de los diferentes métodos diagnósticos para el abordaje de la miopatía auricular.
Fig. 1
Esquema de métodos diagnósticos de la miopatía auricular.
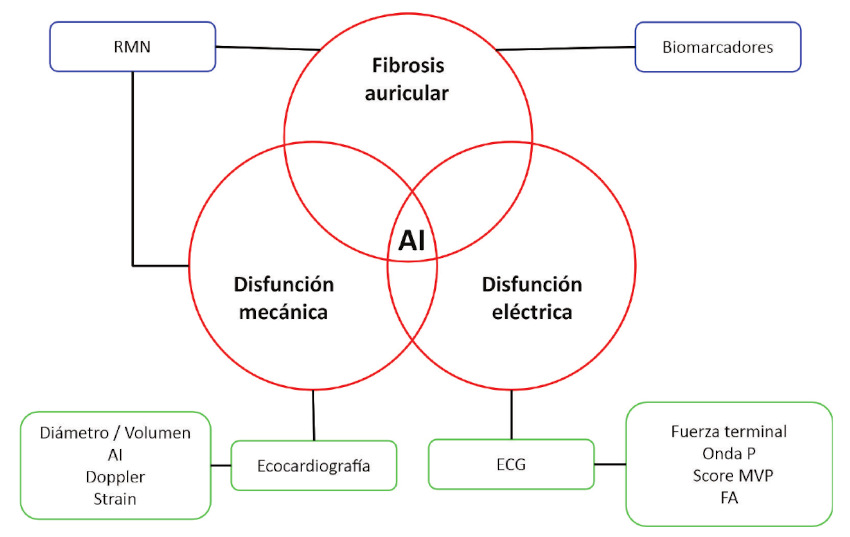
Realizando un abordaje fisiopatológico de la miopatía auricular basada en tres pilares fundamentales que son la fibrosis auricular, la disfunción mecánica y
la disfunción eléctrica, se realiza un esquema interpretativo de los métodos para la aproximación diagnóstica.
AI: Aurícula izquierda; ECG: Electrocardiograma; FA: Fibrilación auricular; MVP: Morphology-Voltage-P; RMN: Resonancia magnética nuclear.
Pronóstico
Las alteraciones estructurales de la AI se asocian a un pronóstico desfavorable en pacientes con IC independientemente de la fracción de eyección o de la presencia de arritmias. ( 23 , 24 ) En la población general un aumento del 30 % del volumen auricular izquierdo se asocia a un 43 % mayor riesgo de desarrollar FA y en pacientes mayores de 65 años duplica el riesgo de desarrollar IC.( 4 ) En una revisión sistemática y metaanálisis publicado por Khan et al. ( 25 ) en el que incluyeron 2 ensayos clínicos y 20 estudios observacionales con una población total de 1974 pacientes sintomáticos con IC con fracción de eyección preservada vs. 751 controles, las alteraciones como el aumento del volumen de la AI y la reducción del strain auricular fueron significativamente más marcadas en los pacientes con IC que en los controles; sin embargo, esto no se tradujo en mayor capacidad pronóstica para el punto final combinado de mortalidad por cualquier causa u hospitalizaciones por IC. Por otro lado, en el subestudio del Heart and Soul Study en el que se incluyeron 855 pacientes con enfermedad coronaria estable y fracción de eyección ventricular izquierda (FEVI) >50 %; la disminución del índice de función de la AI se asoció a un aumento del riesgo de hospitalización por IC, independientemente de variables como la edad, los factores de riesgo cardiovascular clásicos, y otros parámetros ecocardiográficos como el volumen indexado de la AI, la FEVI y el índice de masa ventricular izquierda. ( 26 )
En otro subestudio publicado en 2016 se consideró a pacientes enrolados en el estudio TOPCAT (Spironolactone for Heart Failure with Preserved Ejection Fraction). Se incluyeron 357 pacientes con IC con fracción de eyección preservada y con calidad de imagen por ecocardiografía, suficiente para realizar un análisis de la AI por speckle tracking. De aquellos pacientes con un volumen auricular normal, el 47% presentaba un strain auricular alterado, en comparación con un 71% de los pacientes con dilatación auricular. En un seguimiento promedio de 31 meses los valores más bajos de strain auricular pico se asociaron con el punto final primario compuesto de muerte cardiovascular, hospitalizaciones por IC y muerte súbita reanimada, además de a hospitalizaciones por IC. ( 27 )
En un análisis del estudio PARAMOUNT (LCZ696 Compared to Valsartan in Patients With Chronic Heart Failure and Preserved Left-ventricular Ejection Fraction) en el que incluyeron pacientes con IC con fracción de eyección preservada sintomáticos en clase funcional II – IV, analizaron a 135 pacientes con ritmo sinusal e imágenes ecocardiográficas con calidad suficiente para realizar un análisis de speckle tracking, comparados con 40 controles. Los valores de strain de reservorio, conducción y contracción fueron significativamente más bajos en los pacientes con IC que en los controles, incluso después de ajustar por variables como el volumen indexado de la AI, el volumen de fin de diástole del ventrículo izquierdo, el valor de E´ y las relaciones E/A y E/e´. Además se evidenció que valores más bajos de strain auricular sistólico se asociaron a mayor prevalencia de hospitalizaciones por IC e historia de FA. ( 28 )
Freed et al. ( 10 ) enrolaron prospectivamente a 308 pacientes que tuvieron internación por IC con fracción de eyección preservada a los cuales se les realizó un ecocardiograma con análisis de speckle tracking. Todos los parámetros del strain de la AI fueron predictores de hospitalización por causa cardiovascular y muerte. El strain de reservorio inclusive mantuvo utilidad pronóstica independientemente del antecedente de FA, el volumen de la AI y la masa ventricular izquierda.
Recientemente se publicó una revisión sistemática y metaanálisis en el que incluyeron 25 estudios de cohorte con un total de 252504 pacientes; se analizaron parámetros electrocardiográficos, ecocardiográficos y de laboratorio asociados a miopatía auricular y accidente cerebrovascular. Los resultados muestran que la fuerza terminal de la onda P en V1, el diámetro de la AI, el strain de reservorio y el valor del fragmento amino terminal del péptido B (NT-proBNP) se asociaron estadísticamente a un mayor riesgo de accidente cerebrovascular isquémico. ( 29 )
Implicancia terapéutica
Actualmente no existen terapias con eficacia comprobada para el tratamiento de la miopatía auricular. Sin embargo, sí las hay para el tratamiento de entidades estrechamente relacionadas como la IC y la FA. En pacientes con IC sintomática, tanto la Sociedad Europea de Cardiología como la Asociación Americana del Corazón recomiendan el uso de diuréticos de asa para el alivio sintomático. ( 30 , 31 ) En pacientes que presentan sobrecarga franca de volumen, la presión de la AI está típicamente elevada por lo que el tratamiento diurético es efectivo para el alivio sintomático; en cambio, el uso de diuréticos en pacientes en estado euvolémico con el objetivo de disminuir las presiones de la AI puede ser perjudicial y producir inclusive empeoramiento de la función renal. ( 32 )
En el 2018 se presentó el estudio REDUCE LAP-HF I (Transcatheter Interatrial Shunt Device for the Treatment of Heart Failure With Preserved Ejection Fraction) en el que incluyeron a 94 pacientes con IC con fracción de eyección preservada sintomáticos y con elevación de la presión de enclavamiento al final de la espiración durante una prueba con ejercicio. Los pacientes fueron asignados aleatoriamente 1:1 a un dispositivo de comunicación interauricular (Corvia Medical) o control. Al mes de seguimiento los pacientes en la rama de tratamiento presentaron mayor reducción de la presión de enclavamiento en comparación con los pacientes del grupo control, sin llegar a ser estadísticamente significativa (cambio en la presión de enclavamiento de -3,5 ± 6,4 mm Hg vs -0,5 ± 5,0 mm Hg, p=0,14). Ello no se tradujo en diferencias significativas en cuanto a eventos cardiovasculares o cerebrovasculares. ( 33 )
Posteriormente en el año 2022 se publicó el estudio REDUCE LAP-HF II (Atrial Shunt Device for Heart Failure with Preserved and Mildly Reduced Ejection Fraction) en el que 626 pacientes fueron asignados aleatoriamente 1:1 a colocación de un dispositivo de comunicación interauricular o a un procedimiento placebo. Tras una mediana de seguimiento de 2 años no se evidenciaron diferencias significativas en el punto final primario compuesto de muerte cardiovascular, accidente cerebrovascular isquémico no fatal a los 12 meses post aleatorización, eventos de IC o cambio en la calidad de vida medido por el cuestionario de Kansas, ni en sus componentes individuales. En el único punto en el que se demostró beneficio fue en el cambio de la clase funcional, pero los pacientes a los que se les colocó el dispositivo presentaron eventos cardiacos adversos (muerte cardíaca, infarto de miocardio, taponamiento cardíaco o cirugía cardíaca de emergencia) con mayor frecuencia que el grupo control. ( 34 )
CONCLUSIONES
La miopatía auricular es una entidad clínica subdiagnosticada, que tiene implicancias importantes en el diagnóstico y pronóstico de los pacientes con IC con fracción de eyección preservada. Sin embargo su utilidad como diana específica del tratamiento farmacológico y no farmacológico no ha podido aún ser demostrada.
Financiamiento
Este trabajo no recibió financiamiento público ni privado.
Declaración de conflicto de intereses
Los autores declaran que no tienen conflicto de intereses. (Véanse formularios de conflicto de intereses de los autores en la Web)
Agradecimientos
Agradecemos profundamente al Instituto de Medicina Cardiovascular del Hospital Italiano de Buenos Aires.
