CARTAS
CIENTÍFICAS
Estrategia híbrida. Un método innovador para el manejo de
cardiopatías congénitas complejas
La válvula aórtica bicúspide es un defecto
cardíaco congénito, que involucra un gran espectro de presentaciones, desde la
estenosis valvular aórtica con grave falla cardíaca en un recién nacido, hasta
la disección aórtica en adultos, o pasar inadvertida durante toda la vida sin requerir
tratamiento alguno.
Presentamos un paciente pretérmino
con diagnóstico prenatal de aorta bicúspide con estenosis grave. Al ingreso el
examen clínico muestra taquipnea y tiraje, coloración pálida-cianótica,
frecuencia cardíaca 187 latidos por minuto, R1 y R2 único, soplo sistólico
aórtico 2/6, pulsos braquiales y femorales simétricos, relleno capilar
prolongado, > 3 segundos. Tensión arterial 65/40 mm Hg; SatO2 78%. La
radiografía de tórax presenta cardiomegalia y edema pulmonar. Se coloca en asistencia
respiratoria mecánica y se administran prostaglandinas. El ecocardiograma Doppler color muestra estenosis aórtica crítica con
disfunción grave del ventrículo izquierdo (Figura 1A).

Fig. 1. Ecocardiograma Doppler
en donde se observa estenosis aórtica crítica (A). Angiografía desde acceso
carotideo post valvuloplastia aórtica (B).
Reconstrucción angiográfica de cerclaje quirúrgico de
ambas ramas pulmonares (C).
A las 18 horas de vida, se realiza
cateterismo cardíaco combinado y valvuloplastia
aórtica con balón híbrido (Tylsihak Mini, 6.0 ª 20
mm), mediante un acceso carotídeo derecho (disección)
(Figura 1B). Al cuarto día un ecocardiograma evidencia
gradiente transaórtico pico de 16 mmHg
con insuficiencia aórtica leve y comunicación interauricular amplia y ductus permeable.
Desde el quinto al decimotercer día de vida,
persiste inestabilidad hemodinámica con fallo multiorgánico
(insuficiencia renal, hemorragia intraventricular y
taquicardia supraventricular). Sin mejoría clínica,
se procede a cerclaje bilateral con banda de politetrafluoroetileno,
PTFE, (Figura 1C) y a las 48 horas se completa el
procedimiento híbrido (reapertura de esternotomía y
colocación de stent en ductus
tipo E de Kricenko de 1,7 mm).
A los 5 días del tratamiento el
ecocardiograma refleja disminución de los diámetros cardíacos, hipertrofia biventricular con mejoría de la función de ambos
ventrículos e incremento del gradiente a través de los cerclajes y a nivel del
tracto de salida del ventrículo izquierdo por mejoría de la función.
A los 3 meses del procedimiento híbrido se
procede a la remoción del cerclaje percutáneo (Figura 2A y 2B) y oclusión del stent ductal (Figura 2C).

Fig. 2. Angiografía. Dilatación de ambos cerclajes
de ramas pulmonares (A y B). Oclusión percutánea de stent
ductal (C).
La estenosis aórtica crítica neonatal, en la
que el miocardio inmaduro enfrenta un súbito aumento de la poscarga,
genera mayor estrés parietal con dilatación del ventrículo izquierdo, en lugar
de la hipertrofia compensadora encontrada en niños mayores. El aumento del
volumen y presión telediastólica alteran el flujo
coronario y provocan disfunción diastólica. (1,2) En el miocardio neonatal inmaduro existen problemas, a)
estructurales: los precursores miocíticos se replican
e incrementan su número (hiperplasia), pero no su tamaño (hipertrofia), las
miofibrillas están desorganizadas, hay escasa presencia del sistema tubular T y
del retículo sarcoplásmico mitocondrial, alta
concentración de ADN y predominio de elementos no contráctiles; b) biológicos,
como menor captación de calcio sarcoplásmico y menor
densidad de receptores alfa y beta; y c) metabólicos, como la utilización
preferente de la glucosa como vía energética. (2)
El abordaje híbrido en insuficiencias
cardíacas refractarias de distinta etiología es una alternativa terapéutica,
que consta en un cerclaje bilateral en ramas pulmonares, creación de una
comunicación interauricular (CIA) no
restrictiva y colocación de stent ductal. (3,4) El cerclaje pulmonar sobre el ventrículo derecho (VD)
provoca incremento de la contractilidad (efecto Anrep),
generando hipertrofia y la capacidad de regeneración de los miocitos
de un corazón inmaduro, y mejoría del llenado diastólico del VD. (3,4). Los cambios biológicos y genéticos a nivel de las
fibras compartidas por ambos ventrículos (co-hipertrofia)
puede restaurar la sincronía electromecánica entre ambos y el acoplamiento
ventrículo arterial. (5)
La evolución hemodinámica post valvuloplastia,
puede a veces ser desfavorable por un remodelado ventricular anormal con
consecuencias clínicas inesperadas. El abordaje híbrido es una técnica
innovadora de gran utilidad para diferentes escenarios de insuficiencia
cardíaca pediátrica inmanejables desde el punto de vista clínico, o como puente
a trasplante. Este abordaje pone en marcha varios mecanismos fisiológicos
provocando un apasionante equilibro eficiente entre presiones, flujos y
resistencias, corroborado por estudios computacionales de la dinámica de los
flujos. (6)
Declaración de
conflicto de intereses
Los autores
declaran que no tienen conflicto de intereses
(Véanse
formularios de conflicto de intereses de los autores en la web).
Consideraciones
éticas
No aplica
Edgardo Banille, Alejandro ContrerasMTSAC, Nora BuenoMTSAC,
Juan Diaz, Ignacio JuanedaMTSAC,
Alejandro PeironeMTSAC
Servicio de
Cardiología Pediátrica y Cirugía Cardiovascular. Hospital Privado Universitario
de Córdoba. Instituto Universitario de Ciencias Biomédicas de Córdoba.
E-mail: Ebanille@hotmail.com
Rev Argent Cardiol 2023;91:304-305. http://dx.doi.org/10.7775/rac.es.v91.i4.20656
1. Friedman
KG, Freud L, Escobar-Diaz M, Banka P, Emani S, Tworetzky W. Left Ventricular Remodeling and Function in
Children with Biventricular Circulation After Fetal Aortic Valvuloplasty.
Pediatr Cardiol 2015;36:1502-09.
https://doi.org/10.1007/s00246-015-1193-6
2. García
Guevara C, Cazzaniga M, Perez
Pedregoza J. El diagnóstico prenatal de las
cardiopatías congénitas. Capítulo 1. En: Banille E. Cardiointensivismo Pediátrico II. Una Mirada Ampliada. Tomo
I. Córdoba, Editorial RecFot, 2015.
3. Schranz D, Aknituerk H, Voelkel NF. “End stage” Heart failure therapy: potential
lesson from congenital heart disease: from pulmonary artery banding and interatrial communication to parallel circulation. Heart
2017;103:262-67. https://doi.org/10.1136/heartjnl-2015-309110
4. Schranz D, Rupp S, Muller M, et al. Pulmonary Artery
Banding in Infants and Young Children With Left Ventricular Dilated
Cardiomyopathy: A Novel Therapeutic Strategy Before Heart Transplantation. J Heart Lung Trasplant. 2013;475-81. https://doi.org/10.1016/j.healun.2013.01.988
5. Antonini-Canterin F, Poli S, Vriz O, et
al. The Ventricular-Arterial Coupling: From Basic
Pathophysiology to Clinical Application in the Echocardiography Laboratory. J Cardiovasc Echogr
2013;23:91-95. https://doi.org/10.4103/2211-4122.127408
6. De Campli WM, Argueta-Morales IR, Divo E, Kassab
AJ. Computational
fluid dynamics in congenital heart disease. Cardiol Young 2012; 22:800-08. https://doi.org/10.1017/S1047951112002028
Del paro al ECMO en el tromboembolismo de pulmón:
trabajo entre hospitales.
El tromboembolismo de pulmón
(TEP) es una entidad prevalente que compromete un gran espectro de pacientes,
con amplio rango de edades y comorbilidades. Puede afectar a pacientes jóvenes
sin comorbilidades relevantes, y causar un gran impacto en términos de
morbimortalidad. El TEP de alto riesgo es el que reviste mayor mortalidad,
sobre todo en aquellos que se presentan con paro cardiorrespiratorio (PCR).
Además es un porcentaje significativo el de los pacientes que manifiestan
síntomas de gravedad o descompensación hemodinámica a su ingreso o durante su
evolución. La estrategia indicada en estos pacientes es la reperfusión
inmediata. Lo más respaldado en la actualidad es la trombolisis
sistémica, dejando al tratamiento quirúrgico (ya sea embolectomía quirúrgica o
la asistencia con oxigenación por membrana extracorpórea venoarterial
(ECMO V-A) como una segunda opción, cuando el tratamiento médico falla o está
contraindicado. Sin embargo, existen datos de centros con experiencia que
sugieren que las técnicas quirúrgicas son seguras y efectivas. A continuación
se presenta un caso clínico acerca de un paciente con TEP masivo y PCR, donde
se lleva a cabo trabajo entre dos centros en pos de asistencia ventricular como
terapia de rescate.
Se presenta el caso de un paciente masculino de 39 años,
sin factores de riesgo ni antecedentes cardiovasculares, que como otros
antecedentes refiere haberse sometido a una cirugía de tendón de Aquiles 45
días previos a la consulta. Concurre al Servicio de Urgencias por haber
presentado en su domicilio un episodio de disnea súbita asociado a síncope sin
pródromos con traumatismo craneoencefálico (TEC) Durante su estadía en Guardia
presenta nuevo episodio sincopal. Se realiza un ecocardiograma transtorácico (ETT) Doppler (Figura 1) con evidencia de dilatación de cavidades derechas; por
lo que, asociado al antecedente reciente de cirugía traumatológica, se sospecha
TEP. Rápidamente evoluciona con PCR, por lo que se realizan maniobras de
reanimación cardiopulmonar avanzadas y se decide, debido a antecedente de TEC,
instaurar tratamiento percutáneo con tromboaspiración
y trombolíticos locales. El paciente evoluciona con
inestabilidad hemodinámica por lo que, tras descartar hemorragia intracraneal
con tomografía, se administran trombolíticos
sistémicos, a pesar de lo cual el paciente persiste con shock refractario a
dosis máximas de drogas vasoactivas. Se establece
contacto con Centro de Alta Complejidad y se activa el equipo de ECMO móvil. El
paciente es asistido con ECMO venoarterial en el
centro de origen una vez corregida la coagulopatía y
posteriormente se traslada al Centro de Alta Complejidad. El paciente ingresa
inestable hemodinámicamente, en asistencia
ventricular y respiratoria, con requerimiento de dosis máximas de noradrenalina,
vasopresina y milrinona; presenta en laboratorio
injuria renal y hepática agudas, acidosis metabólica con hiperlactacidemia
y coagulopatía marcada. Los valores de troponina T ultrasensible y de NT-proBNP
al ingreso son 6700 ng/L y 480 pg./ mL respectivamente. El electrocardiograma (Figura 2) evidencia taquicardia sinusal
y la radiografía de tórax, cardiomegalia y signos francos de redistribución de
flujo bilateral. Durante las primeras 24 horas el paciente persiste con shock
mixto (interpretado como cardiogénico y vasopléjico) con requerimiento de drogas vasoactivas, falla multiorgánica
y coagulopatía marcada; se establecen cuidados postparo, sostén hemodinámico, corrección del medio
interno, bajo asistencia ventricular. Tras corregir valores críticos de
fibrinógeno se instaura tratamiento anticoagulante con heparina sódica en
infusión continua, ajustado a valores de anti Factor Xa.
Evoluciona con descenso de drogas vasoactivas,
mejoría de la función ventricular derecha por ETT por lo que a las 72 horas se
realiza prueba de weaning de la ECMO que resulta
favorable y se decide retirar asistencia circulatoria sin complicaciones. El
paciente permanece bajo intubación orotraqueal, con
respuesta neurológica intacta y buen volumen urinario con respuesta a
diuréticos endovenosos (a pesar de valores séricos de creatinina en ascenso con
pico de 10 mg/dL, pero sin requerimiento de
hemodiálisis); por lo que al séptimo día de su ingreso la extubación
es exitosa. Realiza rehabilitación kinésica motora y respiratoria exhaustiva
posterior; se descarta síndrome antifosfolipídico y
otras trombofilias; realiza balance negativo con diuresis forzada a expensas de
furosemida con buena respuesta, por lo que retorna a su centro de origen para
continuar con la rehabilitación en sala general, con un ECG con evidencia de
aumento de los voltajes (Figura 2) y un ETT con función biventricular
completamente normalizada.
Fig. 1. Ecocardiograma transtorácico
al ingreso. A. Vista apical de 4 cámaras, fin de sístole. Se observa marcada
dilatación de cavidades derechas. B. Eje corto paraesternal.
Se observa la dilatación del ventrículo derecho, con aplanamiento del septum
interventricular.
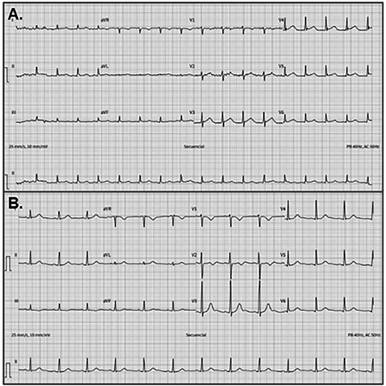
Fig. 2. A. Electrocardiograma al ingreso, taquicardia sinusal. B. Electrocardiograma al egreso, ritmo sinusal, frecuencia cardíaca normal con aumento de voltajes
a nivel generalizado, diferencia más marcada en precordiales derechas.
El TEP es una condición potencialmente mortal, por lo que
se trata de una urgencia cardiovascular, con una incidencia anual de 70 casos
por cada 100000 habitantes.(1) Se
trata de la tercera causa de muerte cardiovascular, detrás del infarto de
miocardio y accidente cerebrovascular.(2,3) La mortalidad de la embolia pulmonar masiva ronda el 30% mientras que en
aquéllos que experimentan paro cardiorrespiratorio puede ser cercana al 95%. (4) Las guías de práctica clínica actuales recomiendan la
terapia de reperfusión inmediata en pacientes con TEP
de alto riesgo: en los pacientes con descompensación hemodinámica se recomienda
trombolisis sistémica, dejando en un segundo lugar
los métodos invasivos (embolectomía quirúrgica o percutánea o asistencia
ventricular) cuando el primero está contraindicado o falla.(5) Sin
embargo en centros de alta complejidad con amplia experiencia en métodos
quirúrgicos (embolectomía y ECMO V-A), con la implementación de los mismos, se
ha visto disminuida drásticamente la mortalidad en los pacientes con TEP
masivo, incluyendo aquellos que han experimentado paro cardiorrespiratorio, a
los cuales se indica asistencia con ECMO con mortalidad cercana al 25%. (2,3) Por lo tanto, en un medio como el nuestro, se torna
fundamental la formación de equipos multidisciplinarios y multicéntricos,
que permitan, en primer lugar, la detección precoz de los pacientes con TEP de
alto riesgo para en un segundo lugar, establecer estrategias de actuación
acorde a cada paciente, como ser la derivación a centros de alta complejidad y
experiencia, y en caso de ser candidatos, poder llevar a cabo asistencia
ventricular o embolectomía quirúrgica cuando esté indicada. De esta manera,
generando redes interhospitalarias, de rápida identificación y respuesta,
podría verse disminuida la alta morbimortalidad que presenta este subgrupo de
alto riesgo. Por otro lado, cabe la reflexión de un cambio de paradigma en el
manejo de estos pacientes, ya que las técnicas quirúrgicas en centros donde
éstas están desarrolladas podrían implementarse como terapia inicial, en lugar
de terapia de rescate como ocurre actualmente, consiguiendo así un impacto
favorable en la evolución de estos pacientes. Podría tratarse de directivas
futuras a nivel mundial, que en nuestro medio impresionan no ser aún
reproducibles; sin embargo, con la potencial existencia de centros de
referencia que centralicen las derivaciones de centros circundantes de
pacientes con requerimiento de terapia quirúrgica de rescate, podría en un
futuro implementarse como terapia inicial de acuerdo con la experiencia.
Declaración de
conflicto de intereses
Los autores
declaran que no tienen conflicto de intereses
(Véanse
formularios de conflicto de intereses de los autores en la web).
Consideraciones éticas
No aplica
Julieta
Micaela Altimare1,
Jose Chas2, Rocío Blanco1, Mauro Gingins3, Horacio Avaca3, Anibal Arias1
1 Servicio de
Cardiología del Hospital Italiano de Buenos Aires
2 Servicio de Cirugía
Cardiovascular del Hospital Italiano de Buenos Aires
3 Servicio de
Cardiología del Hospital Británico
Rev Argent Cardiol 2023;91:305-307. http://dx.doi.org/10.7775/rac.es.v91.i4.20657
1. Ubaldini J, Bilbao J, Spennato
Mario C, Bonorino J, Flores LA, Kenar
M, et al. Consenso de Enfermedad Tromboembólica
Aguda. JE Ubaldini, et al. Rev
Argent Cardiol 2016;84:74-91. http://dx.doi.org/10.7775/rac.es.v84.i1.7739
2. Goldberg JB, Giri J, Kobayashi T, Ruel M, Mittnacht AJC, Rivera- Lebron B,
et al. Surgical Management and Mechanical Circulatory Support
in High-Risk Pulmonary Embolisms: Historical Context, Current Status, and
Future Directions: A Scientific Statement From the American Heart Association. Circulation 2023;147:e628-47. https://doi.org/10.1161/CIR.0000000000001117
3. Goldberg
JB, Spevack DM, Ahsan S, Rochlani Y, Dutta T, Ohira S. Survival and Right Ventricular Function After
Surgical Management of Acute Pulmonary Embolism. J Am Coll Cardiol 2020;76:903–11. https://doi.org/10.1016/j.jacc.2020.06.065
4. Laher AE, Richards G. Cardiac arrest due to pulmonary embolism.
Indian Heart J 2018;70:731-5. https://doi.org/10.1016/j.ihj.2018.01.014
5. Konstantinides SV, Meyer G, Becattini
C, Bueno H, Geersing GJ, Harjola VP, et al. 2019 ESC Guidelines for the diagnosis
and management of acute pulmonary embolism developed in collaboration with the
European Respiratory Society (ERS). Eur Heart J 2020;41:543- 603. https://doi.org/10.1093/eurheartj/ehz405
Disfagia: presentación inusual de una complicación poco frecuente derivada
del implante de un marcapasos
Presentamos el caso de un paciente de 63 años que ingresó
al servicio de urgencias por disfagia. Refería distensión del lado izquierdo
del cuello, que posteriormente afectó su capacidad para comer adecuadamente.
Estos síntomas aparecieron después del implante de un marcapasos, realizado dos
semanas antes, por un bloqueo auriculoventricular de
segundo grado. No se observaron síntomas de insuficiencia cardíaca, síncope, presíncope, palpitaciones, mareos, síntomas
constitucionales ni fiebre. En la exploración física se observó asimetría
cervical, con distensión del lado izquierdo, acompañada de calor local y
discreta asimetría entre los brazos derecho e izquierdo. El resto de la
exploración física fue anodina. El paciente tenía antecedentes de
esquizofrenia, depresión y dislipidemia. Después de
un procedimiento invasivo, los autores sospecharon de una infección relacionada
con el procedimiento, como punto de origen.
Se realizó una tomografía computarizada (TC) en la que se
observó trombosis de la vena yugular interna izquierda, con oclusión de las
venas braquiocefálica y subclavia izquierdas (Fig. 1).
No se apreciaron colecciones ni abscesos. Se realizó una ecocardiografía transtorácica (ETT) en el servicio de urgencias, la que
suscitó sospechas de trombo/endocarditis. En la ecocardiografía transesofágica (ETE) posterior se comprobó la presencia de
un trombo adherido a los cables conductores del marcapasos. En las imágenes se
observó una vegetación dudosa. Se tomaron muestras de sangre para hemocultivo,
y se determinaron las concentraciones de proteína C-reactiva (PCR) y procalcitonina (PCT). Se programó una nueva TC para
determinar la existencia de embolia pulmonar.
Fig. 1. TC: plano axial. Desplazamiento de la carina por trombosis de la vena yugular y edema ipsilateral.
De inmediato, se inició la anticoagulación con heparina
de bajo peso molecular (HBPM). Los resultados del hemocultivo y la PCT se
encontraron dentro de los parámetros normales. No hubo indicios de embolia
pulmonar, según la nueva TC.
Después del tratamiento con HBPM durante una semana, se
produjo la resolución completa del trombo (Fig. 2).
El paciente también fue atendido en una clínica de inmunohemoterapia,
y se descartó trombofilia. A los 12 meses de seguimiento, el paciente sigue
asintomático y se encuentra bien.
Fig. 2. ETE: plano bicavo. Imagen de
los cables del marcapasos después de la anticoagulación; no hay evidencia de
trombo.
Las complicaciones notificadas de los marcapasos
permanentes se relacionan principalmente con riesgos de infección y trombosis,
y eventos embólicos. Las otras complicaciones menos
frecuentes mencionadas anteriormente quedan fuera del alcance de este artículo.
(1) Se han informado eventos trombóticos
graves relacionados con el implante del marcapasos en el 0,6% al 3,5% de los
casos. Estos eventos graves incluyen insuficiencia cardíaca y tromboembolia
pulmonar. (2) Sin embargo, los trombos clínicamente asintomáticos
parecen ser mucho más frecuentes, y su incidencia es del 35% al 45% en las
mismas cohortes. (3) Los casos
sintomáticos pueden presentarse en un contexto agudo, subagudo o tardío, en
función del tiempo transcurrido desde del implante del marcapasos, el cual
puede variar de días a años. (2,4) En los casos agudos parece haber un estado de hipercoagulabilidad
y traumatismo endotelial que favorece la trombosis. (5) No
hay consenso sobre la estrategia terapéutica y el seguimiento de los pacientes
con trombosis sintomática inducida por los cables conductores del marcapasos.
En algunos casos, se analiza el uso del tratamiento médico oral frente al
intravenoso, así como las opciones de trombectomía
mecánica y trombólisis, sobre todo en los casos
agudos. (2)
Exponemos un caso de presentación atípica de trombosis
con disfagia como síntoma más importante. La evaluación ecocardiográfica
y el tratamiento oportuno pueden ser esenciales para prevenir, evitar y mejorar
los desenlaces clínicos en estos pacientes, sin necesidad de recurrir a una
intervención. Nuestro objetivo es concientizar al lector sobre el hecho de que
la trombosis aguda derivada del implante del marcapasos es una entidad que
requiere el reconocimiento de la comunidad médica para lograr un diagnóstico
precoz y evitar desenlaces clínicos desfavorables. Las presentaciones atípicas
no deben desestimarse, y el tiempo transcurrido desde la intervención debe
hacernos sospechar de una posible vinculación. Además, se debe considerar que
no todo lo que está unido a los cables del marcapasos o relacionado con una
intervención reciente es una vegetación.
Declaración de
conflicto de intereses.
Los autores
declaran que no tienen conflicto de intereses.
(Véanse
formularios de conflicto de intereses de los autores en la web/Material
suplementario).
Francisco Dias Claúdio1, 2, Rita Rocha1, 2, David Neves1,2, Pedro Semedo1,2, Manuel Trinca1 Lino Patrício1, 2
1 Departamento de
Cardiología, Hospital Espírito Santo - Évora, Évora, Portugal
2 C-TRAIL - Alentejo Academic Clinic Center, Évora,
Portugal
Autor para
correspondencia: Francisco Dias
Cláudio - Departamento de Cardiología - Hospital
Espírito Santo – Évora - Largo do Sr. da Pobreza - 7000-811 Évora, Portugal -
Correo electrónico: Francisco.dias.claudio@gmail.com
Rev Argent Cardiol 2023;91:307-308. http://dx.doi.org/10.7775/rac.es.v91.i4.20655
1. Phibbs B, Marriott HJL. Complications of
permanent transvenous pacing. N Engl J Med 1985;312:1428–32. https://doi.org/10.1056/NEJM198505303122205
2. Zimetbaum P, Carroll BJ, Locke AH,
Secemsky E, Schermerhorn M.
Lead-Related Venous Obstruction in Patients With Implanted Cardiac Devices:
JACC Review Topic of the Week. J Am Coll Cardiol 2022;79:299–308. https://doi.org/10.1016/j.jacc.2021.11.017
3. Barakat K, Robinson NM, Spurrell
RAJ. Transvenous pacing lead-induced thrombosis: a
series of cases with a review of the literature. Cardiology 2000;93:142–8.
https://doi.org/10.1159/000007018
4. Van Rooden CJ, Molhoek SG, Rosendaal FR, Schalij MJ, Meinders AE, Huisman MV.
Incidence and Risk Factors of Early Venous Thrombosis Associated with Permanent
Pacemaker Leads. J Cardiovasc Electrophysiol 2004;15:1258–62. https://doi.org/10.1046/j.1540-8167.2004.04081.x
5. Spittell PC, Hayes DL. Venous Complications After Insertion of a Transvenous
Pacemaker. Mayo Clin Proc
1992;67:258–65. https://doi.org/10.1016/S0025-6196(12)60103-7
![]() https://creativecommons.org/licenses/by-nc-sa/4.0/
https://creativecommons.org/licenses/by-nc-sa/4.0/
©Revista
Argentina de Cardiología