CARTAS
CIENTÍFICAS
http://dx.doi.org/10.7775/rac.es.v91.i3.20638
Infarto agudo de
miocardio por embolismo coronario en una mujer joven con prótesis valvular
mecánica aórtica y origen anómalo de dos vasos coronarios: reporte de un caso
Las
valvulopatías afectan aproximadamente al 2,5% de los adultos en países
desarrollados. Desde 1960 el reemplazo valvular con prótesis mecánicas es una
de las alternativas terapéuticas para el manejo de la enfermedad valvular. Su
principal complicación es el desarrollo de trombosis o fenómenos embólicos, con
una incidencia anual estimada del 0,3-1,3% y del 0,7-6%, respectivamente. (1) El riesgo
está incrementado en los primeros meses de implante, según su posición
anatómica y su asociación con otros factores de riesgo tromboembólicos (por
ej., fibrilación auricular).
Presentamos
un caso de infarto agudo de miocardio con elevación del segmento ST en una
mujer joven con prótesis valvular aórtica que había suspendido voluntariamente
la anticoagulación.
Mujer
de 23 años, procedente del Pacífico colombiano, con antecedente de
insuficiencia mitral con implante de prótesis valvular mecánica a los 8 años,
anticoagulada con warfarina hasta hace 2 años, cuando suspendió el tratamiento
médico. Consultó al servicio de urgencias por 8 horas de dolor torácico
opresivo de alta intensidad con irradiación al miembro superior derecho, sin
otros síntomas asociados. Al examen físico se encontraba afebril, con presión
arterial de 121/76 mm Hg, frecuencia cardíaca 82 lpm y frecuencia respiratoria
19 rpm. La auscultación reveló un soplo holosistólico en el foco mitral de
grado III / VI, y un soplo diastólico en el foco aórtico de grado III / VI, sin
signos de insuficiencia cardíaca aguda y sin otros hallazgos relevantes. El
electrocardiograma demostró ritmo sinusal con elevación del segmento ST de V1 a
V3 e infradesnivel del segmento ST en cara inferior, con presencia de ondas Q
patológicas en DI y aVL, y signos de crecimiento ventricular izquierdo. Se
realizó coronariografía de urgencia a las 12 horas del ingreso, que documentó
una oclusión total de aspecto crónico en el segmento medio-proximal en la
arteria descendente anterior (Figura 1) y una lesión trombótica en la primera obtusa marginal de la
circunfleja, con una estenosis del 90% (Figura
2), sin otras lesiones angiográficamente significativas. Se
evidenció pérdida de la movilidad de uno de los hemidiscos de la prótesis
valvular mecánica de doble disco, por trombo in situ.
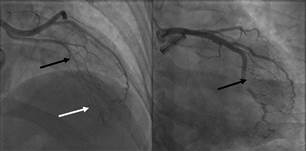
Fig. 1. Izquierda: Oclusión crónica de la arteria descendente anterior
en la unión del segmento proximal y medio (flecha negra) con circulación
colateral hetero y homocoronaria (flecha blanca). Derecha: Arteria obtusa
marginal con defecto de lleno compatible con trombo que genera suboclusión y
flujo TIMI 2 (flecha negra).
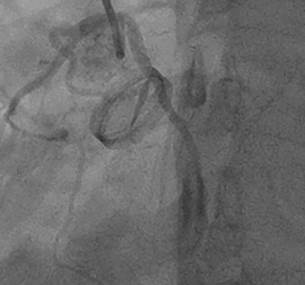
Fig. 2. Pérdida de la movilidad de uno de los hemidiscos de la prótesis
mecánica de doble disco por trombo in situ.
Como
hallazgo incidental se demostró origen anómalo de la arteria coronaria derecha
y de una segunda arteria obtusa marginal, de forma independiente desde el seno
coronario izquierdo. Debido al alto riesgo de trombosis protésica, inicialmente
se decidió anticoagular con heparina de bajo peso molecular y warfarina hasta
alcanzar metas del índice internacional normalizado (INR). En el laboratorio,
troponina cardíaca I positiva (6,53 ng/mL para un límite superior normal de
0,12 ng/mL). El ecocardiograma transesofágico evidenció acinesia sin
adelgazamiento de las paredes anterolateral e inferolateral, con una fracción
de eyección ventricular izquierda de 47% por el método de Simpson; prótesis
aórtica mecánica en adecuada posición con restricción al movimiento del velo en
localización posterior, y presencia de pannus y marcada turbulencia en
el flujo anterógrado, con una velocidad máxima de 3,2 m/s con un gradiente
medio de 22,5 mm Hg e insuficiencia mitral grave secundaria a perforación del
velo anterior.
Con
estos hallazgos fue llevada a cambio de prótesis aórtica por una prótesis
mecánica Medtronic n.° 23. Se realizó agrandamiento del anillo aórtico con
parche pericárdico heterólogo con técnica de Manougian, y reparación de la
válvula mitral con cierre del orificio del velo anterior. Se encontraron en la
prótesis mecánica aórtica trombos frescos a nivel de la bisagra de ambos discos
y pannus severo subvalvular. No fue posible realizar la revascularización de la
arteria descendente anterior al no poderse visualizar su trayecto por presencia
de adherencias epicárdicas-pericárdicas de la cirugía previa, por lo cual se
indicó angioplastia coronaria. En la segunda coronariografía realizada a los 25
días del ingreso, se encontró resolución completa de la lesión trombótica en la
arteria obtusa marginal. Persistía la oclusión total de la arteria descendente
anterior, pero no fue posible realizar revascularización percutánea al
encontrase vaso con pequeño calibre. Se decidió continuar tratamiento médico,
acompañamiento por el servicio de Psicología y educación; se dio de alta
después de 41 días de hospitalización, sin complicaciones, con un INR de 3,2 y
con indicaciones de control médico estricto.
La
cardiopatía isquémica es la principal causa de muerte a nivel mundial, asociada
principalmente a ateroesclerosis. Hasta en un 7% de los casos no se encuentran
lesiones ateroscleróticas significativas. La embolia coronaria es una causa de
infarto no aterosclerótico, y se estima que representa el 3% de todos los
infartos de miocardio. Generalmente afecta la circulación coronaria izquierda, (1) como en el
caso de nuestra paciente.
Las
principales causas asociadas son fibrilación auricular, miocardiopatías,
presencia de prótesis valvulares, endocarditis, tumores y estados
protrombóticos. Existen reportes de trombosis coronaria asociada a infección
aguda por SARS-CoV-2 durante la época de pandemia por esta entidad. (2) Antes del uso
de válvulas protésicas la endocarditis constituía la causa principal;
actualmente se considera principalmente a la fibrilación auricular. (1) Actualmente,
el reemplazo valvular protésico es el estándar de oro de manejo de las valvulopatías
graves en pacientes con riesgo quirúrgico bajo o intermedio. Las válvulas
mecánicas cuentan con mayor vida de uso, pero son protrombóticas, por lo cual
requieren anticoagulación indefinida para evitar trombosis valvular y fenómenos
embólicos.
Existen
tres tipos de embolia coronaria: de forma directa, paradójica e iatrogénica. El
embolismo coronario directo ocurre al ingresar un émbolo a la circulación
coronaria proveniente del ventrículo izquierdo, la orejuela de la aurícula
izquierda, venas pulmonares, válvula aórtica o mitral. (3)
Las
manifestaciones clínicas, electrocardiográficas y ecocardiográficas del infarto
de miocardio por embolia coronaria son indistinguibles del infarto de origen
aterosclerótico; debe sospecharse ante dolor torácico súbito en pacientes con
factores de riesgo protrombóticos. (4)
No
existen actualmente guías para el manejo de la embolia coronaria. Se ha
comparado la aspiración de trombo intracoronario vs. angioplastia sola en
pacientes con infarto con elevación del ST, sin demostrar un beneficio
adicional en la mortalidad. Sin embargo, los pacientes con alta carga
trombótica, como los pacientes con embolia coronaria, podrían tener mayor
beneficio con esta medida. (5) Existen reportes de trombolisis sistémica en casos de embolismo
coronario con activador de plasminógeno tisular (t-PA), con éxito en
restauración de flujo coronario. Karakoyun et al (5) trataron con éxito y de forma segura con t-PA en dosis bajas
intravenosas, a tres pacientes con embolia coronaria asociada a válvulas
protésicas. Así mismo, hay reporte de infusión endovenosa de bivalirudina por
48 horas en embolismo coronario de la arteria coronaria derecha distal, con
resolución completa del trombo sin sangrados mayores. (6) Otras terapias incluyen la angioplastia con balón, que ha
demostrado éxito en la restauración del flujo sanguíneo, tanto de forma
aislada, como empleada como terapia complementaria a la aspiración trombótica. (5)
En
conclusión, describimos el caso de una mujer joven con prótesis valvular
mecánica aórtica quien suspendió voluntariamente la anticoagulación y que
presentó un infarto agudo de miocardio por embolia coronaria. Esta condición es
potencialmente fatal, por lo que es esencial la adherencia al tratamiento
farmacológico y la educación respecto de la enfermedad en un paciente con alto
riesgo de trombosis. La anticoagulación permanente, el seguimiento clínico
estricto y la educación del paciente, son las medidas más importantes para
prevenir nuevos eventos.
Declaración de conflicto de intereses:
Los
autores declaran que no tienen conflicto de intereses
(Véanse
formularios de conflicto de intereses de los autores en la web/Material
suplementario).
Consideraciones éticas
No
aplica
Fernando
Araque-Villaquirán, Raúl Vallejo-Serna, Mónica Fernandes Pineda, Álvaro
Herrera-Escandón
Departamento
de Medicina Interna, Universidad del Valle. Cali, Colombia.
Institución:
Hospital Universitario del Valle, Santiago de Cali - Colombia.
Autor para separatas: Mónica
Fernandes Pineda Dirección postal: 760032. Correo electrónico: monica.fernandes.pineda@gmail.com
1.
Roudaut, R., Serri, K., & Lafitte, S. (2007). Thrombosis of prosthetic heart valves:
diagnosis and therapeutic considerations. Heart (British Cardiac Society),
93(1), 137–142. https://doi.org/10.1136/hrt.2005.071183
2. Prizel KR, Hutchins GM, Bulkley BH.
Coronary artery embolism and myocardial infarction. Ann Intern Med. 1978
Feb;88(2):155-61. doi: 10.7326/0003-4819-88-2-155.
3. Chikkabasavaiah N, Rajendran R.
Percutaneous coronary intervention for coronary thrombo embolism during balloon
mitral valvuloplasty in a pregnant woman. Heart Lung Circ 2016;25:e29-31.
4. Lacey MJ, Raza S, Rehman H, Puri R,
Bhatt DL, Kalra A. Coronary Embolism: A Systematic Review. Cardiovasc Revasc
Med. 2020 Mar;21(3):367-374. doi: 10.1016/j.carrev.2019.05.012.
5. Karakoyun S, Gürsoy MO, Kalçık M,
Yesin M, Özkan M. A case series
of prosthetic heart valve thrombosis-derived coronary embolism. Turk Kardiyol
Dern Ars. 2014 Jul;42(5):467-71. doi: 10.5543/tkda.2014.05031.
6. Steinwender C, Hofmann R, Hartenthaler B, Leisch F.
Resolution of a coronary embolus by intravenous application of bivalirudin. Int
J Cardiol. 2009 Mar 6;132(3):e115-6. doi: 10.1016/j.ijcard.2007.08.032.
http://dx.doi.org/10.7775/rac.es.v91.i3.20643
Asistencia ventricular extracorpórea
en el paro cardiaco intrahospitalario: ¿una realidad posible en nuestro medio?
La reanimación
cardiopulmonar extracorpórea (RCPE) es la utilización de la oxigenación por
membrana extracorpórea (ECMO) en pacientes en los que las medidas de
reanimación cardiopulmonar convencional (RCPC) no logran un retorno sostenido
de la circulación espontánea luego de un paro cardiorrespiratorio (PCR). (1) Los pacientes en los que
se implanta una ECMO durante o inmediatamente después de un PCR tienen un
pronóstico especialmente desfavorable. (2)
Pese a que no hay
recomendaciones sistemáticas vigentes de la indicación de ECMO en el PCR,
podría considerarse como una terapia emergente cuando la reanimación
cardiopulmonar convencional falla en casos seleccionados. (3)
Actualmente, no hay reportes de ensayos aleatorizados controlados que comparen
los resultados de RCPE con RCPC en el PCR intrahospitalario. (1) Múltiples estudios de
cohorte han demostrado que dicha terapéutica se asocia con una mayor tasa de
supervivencia hasta el alta y resultados neurológicos favorables. (4) En nuestro conocimiento,
existe limitada información publicada en nuestro medio.
El objetivo de
este estudio fue analizar e informar las características y los resultados
clínicos de una cohorte retrospectiva y consecutiva de pacientes adultos
tratados con RCPE después de un paro cardíaco intrahospitalario (PCRIH) en un
centro de alta complejidad de Argentina.
Se analizaron
pacientes mayores de 18 años que fueron asistidos con ECMO venoarterial (VA)
por PCRIH entre 2014 y 2022. Se incluyeron pacientes con PCRIH presenciado, de
probable causa cardíaca (principalmente con taquicardia ventricular o
fibrilación ventricular como ritmo de inicio, que se extendieron más de 20 minutos),
(1)
aún con una adecuada reanimación cardiopulmonar desde el inicio del mismo. Se
excluyeron aquellos con PCR en cirugía cardíaca. En la Tabla
1
se resumen los criterios de inclusión para RCPE de nuestro centro.
Tabla 1:
Criterios de Inclusión para ECPR
|
Edad
< 70 años |
|
RCP
intrahospitalaria |
|
Tiempo
al inicio de la primera RCP < 5 minutos |
|
Ritmo
cardíaco inicial de fibrilación ventricular, taquicardia ventricular o
actividad eléctrica sin pulso |
|
Tiempo
estimado de PCR a flujo ECMO < 60 minutos |
|
Retorno
de la circulación espontánea intermitente o FV recurrente |
|
Ausencia
de comorbilidades limitantes de vida previamente conocidas |
ECMO:
oxigenación por membrana intracorpórea; FV: fibrilación ventricular; PCR: paro
cardiorrespiratorio; RCP: reanimación cardiopulmonar
Se realizó un
análisis de la base de datos de asistencia ventricular, que es completada en
forma prospectiva, e incluye entre las variables principales, las
características demográficas, información del tipo de asistencia ventricular,
complicaciones, eventos clínicos de relevancia, y predictores de evolución
clínicos, bioquímicos, y ecocardiográficos. Respecto a los eventos clínicos de
relevancia, se evalúan dos tipos de sobrevida:
– Sobrevida en
ECMO: Evalúa la supervivencia en ECMO, y hasta las 24 horas del destete de la
asistencia ventricular. En este caso, los motivos de desvinculación de la ECMO
son por recuperación de la función cardíaca o porque se realizó un trasplante
cardíaco.
– Sobrevida al
alta: Evalúa la supervivencia al alta hospitalaria, ya sea por alta sanatorial
o derivación a otro centro sanitario (por ej., tercer nivel de rehabilitación).
Además, se
analizaron las complicaciones neurológicas: muerte cerebral (pérdida
irreversible de la conciencia y de las funciones neurovegetativas, incluida la
capacidad de respirar), y accidente cerebrovascular (foco neurológico agudo, y
cambios isquémicos o hemorrágicos nuevos en la tomografía de cerebro).
Se incluyeron en
el análisis 8 pacientes, representando el 11,9% de los ECMO VA implantados en
ese periodo en el centro. La mediana (rango intercuartílico, RIC) de edad fue
46 años (30-58); el 66% eran mujeres. Tres pacientes tenían antecedentes de
hipertensión arterial y dislipemia, y uno de diabetes. Ningún paciente presentó
antecedentes de enfermedad pulmonar obstructiva, enfermedad renal crónica,
accidente cerebrovascular (ACV), enfermedad vascular periférica, fibrilación
auricular o anemia.
Tres pacientes
presentaron de base un síndrome coronario agudo, dos tormenta eléctrica, y las
causas restantes fueron miocardiopatía periparto, miocarditis y miocardiopatía
restrictiva no filiada.
La canulación fue
periférica en el 87,5% de los casos (7 pacientes). El mismo número requirió la
utilización de balón de contrapulsación intraaórtico y en dos casos se requirió
descompresión quirúrgica del ventrículo izquierdo, mediante venting de
la vena pulmonar. El 100% de las ECMO se implantaron como estrategia de puente
a la recuperación.
La mediana de
duración de la asistencia circulatoria fue de 5 días (RIC 2-8). Se pudo extraer
la ECMO VA de forma exitosa en 5 pacientes.
La tasa de
supervivencia en ECMO VA fue del 62,5% (n = 5), y al alta del 37,5% (n = 3). La
causa de muerte fue no cardiovascular en 4 de los 5 fallecidos.
Las complicaciones
reportadas incluyen: hemorragia mayor (66%), insuficiencia renal aguda no
dialítica (66%), infección (33%), convulsiones (11%) y complicaciones
tromboembólicas (33%). No se reportó ninguna muerte cerebral, y 1 paciente tuvo
un accidente cerebrovascular isquémico.
La mediana de
seguimiento luego del alta fue de 14 meses (RIC 7-30). De los 3 pacientes que
sobrevivieron, uno se encuentra en lista de trasplante cardíaco electivo y dos
en seguimiento con función biventricular conservada.
La RCPE se utiliza
cada vez más en todo el mundo como técnica de rescate en pacientes con PCR
refractario. Aunque faltan ensayos controlados aleatorios que demuestren la
eficacia en este escenario, los estudios observacionales han informado entre
20% y 40% de sobrevida. (5)
Actualmente no
disponemos de datos suficientes para identificar a aquellos que pueden
beneficiarse con RCPE. Se recomienda internacionalmente formular en cada centro
criterios de inclusión acordados para guiar a los médicos sobre cómo equilibrar
el uso inteligente de los recursos entre los pacientes que se cree que tienen
una mejor probabilidad de sobrevida después de un PCR. (2)
En nuestro centro a partir de la formación del equipo multidisciplinario “ECMO team”
se estandarizaron los criterios de inclusión (Tabla
1),
teniendo en cuenta que la toma de decisiones para RCPE a menudo es crítica en
cuanto al tiempo e influyen factores externos como horario y día de la semana.
Para ello es fundamental presentar una adecuada logística, con personal
capacitado para la canulación las 24 horas del día, los 7 días de la semana (ya
que se recomienda que la ECMO esté funcionando a los 60 minutos del inicio del
PCR), para el armado y purgado del equipo rápidamente en la emergencia, y
personal de salud que pueda detectar dentro de los 10 minutos del PCR los
posibles candidatos a RCPE.
Los protocolos y
algoritmos se esfuerzan por identificar rápidamente los casos con mayor
probabilidad de sobrevivir con un resultado neurológico favorable, como
aquellos pacientes con PCR presenciado y en quienes se inició rápidamente una
RCP de alta calidad, además de los paros cardíacos con una patología
presuntamente reversible, como las obstrucciones coronarias agudas. (2) Otros factores que
también pueden influir para indicar la RCPE suelen ser la edad, la causa del
PCR, el tiempo, las comorbilidades y el ritmo cardíaco al inicio del PCR. (3) Recientemente se publicó
el puntaje de riesgo de predicción de sobrevida llamado RESCUE-IHCA, derivado
de 1075 pacientes. El 28% sobrevivió al alta, y se identificaron 6 variables
que se asociaron con la muerte hospitalaria: edad, hora del día, ritmo inicial,
antecedentes de insuficiencia renal, tipo de paciente (cardíaco vs no cardíaco
y médico vs quirúrgico) y duración del paro cardíaco. (5)
La mayor probabilidad de éxito suele darse en el paciente joven (en algunos
grupos de trabajo se considera hasta 50 años para realizar RCPE), con pocas
comorbilidades, con un PCR presenciado, preferentemente durante el día (cuando
es más sencilla la logística, y hay mayor accesibilidad al personal
capacitado), con maniobras de RCP adecuadas y de manera inmediata (preferentemente
en unidades de cuidados críticos), y causa cardíaca, con un ritmo inicial
desfibrilable.
Nuestros resultados
son comparables a los reportados por el registro internacional multicéntrico de
la ELSO (Extracorporeal Life Support Organization), en el que la sobrevida
en ECMO fue de 41% y al alta sanatorial de 30% a nivel internacional, (6) y a los resultados del
estudio RESCUE-IHCA. (5)
La ECMO VA como
tratamiento del PCRIH en nuestro centro presentó una sobrevida aceptable al
alta hospitalaria. La ECMO VA puede ser un tratamiento efectivo en pacientes
altamente seleccionados cuando las terapias convencionales fallan, siendo útil
y aplicable en un país de bajos y medianos ingresos con acceso limitado a los
dispositivos de asistencia circulatoria. Probablemente estos resultados no
puedan ser extrapolados a otros centros de la región, ya que nuestra
institución es un centro monovalente de alta complejidad cardiovascular,
referente en ECMO VA, con un programa de asistencia desarrollado, más de 7 años
de experiencia, y actualmente con más de 15 implantes por año. Si bien el
número de pacientes incluidos en esta serie es reducido, no deja de ser
novedoso, ya que sería la primera experiencia publicada que analiza los resultados
de la ECMO VA en PCRIH refractario en nuestro país.
Declaración
de conflicto de intereses
Los autores
declaran que no tienen conflicto de intereses
(Véanse
formularios de conflicto de intereses de los autores en la web/Material
suplementario).
Consideraciones
éticas
El estudio fue
conducido según las normas de investigación
(Declaración de
Helsinki) y ha sido aprobado por el Comité de Ética institucional.
Lucrecia María
Burgos1, Ana
Spaccavento, Leonardo Seoane1, Juan
Francisco Furmento1, Mariano
Vrancic1, Mirta
Diez1,
1 Instituto
Cardiovascular de Buenos Aires. Ciudad de Buenos Aires. Argentina.
E-mail: insuficienciacardiaca@icba.com.ar
1. Jacobs I, Nadkarni V, Bahr J, Berg RA, Billi JE,
Bossaert L, et al; International Liaison Committee on Resuscitation; American
Heart Association; European Resuscitation Council; Australian Resuscitation
Council; New Zealand Resuscitation Council; Heart and Stroke Foundation of
Canada; InterAmerican Heart Foundation; Resuscitation Councils of Southern
Africa; ILCOR Task Force on Cardiac Arrest and Cardiopulmonary Resuscitation
Outcomes: Cardiac arrest and cardiopulmonary resuscitation outcome reports:
Update and simplification of the Utstein templates for resuscitation
registries: A statement for healthcare professionals from a task force of the
International Liaison Committee on Resuscitation (American Heart Association,
European Resuscitation Council, Australian Resuscitation Council, New Zealand
Resuscitation Council, Heart and Stroke Foundation of Canada, InterAmerican
Heart Foundation, Resuscitation Councils of Southern Africa). Circulation
2004;110:3385-97. http://doi.org/10.1016/j.resuscitation.2004.09.008
2. Keebler ME, Haddad EV, Choi CW, McGrane S,
Zalawadiya S, Schlendorf KH, et al. Venoarterial Extracorporeal Membrane Oxygenation
in Cardiogenic Shock. JACC Heart Fail 2018;6:503-16. http://doi.org/10.1016/j.jchf.2017.11.017
3. Richardson ASC, Tonna JE, Nanjayya V, Nixon P,
Abrams DC, Raman L, et al. Extracorporeal Cardiopulmonary Resuscitation in
Adults. Interim Guideline Consensus Statement From the Extracorporeal Life
Support Organization. ASAIO J 2021;67:221-8. http://doi.org/10.1097/MAT.0000000000001344
4. Klee TE, Kern KB. A review of ECMO for cardiac
arrest. Resusc Plus 2021;5:100083.
5. Tonna JE, Selzman CH, Girotra S, Presson AP,
Thiagarajan RR, Becker LB, et al; American Heart Association Get With the Guidelines–Resuscitation
Investigators. Resuscitation Using ECPR During In-Hospital Cardiac Arrest
(RESCUE-IHCA) Mortality Prediction Score and External Validation. JACC
Cardiovasc Interv 2022;15:237- 47. http://doi.org/10.1016/j.jcin.2021.09.032
6. Registro ELSO. Extracorporeal Life Support
Organization. Revisado 17/2/2022. Extracorporeal Life Support Registry Report.
Available online: https://www.elso.org/Registry/Statistics/InternationalSummary.aspx.
http://dx.doi.org/10.7775/rac.es.v91.i3.20637
Accidente cerebrovascular posterior
embólico secundario a trombosis arterial subclavia
El accidente
cerebrovascular (ACV) posterior acompañado de isquemia arterial de miembro
superior es una asociación infrecuente como forma de presentación clínica. Sus
causas pueden ser embolia, disección aortica, trauma vascular, el síndrome de
opérculo torácico, trastornos de la coagulación y, menos común, la trombosis
arterial subclavia.
Se presenta un
varón de 59 años, extabaquista (40 pack/year), hipertenso y
dislipidémico, que presentó un trastorno de la marcha de 2 semanas de evolución
y relató un registro de hipotensión arterial en el miembro superior izquierdo.
En consulta con su médico laboral se constató afasia de expresión, hemianopsia
temporal derecha e inestabilidad de la marcha, y se decidió su internación. En
el electrocardiograma se constató ritmo sinusal; en el ecocardiograma, función
sistólica ventricular izquierda conservada, sin shunt intracavitario ni
trombos intraluminales. En el eco Doppler de vasos de cuello: ateromas
subintimales carotídeos sin hallazgos hemodinámicamente significativos, con
flujo de muy baja velocidad en la arteria vertebral izquierda. La tomografía
axial computada (TAC) de cerebro reveló áreas hipodensas en la sustancia blanca
bifrontoparietales. La angioresonancia magnética nuclear de cerebro evidenció
una lesión isquémica aguda temporo-occipital izquierda en territorio de la
arteria cerebral posterior izquierda, con ausencia de flujo en el segmento
intracraneal de la arterial vertebral. (Figura
1)
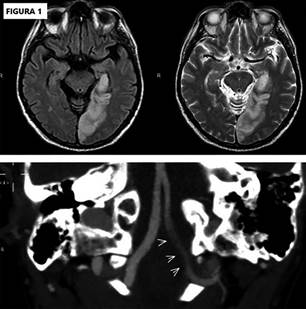
RMN:
resonancia magnética nuclear
Fig. 1.
RMN de cerebro con angiorresonancia: lesión isquémica aguda temporo-occipital
izquierda con ausencia de flujo en el segmento intracraneal de la arteria
vertebral
Al segundo día el
paciente refirió parestesias en el miembro superior izquierdo, se detectó
disminución de la temperatura con ausencia de pulsos humeral, radial y cubital.
El eco Doppler arterial
del miembro superior izquierdo mostró flujo monofásico de muy baja velocidad y
resistencia en las arterias humeral, radial y cubital, con trombosis arterial
subclavia. Se descartó disección aortica y síndrome de opérculo torácico por
angiotomografía de vasos de cuello y cayado aórtico, que mostró trombosis
completa arterial subclavia izquierda desde su origen, con parte del trombo
intraaórtico, y alteración de la tinción de la arteria vertebral homolateral en
segmento intraóseo e intracraneal (Figura
2A).
En la TAC de tórax, abdomen y pelvis: enfisema pulmonar bilateral. En el
laboratorio: plaquetas 373.000 mil/mm3, dímero D y anticuerpos
antifosfolípidos IgG e IgM normal, Inhibidor Lúpico negativo, homocisteína
normal, anticuerpos anti Beta 2 Glicoproteína IgG e IgM negativo. Proteína C:
108%, Proteína S libre: 66%. En el electrocardiograma Holter de 24hs: ritmo
sinusal predominante, sin extrasístoles ventriculares ni supraventriculares. Al
4to día la
resonancia magnética nuclear (RMN) de cerebro de control no evidenció
trasformación hemorrágica de la lesión temporo-occipital.
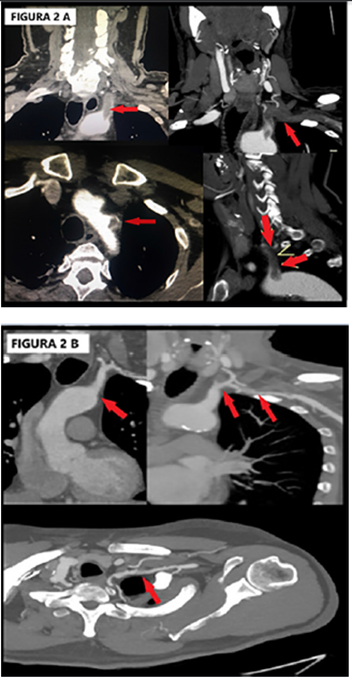
Fig. 2.
A. Angiotomografía de vasos de cuello y cayado aórtico: trombosis completa
arterial subclavia izquierda desde su origen, con parte del trombo
intraaórtico. B. Angiotomografía de control a los 3 años: recanalización
parcial de la trombosis subclavia, con desaparición total del trombo
intraaórtico en el ostium subclavio
Por la trombosis
completa arterial subclavia izquierda con extensión intraaórtica asociada a
accidente cerebrovascular posterior isquémico, se descartó el tratamiento
endovascular o quirúrgico por el alto riesgo de complicaciones embolicas
sistémicas y se decidió anticoagulación con heparina sódica por bomba de
infusión continua, bajo estricto control neurológico y posterior rotación a
acenocumarol vía oral. Al día 10 se fue de alta sin complicaciones
neurológicas, ni isquémicas en el miembro superior. Al año se suspendió la
anticoagulación debido a hematuria y hematemesis reiteradas, y continuó con
clopidogrel y cilostazol vía oral. El último control a los 3 años por
angiotomografía evidenció recanalización parcial de la trombosis subclavia, con
desaparición total del trombo intraaórtico en el ostium subclavio. (Figura
2B)
El paciente se
encuentra asintomático, con recuperación de pulso humeral; se repitieron
estudios de trombofilia que fueron negativos.
El 20-25% de los
ACV ocurren en el sistema de circulación posterior (arteria cerebral posterior,
basilar y vertebral) y pueden comprometer el tronco encefálico, cerebelo,
tálamo y/o la región temporo-occipital. Caplan et. al describieron la embolia
como el mecanismo más frecuente de ACV posterior (40-54%), principalmente de
origen cardíaco (24% de los casos), mientras que la embolia arterio-arterial
solo se informó en el 14%. (1)
Otros mecanismos son las lesiones ateroscleróticas de las grandes arterias,
oclusión de vasos pequeños, y causas raras como trastornos de la coagulación o
ateroembolia carotídea asociada al origen fetal de la arteria cerebral
posterior. Debido a la amplia área cerebral irrigada por el sistema arterial
vertebro-basilar, los accidentes isquémicos en este territorio dan variados
signos y síntomas. Los signos más frecuentes son ataxia de la marcha, debilidad
unilateral de una extremidad, disartria, nistagmo y defectos en el campo
visual, mientras que los síntomas referidos suelen ser vértigo, mareos, náuseas
y vómitos, dolor de cabeza y alteración de la conciencia.
La trombosis de la
arteria subclavia ocurre debido a daño en la íntima de la pared del vaso; la
aterosclerosis es la etiología más frecuente, y se localiza más en las áreas
carótido-subclavia derecha y subclavio-vertebral izquierda, por lo que estas
regiones suelen estar involucradas en la trombosis oclusiva. Los factores de
riesgo para aterosclerosis subclavia son la hipertensión arterial, el
tabaquismo, la diabetes, la obesidad y la dislipidemia. (2)
La trombosis de la arteria subclavia se presenta en menos del 1% de la
población y en general es asintomática, por lo que es una patología
subdiagnosticada. La trombosis subclavia izquierda es cuatro veces más común
que la derecha. (2)
La aparición de
síntomas isquémicos por disminución del flujo arterial debido a la trombosis
arterial subclavia está condicionada a la presencia o no de circulación
colateral, y las manifestaciones clínicas más frecuentes incluyen la
claudicación intermitente y parestesias en el miembro superior. Las
complicaciones de la trombosis arterial subclavia son la gangrena isquémica del
miembro superior, principalmente digital, la isquemia arterial aguda del
miembro y rara vez el ACV isquémico posterior. La patogenia de estos infartos
en territorio vertebro-basilar se debería a una embolia arterio-arterial o a la
propagación “retrograda” a la arteria vertebral a partir de una trombosis
arterial subclavia homolateral. (3,4)
Otras causas
descriptas de trombosis arterial subclavia asociadas a ACV posterior son los
estados de hipercoagulabilidad (déficit de Proteína S, trombocitemia esencial,
etc.), la disección aórtica, el trauma arterial, la embolia cardiaca y el
síndrome de opérculo torácico con compromiso arterial (SOT arterial), que se
caracteriza por una enfermedad de la arteria subclavia debida a compresión por
anomalías óseas como una costilla cervical, con lesión de la íntima con o sin
dilatación post-estenótica y formación de trombos propensos a embolización
distal, que genera complicaciones graves como la isquemia arterial de la
extremidad superior y más infrecuentemente un ACV posterior isquémico. (3-6)
Castillo Costa y
col. reportaron un caso de ACV posterior con isquemia de miembro superior por
trombosis de la aorta estructuralmente sana con embolia sistémica. (7)
La angiotomografía
del cayado de la aorta y el miembro superior comprometido permite confirmar el
diagnóstico de trombosis arterial subclavia como posible fuente embolígena en
pacientes con ACV posterior, así como identificar algunas de sus causas
(aterosclerótica, SOT arterial, disección, traumática, etc.)
El tratamiento de
la trombosis arterial subclavia en pacientes complicados con un ACV posterior
dependerá del grado de isquemia del miembro superior y de la patología vascular
que la originó. En líneas generales, las intervenciones terapéuticas endovasculares
o quirúrgicas (embolectomía o el tratamiento descompresivo con
revascularización en el SOT arterial) solo están indicadas en pacientes que
presentan su miembro superior amenazado, debido al riesgo de embolización
sistémica que existe durante la intervención. (3-4)
El tratamiento anticoagulante mediante infusión endovenosa inicial de heparina
sódica y posterior anticoagulación oral es una terapéutica efectiva descripta
para pacientes con trombosis arterial subclavia y ACV posterior que cursa con
una isquemia del miembro superior compensada para evitar la progresión de la
trombosis arterial y su cuadro clínico. (2,5,6)
En resumen, el ACV
isquémico posterior es una complicación infrecuente de la trombosis arterial
subclavia, que debe sospecharse en pacientes con infartos del territorio
vertebro-basilar y ausencia de pulso arterial en el miembro superior
homolateral. Su diagnóstico puede confirmarse por angiotomografía.
Declaración
de conflicto de intereses
Los autores
declaran que no tienen conflicto de intereses
(Véanse
formularios de conflicto de intereses de los autores en la web/Material
suplementario).
Consideraciones
éticas
No aplica
Robertino Bevacqua1, Pablo
Cassaglia2, Jorge
Leandro Fuentes3, Ramiro
Malagrini2, Alicia
Victoria Chavarri4, Mariano
Norese1
1
Servicio
de Cirugía Vascular. Clínica Bazterrica
2
Servicio
de Diagnóstico por imágenes, Diagnóstico Maipú DASA.
3
Servicio
de Clínica Médica. Clínica Bazterrica
4
Servicio
de Hematología. Clínica Bazterrica
Institución:
Clínica Bazterrica - C.A.B.A
Dirección
para separatas: e-mail: marianonorese@hotmail.com
1. Caplan L, Chung CS, Wityk R, Glass T, Tapia J,
Pazdera L, et al. New England medical center posterior circulation stroke
registry: I. Methods, data base, distribution of brain lesions, stroke
mechanisms, and outcomes. J Clin Neurol 2005;1:14-30. https://doi.org/10.3988/jcn.2005.1.1.14
2. Hassan SA, Akhtar A, Falah NU, Khan M, Zahra U. A
Case of Subclavian Artery Thrombosis. Cureus 2020;12:e6842. https://doi.org/10.7759/cureus.6842
3. Vemuri C, McLaughlin LN, Abuirqeba AA, Thompson RW.
Clinical presentation and management of arterial thoracic outlet syndrome. J
Vasc Surg 2017;65:1429-9. https://doi.org/10.1016/j.jvs.2016.11.039
4. Baek JH, Shin DH, Kang CK, Lee YB. Distal
subclavian artery occlusion causing multiple cerebral infarcts consequence of
retrograde flow of a thrombus? J Cerebrovasc Endovasc Neurosurg 2013; 15:221-4.
https://doi.org/10.7461/jcen.2013.15.3.221
5. Kumar KR, Kiley M. Essential thrombocythaemia
presenting with subclavian artery thrombosis and multiple embolic events. BMJ
Case Rep. 2009;2009:bcr11.2008.1240. https://doi.org/10.1136/bcr.11.2008.1240
6. Chavali S, Shukla U, Chauta S. Traumatic subclavian
arterial thrombosis presenting with cerebral infarct--a case report. Heart,
Lung & Circulation. 2014;23:e202-6. https://doi.org/10.1016/j.hlc.2014.04.254
7. Castillo Costa
Y, Delfino F, Mauro V, Barsotti A, Saltos F, Barrero C. Trombosis de aorta
estructuralmente sana con embolia sistémica. Rev Argent Cardiol 2016;86:446-7. http://dx.doi.org/10.7775/rac.es.v86. i6.14074
http://dx.doi.org/10.7775/rac.es.v91.i3.20639
Endocarditis infecciosa de implante
valvular pulmonar. Resolución quirúrgica con homoinjerto
Se presenta a una
paciente de 20 años que consulta por un síndrome febril de 7 días de evolución,
con astenia y adinamia. Como antecedente relevante la paciente presenta al
nacimiento estenosis valvular pulmonar y displasia de la válvula aortica como
parte de la sospecha clínica de síndrome de Noonan. A lo largo de su
crecimiento la paciente debió ser sometida a varias intervenciones quirúrgicas;
al año de vida se le realizó ampliación del tracto de salida de la arteria
pulmonar y plástica de válvula aortica; a los trece años necesitó un reemplazo
de la válvula aortica por prótesis mecánica bidisco tipo ATS número 18, con
ampliación del anillo y reemplazo de la válvula pulmonar por prótesis biológica
tipo Freestyle numero 19; y a los 17 años, dado el aumento marcado de los
gradientes a través del injerto pulmonar, se colocó una válvula vía percutánea
tipo Melody número 20. Cabe aclarar que a pesar de las múltiples intervenciones
la paciente se desarrolló física, social e intelectualmente en forma normal.
Dados los
antecedentes cardiológicos relevantes se decidió la internación de la paciente
para clarificar y lograr identificar el foco que originaba la fiebre. Como
datos positivos se identificó en hemocultivos seriados al bacilo gran negativo
Cardiobacterium del grupo HACEK; el eco Doppler color transesofágico evidenció
un aumento marcado de los gradientes de la válvula pulmonar tipo Melody, con
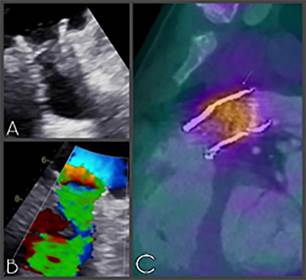
estructuras móviles compatibles con vegetaciones (Figura
1, A y B) y en el estudio de tomografía por emisión de
positrones (PET/ TC) se vio un claro aumento de la captación de la región
valvular pulmonar (Figura 1, C).
Fig. 1.
estudios preoperatorios. A, B: Ecocardiograma de válvula pulmonar. C: PET/TC
con captación protésica.
Con el diagnóstico
clínico y por estudios complementarios se interpretó el cuadro febril como una
endocarditis de la endoprótesis pulmonar, motivo por el cual se realizó una
nueva cirugía para reemplazar la prótesis claramente infectada y el tracto de
salida de la arteria pulmonar con un homoinjerto número 21. Se observo
indemnidad de la válvula protésica aórtica, por lo que no se requirió reemplazo
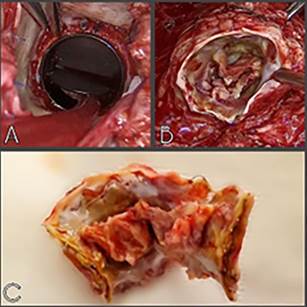
de esta (Figura 2, A, B y C).
Fig. 2.
imágenes intraoperatorias A: válvula aórtica indemne. B/C: prótesis en posición
pulmonar con claros signos de endocarditis.
La evolución del
postoperatorio fue satisfactoria y la antibioticoterapia incluyó, dada la
sensibilidad del germen Cardiobacterium, ceftriaxona y gentamicina. Al año del
seguimiento la paciente realiza una vida normal, hemodinámicamente estable y
libre de infección cardiaca con un normal funcionamiento del homoinjerto
colocado en posición pulmonar.
El riesgo de
endocarditis infecciosa (EI) tras el implante de una válvula percutánea
(Melody) en posición pulmonar (IVMP) es significativo, al menos durante los
primeros 3 años después del implante. Sin embargo, la incidencia reportada
varía considerablemente entre los diferentes estudios.
En un metaanálisis
que incluyo a 851 pacientes la incidencia acumulada de EI sobre IVMP osciló
entre el 3,2% y el 25%, con una tasa de incidencia anualizada que osciló entre
1,3 y 9,1% paciente-año. La mediana (rango intercuartílico) del tiempo desde la
EI del IVMP hasta el inicio de la EI fue de 18 meses (9-30,4), con un rango
entre 1 y 72 meses. La incidencia de EI ocurrió en el 32% de los casos en el
primer año, 27% en el segundo año, 18% luego en el tercer año y 23% más allá de
los 3 años del IVPM. (1)
En un estudio
realizado por McElhinney y col. en 309 pacientes con un seguimiento cercano a 5
años, encontraron por análisis multivariado como predictores de EI la edad
menor a 12 años en el momento del IVMP (OR 2,8; IC 95% 1,3-5,7; p = 0,006) y un
gradiente máximo inmediatamente posterior al implante mayor que 15 mm Hg (OR
2,6; IC 95% 1,3–5,2; p = 0,008). (2)
El diagnóstico de
este tipo de EI es un desafío, especialmente en términos de documentación del
proceso infeccioso de la prótesis valvular. Los criterios clásicos de Duke
modificados, que se basan en signos ecocardiográficos, muestran que el
diagnóstico de EI luego de IVMP no es tan sencillo. Es bien sabido que la
ecocardiografía, especialmente ecocardiografía transtorácica (ETT), sólo ofrece
una modesta sensibilidad (30%) para la detección de vegetaciones en la válvula
pulmonar, probablemente debido a la posición anterior del tracto de salida del
ventrículo derecho y los artefactos de la válvula protésica (stent,
degeneración valvular, calcificación del conducto, etc.). En cuanto a la ecocardiografía
transesofágica (ETE), a diferencia de la alta sensibilidad de detección de EI
de las válvulas aórtica y mitral, no siempre tiene valor agregado respecto de
los resultados del ETT en la EI de válvula pulmonar protésica. En el caso
reportado creemos que el estudio PET/CT pudo identificar el proceso infeccioso
en la prótesis pulmonar y descarto la afección de la válvula aortica, dato
sumamente importante al programar la táctica quirúrgica.
La 18F-FDG PET/CT
combina una técnica con gran sensibilidad para detectar actividad
inflamatoria-infecciosa y gran resolución anatómica para valorar las lesiones
estructurales asociadas a la endocarditis. Con una sensibilidad diagnóstica
entre 91-97%, la PET/CT se ha convertido en una herramienta de diagnóstico útil
en la sospecha de endocarditis infecciosa de pacientes con válvulas protésicas
y/o dispositivos, convirtiéndose en un criterio mayor en el algoritmo
diagnóstico de las guías actuales. (3)
Los hallazgos
clínicos más comunes encontrados en la EI del IVMP fueron hemocultivos
positivos (93%), fiebre (89%) y aumento progresivo del gradiente transvalvular
pulmonar (79%); en cuanto a la detección de vegetaciones por ETT se dio solo en
el 34% de los casos. Estos datos reportados por la bibliografía fueron los que
presentó nuestra paciente, siendo el ETT muy débil para definir el origen del
cuadro infeccioso.
En el metaanálisis
citado, de 69 pacientes que desarrollaron EI después del IVMP, 6 (8,7%)
fallecieron y 35 (52%) se sometieron a una reintervención quirúrgica y/o
transcatéter. (1)
Los gérmenes más
comunes que se han detectado en los hemocultivos de los pacientes con EI post
IVMP son: Estafilococo 42 %, Estreptococo 30,4%, Corynebacterium 5,8%, grupo
HACEK 4,3%, Haemophilus 2,9%; y se han detectado hemocultivos negativos en poco
más del 7% de los pacientes. (1, 4)
Dentro del grupo HACEK se encuentra el Cardiobacterium hominis (germen
responsable de nuestro caso), que tiene como hábitat natural la orofaringe y
produce EI en forma subaguda.
La vía de entrada
microbiana está relacionada en la mayoría de los casos a procesos bucodentales.
Sin embargo, hay reportes en pacientes con antecedentes de gastroenteritis,
cistitis, neumonía, procesos dérmicos y ungueales, como así también en tatuajes
de piel. (5)
La incidencia de
EI después de la implantación de una válvula percutánea en posición pulmonar es
muy variable según reportado en los estudios, y se presenta principalmente
durante los primeros 3 años después del procedimiento, y mayormente en presencia
de gradientes aumentados transpulmonares. Los antecedentes cardiológicos deben
hacer pensar en la EI ante un cuadro febril de origen desconocido. Los estudios
multi imágenes, incluida la PET/TC, han sido de suma utilidad para identificar
el foco de infección secundario a EI por Cardiobacterium en nuestra paciente.
Creemos que la resolución satisfactoria del caso se debe a la interacción de
los integrantes del servicio de cardiología y cirugía en patologías congénitas
del adulto dada la complejidad en la toma de decisiones y las intervenciones quirúrgicas
previas. El homoinjerto nos ha permitido resolver una situación quirúrgica
compleja.
Declaración
de conflicto de intereses
Los autores
declaran que no tienen conflicto de intereses
(Véanse
formularios de conflicto de intereses de los autores en la web/Material
suplementario).
Consideraciones
éticas
No aplica
Guillermo
Gutiérrez, Manuel Clusa, Mariana López Daneri, Sergio BarattaMTSAC, Eduardo Martino, Jorge
BilbaoMTSAC,
Guillermo VaccarinoMTSAC,
Hospital Universitario Austral
1. Abdelghani M, Nassif M, Blom N, Van Mourik M,
Straver B, Koolbergen D, et al. Infective Endocarditis After Melody Valve
Implantation in the Pulmonary Position: A Systematic Review. J Am Heart Assoc.
2018;7:e008163. https://doi.org/10.1161/JAHA.117.008163
2. McElhinney DB, Sondergaard L, Armstrong AK,
Bergersen L, Padera R, Balzer DT et al. Endocarditis After Transcatheter Pulmonary
Valve Replacement. J Am Coll Cardiol 2018;72:2717–28. https://doi.org/10.1016/j.jacc.2018.09.039
3. Swart L, Gomes A, Scholtens A, Sinha B, Tanis W,
Marnix Lam M, et al. Improving the Diagnostic Performance of 18F-FDG PET/CT in
Prosthetic Heart Valve Endocarditis. Circulation, 2018;138:1412-17. https://doi.org/10.1161/CIRCULATIONAHA.118.035032
4. Avellana P, Garcia Aurelio M, Swieszkowski S,
Nacinovich F, Kazelian L, Spennato M, et al. REPRESENTACIÓN DE
LOS INVESTIGADORES DEL ESTUDIO EIRA-3. Endocarditis infecciosa en la República
Argentina. Resultados del estudio EIRA 3. Rev Argent Cardiol 2018;86:20-8. http://dx.doi.org/10.7775/rac.es.v86.i1.10935.
5. Malani A, Aronoff D, Bradley S, Kauffman A.
Cardiobacterium hominis endocarditis: Two cases and a review of the literature.
European journal of clinical microbiology & infectious diseases: official
publication of the European Society of Clinical Microbiology 2006;25:587-95 http://dx.doi.org/10.1007/s10096-006-0189-9.
![]() https://creativecommons.org/licenses/by-nc-sa/4.0/
https://creativecommons.org/licenses/by-nc-sa/4.0/
©Revista Argentina
de Cardiología