ARTÍCULO
DE REVISIÓN
Manejo del aneurisma de aorta abdominal sintomático no
roto: últimos adelantos
Management of
symptomatic unruptured abdominal aortic aneurysms:
state of the art
Fernando D. Garagoli1, María L. Fernández Recalde1, Andrés M. Izaguirre1
1 Departamento de Cardiología, Hospital Italiano de Buenos Aires,
Buenos Aires, Argentina
Dirección para correspondencia: Dr.
Fernando Garagoli - E-mail: fernando.garagoli@hospitalitaliano.org.ar - Perón 4190, Buenos Aires, Argentina - Teléfono: +541149590200
(5303) - Código postal: C1199ABB
Rev
Argent Cardiol 2023;91:225-230.
http://dx.doi.org/10.7775/rac.es.v91.i3.20636
RESUMEN
El aneurisma de aorta abdominal (AAA) sintomático no roto es una
patología que involucra a aquellos pacientes con AAA intacto, pero que
presentan dolor abdominal y/o lumbar atribuido al aneurisma. Esta forma de
presentación clínica es potencialmente mortal dado que su etiopatogenia
comprende cambios agudos en la pared aórtica, incluyendo inflamación, lo que
incrementa la probabilidad de ruptura inminente. Está claro que estos pacientes
deben ser derivados a reparación del AAA. Sin embargo, el momento de la intervención
es controvertido. Por lo tanto, el objetivo del presente trabajo fue revisar la
información actualizada sobre el abordaje diagnóstico-terapéutico del AAA
sintomático no roto.
Palabras clave: Aneurisma de aorta abdominal sintomático no roto - Inflamación -
Cirugía abierta - Reparación endovascular del
aneurisma
ABSTRACT
Symptomatic unruptured
abdominal aortic aneurysm (AAA) refers to a group of patients with intact AAA
but who present abdominal and/or lumbar pain attributed to the aneurysm. This
form of clinical presentation is potentially fatal since its etiopathogenesis, involving acute changes in the aortic
wall, including inflammation, increases the probability of impending rupture.
It is clear that these patients should be referred to AAA repair. However, the
timing of the intervention is controversial. Therefore, the aim of the present
work was to review updated information on the diagnostic-therapeutic approach
of symptomatic unruptured AAA.
Key words:
Symptomatic unruptured abdominal aortic aneurysm -
Inflammation - Open surgery - Endovascular aneurysm repair
Recibido: 19/03/2023
Aceptado: 29/05/2023
INTRODUCCIÓN
La etimología de la palabra aneurisma puede rastrearse en el
lenguaje de la antigua Grecia, (1,2) y deriva de la palabra aνευρυσμa
(aneurysma) que significa dilatación. (2)
Por lo tanto, “aneurisma aórtico” se refiere a una dilatación
anormal de la aorta que compromete uno o más segmentos de su pared. En este
sentido, un incremento del diámetro aórtico mayor que el 50% a nivel del
diafragma se considera anormal. Sin embargo, esta definición no es siempre
aplicable, ya que a menudo el límite entre la aorta sana y patológica no es
preciso. (3,4) En consecuencia, existe un consenso general en considerar que el
aneurisma de aorta abdominal (AAA) sea una dilatación de la aorta igual o mayor
a 30 mm. (4-7) Se han llevado a cabo numerosos estudios para evaluar los
resultados de la reparación electiva de los AAA, así como los de la cirugía de
emergencia en el caso de los aneurismas rotos. (8-15) No obstante, existe un tipo de presentación clínica de AAA
potencialmente mortal y escasamente estudiado: el AAA sintomático no roto. (16) Por este
motivo, el propósito del presente estudio fue revisar información actualizada
sobre el abordaje diagnóstico-terapéutico del AAA sintomático no roto.
MATERIAL Y MÉTODOS
Se llevaron a cabo búsquedas para identificar estudios clínicos
que evaluaran el abordaje diagnóstico-terapéutico del AAA sintomático no roto.
Las búsquedas se realizaron en las bases de datos electrónicas de
PUBMED/Medline, EMBASE y Cochrane Clinical
Trials utilizando los términos: “aneurisma de aorta
abdominal”, “aneurisma sintomático”, “aneurisma no roto”, “cirugía abierta” y
“reparación endovascular de aneurisma”.
La selección de artículos se efectuó de acuerdo con los siguientes
criterios: a) publicaciones desde 1990 hasta el presente; b) estudios
observacionales, ensayos clínicos, revisiones sistemáticas y recomendaciones de
sociedades científicas; c) estudios en seres humanos; y d) artículos referidos
al manejo del AAA sintomático no roto. Se excluyeron los estudios en los cuales
no estuviera accesible el texto completo.
El objetivo primario de este estudio fue: a) sintetizar el
conocimiento acerca de la epidemiología y el abordaje diagnóstico-terapéutico
del AAA sintomático no roto; y b) desarrollar un algoritmo para su manejo
diagnóstico-terapéutico.
Definición y
epidemiología
El AAA sintomático no roto se refiere a un grupo de pacientes con
AAA intacto, pero con dolor abdominal y/o lumbar atribuido al aneurisma. Otro
síntoma incluye sensibilidad a la palpación en el abdomen, espalda o flanco en
el lugar donde está ubicado el AAA. (17) La presencia de dolor se debe a múltiples causas, que incluyen
cambios agudos en la pared aórtica, como describiremos más adelante. En los
aneurismas grandes, el dolor puede ser causado por compresión de estructuras
adyacentes. Los pacientes con AAA sintomático no roto generalmente no tienen
hipotensión arterial porque la pared aórtica está indemne, sin evidencia de
hemorragia retroperitoneal. (7) La incidencia de este tipo de presentación clínica oscila entre
el 3% y 15%. (18,19)
Fisiopatología
La fisiopatología del AAA sintomático no roto involucra cambios
agudos en la pared aneurismática, que incluyen incremento del stress parietal y
extensión del trombo intraluminal o nuevo sangrado,
que aumentan la probabilidad de ruptura inminente. (20) Existe evidencia que demuestra el rol de la inflamación de la
pared aneurismática en la etiopatogenia de este tipo de presentación clínica.
Asimismo, el metabolismo aumentado de la fluorodesoxiglucosa
en tomografía computada por emisión de positrones (PET/TC) en pacientes con AAA
sintomático no roto en comparación con pacientes asintomáticos se ha
correlacionado con aumento de la densidad de infiltrado inflamatorio en
biopsias de la pared aneurismática. (21)
Pronóstico y resultados de la
reparación
La tasa actual de mortalidad perioperatoria
en pacientes con AAA sintomático no roto es menor que la comunicada previamente
en la literatura. Así, De Martino y col. demostraron
una mortalidad hospitalaria del 1,7% (2,2% en pacientes operados y 0% en los
que fueron sometidos a reparación endovascular). (22) De manera
similar, Chandra y col. publicaron una mortalidad perioperatoria global contemporánea (2005-2014) del 5,9%,
siendo 8% en pacientes quirúrgicos y 5% en los que fueron tratados en forma endovascular. (17) Con respecto a las complicaciones postoperatorias y la
supervivencia a largo plazo, De Martino y col. reportaron
que la tasa de complicaciones postoperatorias, incluyendo insuficiencia renal,
infarto agudo de miocardio, arritmias e insuficiencia respiratoria, fue de 35%
en pacientes con AAA sintomático no roto versus 20% y 63% en aquellos con AAA
asintomático y roto, respectivamente. La supervivencia a 1 y 4 años fue de 83%
y 68%, respectivamente, en pacientes con AAA sintomático no roto, mientras que
en asintomáticos fue de 89% y 73%, y en aquellos con AAA roto, de 49% y 35%,
respectivamente. (22) En conclusión, la mortalidad hospitalaria del AAA sintomático no
roto es similar o discretamente superior a la observada para una intervención
electiva. Sin embargo, las tasas de complicaciones postoperatorias y de
supervivencia a largo plazo son intermedias en comparación con la reparación de
AAA asintomáticos y rotos. (23-27)
Abordaje
diagnóstico-terapéutico
Ante la sospecha de un AAA sintomático, se debe colocar un catéter
venoso de gran calibre, realizar monitoreo invasivo de la presión, y llevar a
cabo la confirmación diagnóstica y el tratamiento inmediato en el centro de la
localidad donde reside el paciente. Si no existen las condiciones para realizar
el diagnóstico y tratamiento en el centro, se debe activar el traslado
inmediato a un hospital de alta complejidad. (7) La mayoría de los pacientes presentarán estabilidad hemodinámica
ya que, por definición, no hay ruptura de la pared aórtica. (17) Es necesario un alto grado de sospecha clínica dado el mal
pronóstico de AAA rotos y sintomáticos no rotos. En un metaanálisis
que incluyó estudios publicados después de 1990, se encontró un diagnóstico
erróneo de AAA roto en 32% de los casos. Los diagnósticos diferenciales
erróneos más comunes fueron cólico renal e infarto de miocardio. (28,29) La Figura
1 postula un algoritmo para el abordaje diagnóstico-terapéutico del
AAA sintomático. Todos los individuos admitidos a un centro de emergencias con
dolor abdominal y/o lumbar con diagnóstico de AAA y estabilidad desde un punto
de vista hemodinámico, deben ser sometidos rápidamente a una angiotomografía computarizada (ATC) de abdomen y pelvis. (5)
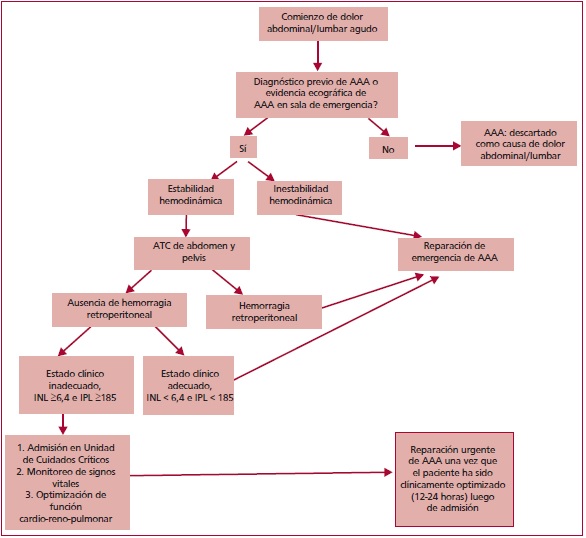
AAA: Aneurisma aórtico abdominal; ATC: Angiotomografía computarizada; INL: Índice
neutrófilo-linfocito; IPL: Índice plaqueta-linfocito.
Fig.
1.
Algoritmo para el abordaje diagnóstico-terapéutico del AAA sintomático.
Algoritmo de Sullivan modificado. (34)
Cuando existe disponibilidad, los clínicos pueden recurrir a la
ecografía doppler abdominal como ayuda para hacer el
diagnóstico. (30) Mientras que la ecografía doppler puede
identificar la presencia de AAA y fluido intraabdominal,
es menos efectiva para detectar signos de ruptura aórtica. (31) Por lo tanto, la ecografía doppler no
se considera un estudio confirmatorio de ruptura, aunque representa una herramienta
útil para identificar el AAA. Aquellos pacientes con sospecha clínica y
presencia de AAA en la ecografía doppler pueden ser
considerados de alto riesgo para AAA sintomático, permitiendo la derivación
urgente para una ATC. Por otra parte, en pacientes con riesgo bajo de AAA
sintomático, la ausencia de AAA en la ecocardiografía puede ser suficiente para
no realizar otros estudios, especialmente si existe otra causa más probable que
explique los síntomas. (32) Si se confirma AAA sintomático, una hemorragia retroperitoneal o
la ausencia de ruptura aórtica con dolor persistente, a pesar de tratamiento
médico óptimo, incluyendo analgesia y control de signos vitales, obliga a una
reparación de emergencia. Si, por el contrario, no se observan hallazgos tomográficos de ruptura aneurismática, el momento de la
intervención es controvertido y sigue siendo un desafío. (8) Numerosas series de casos retrospectivos han publicado tasas más
altas de morbilidad y mortalidad en la reparación de emergencia de AAA en comparación
con la intervención urgente (18-26% vs. 4-5%). (33-
35) Asimismo, no se han comunicado muertes
asociadas con ruptura de aneurisma en pacientes con AAA sintomático no roto, en
los cuales la intervención fue postergada y realizada semi
electivamente. (18) Con respecto a este aspecto, diversas series que han evaluado las
causas de muerte en este grupo de pacientes han demostrado que, en la mayoría
de los casos, estos son secundarios al infarto de miocardio, insuficiencia
respiratoria, insuficiencia renal, falla multiorgánica
y sepsis. (34, 36) En nuestra opinión, considerando que la morbilidad y mortalidad
de los pacientes con AAA sintomático no roto sometidos a cirugía de emergencia
están relacionadas a disfunción cardio-reno-pulmonar,
es razonable priorizar la optimización de estos sistemas antes de la reparación
del AAA. En este sentido, consideramos que estos objetivos podrían alcanzarse
en un lapso de 12-24 horas, siempre y cuando el centro cuente con los recursos
necesarios. Es esencial que el paciente sea admitido a una unidad de cuidados
críticos, con monitoreo adecuado de sus signos vitales. Desde un punto de vista
cardiovascular, hay evidencia de la utilidad de realizar ecocardiografía transtorácica focalizada (FoCUS)
para la evaluación de pacientes críticos, así como para su evaluación prequirúrgica. (37) Un ecocardiograma realizado en la sala de emergencias
proporcionará información esencial para el manejo hemodinámico,
incluyendo la fracción de eyección ventricular izquierda, presencia de
enfermedades valvulares significativas y el grado de precarga del paciente, a
través del patrón de llenado transmitral, la relación
E/E’, la presión sistólica pulmonar, y el diámetro y el colapso inspiratorio de
la vena cava inferior. (37)
Frecuentemente, los pacientes añosos presentan precarga reducida antes de la
cirugía con impacto negativo en el volumen minuto, lo que puede optimizarse con
una carga de volumen adecuado. Algunos casos pueden requerir un monitoreo más
invasivo con un catéter de Swan- Ganz,
lo que permite una orientación terapéutica en función del estado hemodinámico
del paciente. Además, alcanzar una precarga adecuada reducirá el riesgo de
insuficiencia renal postoperatoria. Desde la perspectiva respiratoria, la
enfermedad pulmonar obstructiva reversible puede mejorar por medio del
tratamiento breve con esteroides endovenosos y broncodilatadores en aerosol. (34)
Por
lo tanto, en este subgrupo de pacientes con AAA sintomático no roto es crucial
identificar a los individuos de alto riesgo preoperatorio que pueden
beneficiarse con la rápida optimización de su estado clínico (cardiológico,
pulmonar y/o renal) previo a una intervención urgente. (17,34)
Con el propósito de responder a este problema, se han desarrollado diversos
trabajos que evalúan la utilidad de puntajes y ciertos marcadores bioquímicos
para predecir la mortalidad hospitalaria en pacientes con AAA sintomático no
roto. Antonello y col. comunicaron que la Escala de
Glasgow en Aneurismas es un buen predictor de morbilidad y mortalidad perioperatoria luego de la cirugía abierta urgente del AAA
sintomático no roto. Los autores sugieren que los pacientes con puntaje <90
pueden ser sometidos de manera segura a una reparación abierta de emergencia. Los
pacientes con puntaje ≥90 deberían recibir una evaluación exhaustiva y
optimización del estado clínico preoperatorio. (38)
Por otra parte, considerando el rol de la inflamación en la etiopatogenia de
esta enfermedad, recientemente Garagoli y col.
evaluaron la utilidad de marcadores bioquímicos de inflamación para la
predicción de mortalidad hospitalaria en pacientes sometidos a reparación
quirúrgica y endovascular de AAA sintomático no roto.
Los autores concluyeron que los pacientes con índices neutrófilos-linfocitos
≥6,4 y plaquetas-linfocitos ≥185 son de alto riesgo y podrían
beneficiarse de una conducta de espera supervisada previo a la optimización del
estado clínico prequirúrgico o, aún considerar una
reparación endovascular. (36,39)
Estos biomarcadores están ampliamente disponibles,
son de bajo costo y, además, tienen la ventaja de representar el estado
inflamatorio del paciente en el momento de su admisión al hospital. Esto es
diferente de la Escala de Glasgow en Aneurismas, que usa variables clínicas
referidas a la historia clínica previa del paciente y considera al shock como
la única variable del estado clínico en el momento de la presentación, lo que
estimamos es insuficiente ya que, como mencionamos previamente, estos individuos
generalmente presentan estabilidad hemodinámica. (36,
39)
No
obstante, durante la evaluación preoperatoria, es fundamental que el médico
tratante esté alerta a signos y síntomas que indiquen una intervención de
emergencia obligatoria. El desarrollo de hipotensión, taquicardia, oliguria o
acidosis metabólica requiere una reparación inmediata. (7)
Decisión sobre el tipo de reparación
de AAA sintomático no roto: cirugía abierta versus procedimiento endovascular
Existen
evidencias que demuestran que el procedimiento endovascular
reduce la morbilidad y mortalidad luego de la reparación de AAA sintomático no
roto. En este sentido, este tipo de reparación ofrece algunas ventajas
potenciales en comparación con el tratamiento quirúrgico convencional en esta
condición clínica: menor agresión fisiológica al organismo, menor necesidad de
anestesia profunda, menos pérdida de sangre, minimiza la hipotermia y reduce el
tiempo de intervención. (7)
El análisis del Registro ENGAGE demostró la falta de diferencias entre la
reparación endovascular del AAA asintomático y el AAA
sintomático no roto. (19)
Una revisión sistemática identificó 23 estudios observacionales que evaluaron
7040 reparaciones de AAA sintomáticos no roto y roto (con procedimientos
quirúrgico y endovascular) y demostraron que los
pacientes sometidos a intervención endovascular
presentaban una menor tasa de mortalidad intrahospitalaria en comparación con
la cirugía abierta (odds ratio 0,624, IC 95%
0,518-0,752, p<0,0001), así como una menor estadía hospitalaria, menor
sangrado y reducción del tiempo de intervención. (40)
Sin
embargo, para realizar la reparación endovascular es
esencial cumplir con los criterios anatómicos requeridos además de contar con
un programa institucional para la intervención endovascular
de emergencia. En este contexto, el papel de la ATC es fundamental para definir
aquellos pacientes apropiados para reparación endovascular.
(5,8)
Asimismo, consideramos que el traslado a un centro vascular de alta complejidad
es conveniente en pacientes hemodinámicamente
estables y anatómicamente aptos para reparación endovascular,
especialmente si el riego quirúrgico es alto.
CONCLUSIONES
El
AAA sintomático no roto constituye una condición clínica de AAA potencialmente
mortal, con pronóstico intermedio entre pacientes asintomáticos y aquellos con
aneurismas rotos. Aunque el tiempo de intervención es todavía controversial,
consideramos que es fundamental estratificar el riesgo preoperatorio
individual, con la finalidad de identificar a los pacientes de alto riesgo que
se podrían beneficiar de la optimización de su estado clínico previo a la
intervención. La reparación endovascular es factible
en este escenario clínico, principalmente en pacientes con alto riesgo
quirúrgico, siempre y cuando se cumplan los criterios anatómicos necesarios y
la institución tenga un programa para la intervención endovascular
de emergencia.
Financiamiento
Esta
investigación no recibió ningún subsidio específico de agencias públicas,
comerciales o sin fines de lucro.
Declaración de conflicto de interese
Los
autores declaran que no tienen conflictos de intereses.
(Véase
formulario de conflictos de intereses de los autores en la web/Material
suplementario).
![]() https://creativecommons.org/licenses/by-nc-sa/4.0/
https://creativecommons.org/licenses/by-nc-sa/4.0/
©Revista Argentina de Cardiología
1. Antoniou GA, Antoniou AI, Antoniou SA, Lazarides MK. A historical perspective of medical terminology of aortic aneurysm. J Vasc Surg
[Internet]. 2011;54:1527-8. Available from: http://dx.doi.org/10.1016/j.jvs.2011.04.036
2. Real Academia Real Academia de la
Lengua Espanola, de la lengua Española Asociacion de Academias. Diccionario de la Lengua Espanola RAE [Internet]. Planeta Publishing; 2014. Available from: https://books.google.com/books/about/Diccionario_de_la_Lengua_Espanola_RAE.html?hl=&id=naqwoQEACAAJ
3. Doval HC,
Lucas LO. Aneurisma de aorta abdominal. En: Doval HC,
Tajer CD, editores. Evidencias en cardiología: De los
ensayos clínicos a las conductas terapéuticas. 8° edición. Ciudad Autónoma de Buenos
Aires: GEDIC; 2016. p. 1139-69.
4. Erbel R, Aboyans V, Boileau C, Bossone E, Bartolomeo RD, Eggebrecht H, et
al. 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases:
Document covering acute and chronic aortic diseases of the thoracic and
abdominal aorta of the adult. The Task Force for the
Diagnosis and Treatment of Aortic Diseases of the European Society of
Cardiology (ESC). Eur Heart J [Internet]. 2014;35:2873–926. Available from: http://dx.doi.org/10.1093/eurheartj/ehu281
5. Chaikof EL, Dalman RL, Eskandari MK, Jackson BM, Lee WA, Mansour MA, et al. The
Society for Vascular Surgery practice guidelines on the care of patients with
an abdominal aortic aneurysm. J Vasc Surg [Internet]. 2018;67:2–77.e2.
Available from: http://dx.doi.org/10.1016/j.jvs.2017.10.044
6. Writing
Committee Members, Isselbacher EM, Preventza O, Hamilton Black J Iii, Augoustides
JG, Beck AW, et al. 2022 ACC/AHA Guideline for the Diagnosis and Management of
Aortic Disease: A Report of the American Heart Association/American College of
Cardiology Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol [Internet].2022;80:e223-393. Available from: http://dx.doi.org/10.1016/j.jacc.2022.08.004
7. Bluro I.
Consenso de Enfermedad Vascular Periférica (versión resumida). Rev Argent Cardiol
[Internet].2015;83:461-86. Available from: http://ppct.caicyt.gov.ar/index.php/rac/article/view/6400/pdf_1
8. Wanhainen A, Verzini F, Van Herzeele I, Allaire E, Bown M, Cohnert T, et al.
Editor’s Choice - European Society for Vascular Surgery (ESVS) 2019 Clinical
Practice Guidelines on the Management of Abdominal Aorto-iliac
Artery Aneurysms. Eur J Vasc
Endovasc Surg [Internet].
2019;57:8-93. Available from: http://dx.doi.org/10.1016/j.ejvs.2018.09.020
9. Reimerink JJ, Hoornweg LL, Vahl AC, Wisselink W, van den Broek TAA, Legemate DA, et al. Endovascular repair versus open repair of ruptured
abdominal aortic aneurysms: a multicenter randomized controlled trial. Ann Surg [Internet]. 2013;258:248-56.
Available from: http://dx.doi.org/10.1097/SLA.0b013e31828d4b76
10. IMPROVE
Trial Investigators, Powell JT, Sweeting MJ, Thompson MM, Ashleigh R, Bell R,
et al. Endovascular or open repair strategy for ruptured abdominal aortic aneurysm:
30 day outcomes from IMPROVE randomised trial. BMJ
[Internet]. 2014;348:f7661. Available from: http://dx.doi.org/10.1136/bmj.f7661
11. Desgranges P, Kobeiter H, Katsahian S, Bouffi M, Gouny P, Favre JP, et al. Editor’s Choice - ECAR (Endovasculaire ou Chirurgie dans les Anévrysmes aorto-iliaques Rompus): A French Randomized Controlled Trial of
Endovascular Versus Open Surgical Repair of Ruptured Aorto-iliac
Aneurysms. Eur J Vasc Endovasc Surg [Internet]. 2015;50:303-10. Available from: http://dx.doi.org/10.1016/j.ejvs.2015.03.028
12. Greenhalgh RM, Brown LC, Kwong
GPS, Powell JT, Thompson SG, EVAR trial participants. Comparison of
endovascular aneurysm repair with open repair in patients with abdominal aortic
aneurysm (EVAR trial 1), 30-day operative mortality results: randomised controlled trial. Lancet
[Internet]. 2004;364:843-8. Available from: http://dx.doi.org/10.1016/S0140-6736(04)16979-1
13. United
Kingdom EVAR Trial Investigators, Greenhalgh RM,
Brown LC, Powell JT, Thompson SG, Epstein D. Endovascular repair of aortic
aneurysm in patients physically ineligible for open repair. N
Engl J Med [Internet]. 2010;362:1872-80.
Available from: http://dx.doi.org/10.1056/NEJMoa0911056
14. Blankensteijn JD, de Jong SECA, Prinssen
M, van der Ham AC, Buth J, van Sterkenburg
SMM, et al. Two-year outcomes after conventional or endovascular repair of
abdominal aortic aneurysms. N Engl
J Med [Internet]. 2005;352:2398-405. Available
from: http://dx.doi.org/10.1056/NEJMoa051255
15. Lederle FA, Freischlag JA, Kyriakides TC, Padberg FT Jr, Matsumura JS, Kohler TR, et al. Outcomes following
endovascular vs open repair of abdominal aortic
aneurysm: a randomized trial. JAMA [Internet]. 2009;302:1535-42.
Available from: http://dx.doi.org/10.1001/jama.2009.1426
16. Signs,
symptoms and risk factors predicting ruptured or symptomatic unruptured aneurysms before arrival at the hospital, and in
non-specialist hospital settings: Abdominal aortic aneurysm: diagnosis and
management: Evidence review N [Internet]. London: National Institute for Health
and Care Excellence (NICE); Available from: https://www.ncbi.nlm.nih.gov/pubmed/32407039
17. Chandra
V, Trang K, Virgin-Downey W, Tran K, Harris EJ, Dalman RL, et al. Management and outcomes of symptomatic
abdominal aortic aneurysms during the past 20 years. J Vasc
Surg [Internet]. 2017;66:1679-85.
Available from: http://dx.doi.org/10.1016/j.jvs.2017.04.033
18. Cambria
RA, Gloviczki P, Stanson
AW, Cherry KJ Jr, Hallett
JW Jr, Bower TC, et al.
Symptomatic, nonruptured abdominal aortic aneurysms:
are emergent operations necessary? Ann Vasc Surg [Internet]. 1994;8:121-6.
Available from: http://dx.doi.org/10.1007/BF02018859
19. Stokmans RA, Teijink JAW, Cuypers PWM, Riambau V, van Sambeek MRHM. No differences in perioperative outcome
between symptomatic and asymptomatic AAAs after EVAR: an analysis from the
ENGAGE Registry. Eur J Vasc
Endovasc Surg [Internet].
2012;43:667- 73. Available from: http://dx.doi.org/10.1016/j.ejvs.2012.02.034
20. Aggarwal S, Qamar A, Sharma V, Sharma
A. Abdominal aortic aneurysm: A comprehensive review. Exp Clin Cardiol [Internet]. 2011;16:11-
5. Available from: https://www.ncbi.nlm.nih.gov/pubmed/21523201
21. Reeps C, Essler M, Pelisek J, Seidl S, Eckstein HH,
Krause BJ. Increased 18F-fluorodeoxyglucose uptake in abdominal aortic aneurysms
in positron emission/computed tomography is associated with inflammation,
aortic wall instability, and acute symptoms. J Vasc Surg [Internet]. 2008;48:417-23;
discussion 424. Available from: http://dx.doi.org/10.1016/j.jvs.2008.03.059
22. De
Martino RR, Nolan BW, Goodney PP, Chang CK, Schanzer A, Cambria R, et al. Outcomes of symptomatic
abdominal aortic aneurysm repair. J Vasc Surg [Internet]. 2010;52:5–12.e1.
Available from: http://dx.doi.org/10.1016/j.jvs.2010.01.095
23. Stather PW, Sidloff D, Dattani N, Choke E, Bown MJ,
Sayers RD. Systematic review and meta-analysis of the early and late outcomes
of open and endovascular repair of abdominal aortic aneurysm. Br J Surg [Internet]. 2013;100:863-72. Available from: http://dx.doi.org/10.1002/bjs.9101
24. Powell
JT, Sweeting MJ, Ulug P, Blankensteijn
JD, Lederle FA, Becquemin
JP, et al. Meta-analysis of individual-patient data from EVAR-1, DREAM, OVER
and ACE trials comparing outcomes of endovascular or open repair for abdominal
aortic aneurysm over 5 years. Br J Surg
[Internet]. 2017;104:166-78. Available from: http://dx.doi.org/10.1002/bjs.10430
25. Li B, Khan
S, Salata K, Hussain MA, de
Mestral C, Greco E, et al. A systematic review and meta-analysis of the long-term
outcomes of endovascular versus open repair of abdominal aortic aneurysm. J Vasc Surg
[Internet]. 2019;70:954-69.e30. Available from: http://dx.doi.org/10.1016/j.jvs.2019.01.076
26.
Sweeting MJ, Balm R, Desgranges P, Ulug P, Powell JT, Ruptured Aneurysm Trialists.
Individual-patient meta-analysis of three randomized trials
comparing endovascular versus open repair for ruptured abdominal aortic
aneurysm. Br J Surg
[Internet]. 2015;102:1229–39. Available from: http://dx.doi.org/10.1002/bjs.9852
27. Alsusa H, Shahid A, Antoniou GA. A comparison of endovascular versus open repair for
ruptured abdominal aortic aneurysm - Meta-analysis of propensity score-matched
data. Vascular [Internet]. 2022;30:628-38. Available from: http://dx.doi.org/10.1177/17085381211025168
28. Tchana-Sato V, Sakalihasan N, Defraigne JO. [Ruptured abdominal aortic
aneurysm]. Rev Med Liege [Internet]. 2018;73:296–9. Available from: https://www.ncbi.nlm.nih.gov/pubmed/29926569
29. Azhar B, Patel SR, Holt PJE, Hinchliffe
RJ, Thompson MM, Karthikesalingam A. Misdiagnosis of
ruptured abdominal aortic aneurysm: systematic review and meta-analysis. J Endovasc Ther [Internet]. 2014;21:568-75. Available from: http://dx.doi.org/10.1583/13-4626MR.1
30. Mai T,
Woo MY, Boles K, Jetty P. Point-of-Care Ultrasound Performed by a Medical
Student Compared to Physical Examination by Vascular Surgeons in the Detection
of Abdominal Aortic Aneurysms. Ann Vasc Surg [Internet]. 2018;52:15-21.
Available from: http://dx.doi.org/10.1016/j.avsg.2018.03.015
31. Shuman
WP, Hastrup W Jr, Kohler
TR, Nyberg DA, Wang KY, Vincent LM, et al. Suspected leaking abdominal aortic
aneurysm: use of sonography in the emergency room. Radiology [Internet]. 1988;168:117-9.
Available from: http://dx.doi.org/10.1148/radiology.168.1.3289085
32.
Fernando SM, Tran A, Cheng W, Rochwerg B, Strauss SA,
Mutter E, et al. Accuracy of presenting symptoms, physical examination, and
imaging for diagnosis of ruptured abdominal aortic aneurysm: Systematic review
and meta-analysis. Acad Emerg Med [Internet]. 2022;29:486–96. Available from: http://dx.doi.org/10.1111/acem.14475
33. Haug ES, Romundstad P, Aadahl P, Myhre HO. Emergency
non-ruptured abdominal aortic aneurysm. Eur J Vasc Endovasc Surg
[Internet]. 2004;28:612-8. Available from: http://dx.doi.org/10.1016/j.ejvs.2004.09.013
34.
Sullivan CA, Rohrer MJ, Cutler BS. Clinical management of the
symptomatic but unruptured abdominal aortic aneurysm.
J Vasc Surg [Internet].
1990;11:799-803. Available from: http://www1.mosby.com/scripts/om.dll/serve?action=searchDB&searchDBfor=art&artType=abs&id=a19420
35. Ten
Bosch JA, Koning SW, Willigendael
EM, VAN Sambeek MR, Stokmans
RA, Prins MH, et al. Symptomatic abdominal aortic
aneurysm repair: to wait or not to wait. J Cardiovasc
Surg [Internet]. 2016;57:830-8.
Available from: https://www.ncbi.nlm.nih.gov/pubmed/23867861
36. Garagoli F, Fiorini N, Pérez MN, Rabellino
JM, Valle Raleigh J, Chas JG, et al. Neutrophil-to-lymphocyte
ratio and platelet-to-lymphocyte ratio predict in-hospital mortality in
symptomatic but unruptured abdominal aortic aneurysm
patients. Int Angiol [Internet].
2022;41:188-95. Available from: http://dx.doi.org/10.23736/S0392-9590.22.04754-X
37. Lenk T, Whittle J, Miller TE, Williams DGA, Bronshteyn YS. Focused cardiac ultrasound in preoperative
assessment: the perioperative provider’s new stethoscope? Perioper Med (Lond)
[Internet]. 2019;8:16. Available from: http://dx.doi.org/10.1186/s13741-019- 0129-8
38. Antonello M, Lepidi S, Kechagias A, Frigatti P, Tripepi A, Biancari F, et al.
Glasgow aneurysm score predicts the outcome after emergency open repair of
symptomatic, unruptured abdominal aortic aneurysms. Eur J Vasc Endovasc
Surg [Internet]. 2007;33:272–6.
Available from: http://dx.doi.org/10.1016/j.ejvs.2006.09.006
39. Samy AK, Murray G, MacBain G.
Glasgow aneurysm score. Cardiovasc Surg [Internet]. 1994;2:41-4.
Available from: https://www.ncbi.nlm.nih.gov/pubmed/8049922
40. Sadat
U, Boyle JR, Walsh SR, Tang T, Varty K, Hayes PD.
Endovascular vs open repair of acute abdominal aortic
aneurysms--a systematic review and meta-analysis. J Vasc
Surg [Internet]. 2008;48:227–36.
Available from: http://dx.doi.org/10.1016/j.jvs.2007.11.028