CARTAS
CIENTÍFICAS
Fístula coronaria-pulmonar como causa de
síndrome coronario agudo
La fístula coronaria (FC) es una malformación rara, congénita o
adquirida, que consiste en la comunicación entre una o más arterias coronarias
con una cámara cardíaca o un gran vaso alrededor del corazón. (1) La fístula
coronaria-pulmonar representa un 15-30% de las FC. (2) Las FC con relevancia clínica son en general las de mayor tamaño,
que se presentan con angina y disnea asociadas al fenómeno de robo coronario, y
ocasionalmente a disfunción miocárdica. (3)
Presentamos el caso de una mujer de 55 años, con antecedente de
hipertensión arterial, poco apego al tratamiento, sin antecedentes quirúrgicos,
cardiológicos o traumas de importancia. Ingresa a emergencias con cuadro
clínico de 24 horas de evolución con cefalea holocraneana
pulsátil, de intensidad moderada, y dolor retroesternal
opresivo de moderada a gran intensidad, que irradia a hombro y brazo izquierdo,
acompañados de disnea y palidez generalizada. Al examen físico presenta presión
arterial de 200/70 mmHg, frecuencia respiratoria 20
rpm, saturación arterial de O2 94%. El
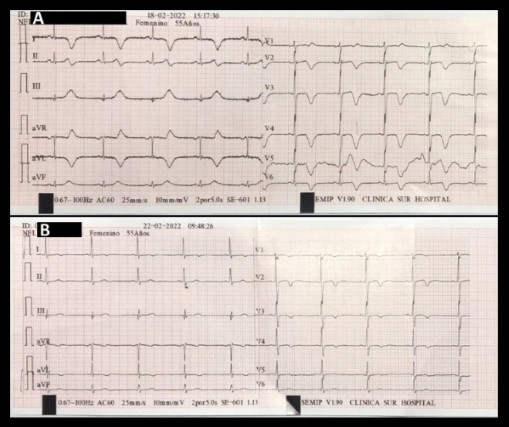
electrocardiograma muestra ritmo sinusal, 58 lpm, presencia de ondas T negativas en cara anteroseptal y lateral alta, y ausencia de ondas Q. (Figura
1A) Datos de laboratorio: Troponina T 82 ng/mL, CK-MB 9,34 ng/ mL. El ecocardiograma Doppler transtorácico informa
fracción de eyección ventricular izquierda (FEVI) de 60%, hipoquinesia
apical, disfunción diastólica grado 1, ausencia de derrame pericárdico o
trombos intracavitarios, sin hipertensión pulmonar
(HP).
Fig. 1. A. Electrocardiograma de
ingreso. Presenta T negativas en las derivaciones DI, AVL, V2- V6 (cara lateral
alta y antero-septal). B. Electrocardiograma al alta:
se observa mejoría en la repolarización ventricular izquierda en las
derivaciones DI, AVL y V1- V6.
Con diagnóstico de infarto agudo de miocardio (IAM) sin elevación del
segmento ST, ingresa a Hemodinamia. En la cinecoronariografía (CCG) se objetiva arterias coronarias epicárdicas sin lesiones, y una fístula coronaria que se
origina en el segmento distal de la arteria coronaria derecha (ACD) y drena en
la circulación pulmonar derecha, vaso de mediano tamaño con calibre de 2,5 mm
en la porción proximal (Figura 2 A y B). En el ventriculograma izquierdo se
observa hipoquinesia apical e inferoapical,
reserva contráctil levemente disminuida.
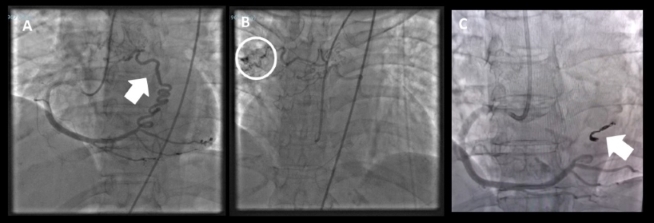
Fig. 2. A. y B. Angiografía de la
arteria coronaria derecha (ACD). Arteria dominante sin lesiones, se objetiva
fistula de mediano tamaño de origen distal y trayecto tortuoso (flecha blanca)
que drena en la circulación pulmonar (círculo blanco). C. Angiografía final de
ACD. Muestra oclusión de la fistula coronaria-pulmonar, dispositivos coils (flecha blanca), y ACD permeable en todos sus ramos
sin imagen de disección, trombo o embolización.
Se decide la embolización percutánea de
la fístula después de la primera curva, usando 3 coils,
de 4,0 mm × 7 cm, 5,0 mm × 10 cm y 3 mm × 9 cm, con resultado exitoso
comprobado en la angiografía final, sin complicaciones. (Figura
2 C) Se decide el alta al tercer día de hospitalización, con la
paciente asintomática, y mejoría de electrocardiograma (Figura
1 B). El ecocardiograma no revela alteraciones en la contractilidad
parietal, la función sistólica está conservada y la presión pulmonar normal.
La FC fue descrita por primera vez en 1865 por Krause; es una
malformación vascular en su mayoría congénita, de relativamente baja
incidencia, 0,3% de las cardiopatías congénitas, pero la patología congénita hemodinámicamente significativa más común de las arterias
coronarias, con un 13-14% de las anomalías coronarias valoradas por CCG.(3,4) La mayoría
de las FC surgen de la ACD o de la arteria descendente anterior, y drenan a
estructuras de baja presión como las cámaras cardíacas derechas, la arteria
pulmonar, la vena cava superior o el seno coronario.(4,5)
Con frecuencia las FC son de pequeño tamaño, asintomáticas, y
habitualmente diagnosticadas como hallazgos en estudios por imágenes. Suelen
ocluirse de manera espontánea; no obstante, las de mayor tamaño o múltiples, en
relación con el grado de gravedad del cortocircuito o el secuestro coronario,
se asocian a síntomas como fatiga, disnea, palpitaciones y/o angina. (2,6) Suelen
complicarse con sobrecarga de volumen, hipertrofia miocárdica e insuficiencia
cardíaca congestiva, o, isquemia/ infarto de miocardio en ausencia de
ateroesclerosis coronaria, arritmias, HP, endocarditis o ruptura. (1,2)
Interpretamos en este caso, que la angina se debe a un mayor
requerimiento miocárdico de O2 secundario
a las cifras de presión arterial elevadas. Mecánicamente consideramos que la
isquemia miocárdica antero-apical fue provocada por un efecto de robo a la
circulación de la arteria descendente anterior a través de los ramos septales, ya que la fístula se originaba en el segmento distal
de la ACD. Clasificamos el cuadro como IAM tipo 2 debido a la elevación de las
enzimas cardíacas.
La FC de gran tamaño debe ocluirse independientemente de la
sintomatología, y la de mediano tamaño debe cerrarse en pacientes que presenten
síntomas. (5,6) El tratamiento depende de la anatomía de la fístula, presentación
clínica y la experiencia del equipo, y se puede elegir técnica quirúrgica o
percutánea, teniendo en consideración el riesgo asociado al procedimiento y su
factibilidad. (2,5) A pesar de la sugerencia de la ligación quirúrgica sobre la embolización con coils, (2) fue
beneficioso individualizar la terapéutica.
En conclusión, la FC es la malformación congénita de las arterias
coronarias hemodinámicamente relevante más común.
Recomendamos tratar toda FC de mediano tamaño. Esta entidad a lo largo de los
años puede condicionar a un mayor crecimiento de la arteria lo que significa un
mayor trastorno cardíaco concomitante y complejidad terapéutica.
Carlos I. Soledispa1,
Marco Larrea 1,
Stephanie S. Alberca1, Ariel Zelaya1,
Klinton Sanango1
1 Clínica
Sur Hospital, Área de Hemodinamia (Guayaquil,
Ecuador).
E-mail: carisosu@gmail.com
Declaración de conflicto de intereses
Los autores declaran que no
tienen conflicto de intereses.
Consideraciones éticas
No aplican.
Rev Argent Cardiol 2023;91:162-164. http://dx.doi.org/10.7775/rac.es.v91.i2.20618
1.
Urmeneta Ulloa J, Molina Borao I, Ochoa Rea ME, Sánchez-Insa
E. Percutaneous closure of coronary artery fistula before lung transplantation.
Arch Bronconeumol 2017;53:520-1.
https://doi.org/10.1016/j. arbres.2017.02.013
2.
Sulemankhil I, Mohamed AH, Gilani SA.
Coronary-Pulmonary Artery Fistula Repair With Coil
Embolization: A Single Center Experience. Cureus.2022;14:e28407.
https://doi.org/10.7759/cureus.28407
3. Buccheri
D, Dendramis G, Piraino D, Chirco PR, Carità P, Paleologo C, et al. Coronary artery fistulas as a cause of angina: How to
manage these patients? Cardiovascular Revascularization
Medicine [Internet]. 2015;16:306–9. https://doi.org/10.1016/j.carrev.2015.04.011
4. Gowda
RM, Vasavada BC, Khan IA. Coronary artery fistulas: Clinical and
therapeutic considerations. Int J Cardiol 2006;107:7–10. https://doi.org/10.1016/j.ijcard.2005.01.067
5. Al-Hijji
M, el Sabbagh A, el Hajj S,
AlKhouli M, el Sabawi B, Cabalka A, et al. Coronary
Artery Fistulas: Indications, Techniques, Outcomes, and Complications of Transcatheter Fistula Closure. JACC Cardiovasc
Interv [Internet]. 2021;14:1393-406.
https://doi.org/10.1016/j.jcin.2021.02.044
6.
Buccheri D, Chirco PR, Geraci S, Caramanno G, Cortese B. Coronary Artery Fistulae: Anatomy, Diagnosis and
Management Strategies. Heart Lung Circ 2018;27:940–51. https://doi.org/10.1016/j. hlc.2017.07.014
Espondiloartropatía inflamatoria como única manifestación del
mixoma auricular izquierdo
Los tumores cardíacos son infrecuentes. Su incidencia es de
0,002%. Pueden originarse en el miocardio o en el pericardio, son primarios y
secundarios, estos últimos 20 veces más frecuentes. (1)
Las neoplasias primarias cardíacas son poco comunes: representan
un 0,25%. El 75% son benignas e incluyen mixomas, rabdomiomas, fibromas y lipomas. (2)
El mixoma auricular es el tumor cardíaco
benigno más frecuente. Un 75% se origina en la aurícula izquierda, un 20% en la
aurícula derecha y el 5% restante en los ventrículos. (1) Clínicamente los mixomas pueden ser
asintomáticos y hallarse incidentalmente, o bien ocasionar sintomatología
variada que depende de su ubicación, tamaño y movilidad. La triada sintomática
clásica incluye manifestaciones sistémicas (pérdida de peso, fatiga, fiebre),
cardíacas (arritmias, insuficiencia mitral o tricúspidea
por interferir en la coaptación valvular, pericarditis, disnea, síncope) y
fenómenos embólicos (pulmonares o sistémicos). (2) Si bien
estas son las manifestaciones más frecuentes se han descripto formas de
presentación atípicas.
El ecocardiograma Doppler es el método
de elección para el diagnóstico y a su vez para establecer las características
y repercusión hemodinámica.
Se describe a continuación el caso clínico de un mixoma auricular izquierdo de presentación atípica.
Mujer de 61 años, dislipidémica y extabaquista. Sin antecedentes cardiovasculares. Consulta
por artralgias sacroilíacas de meses de evolución,
por lo que se realizan determinaciones de laboratorio, que revelan eritrosedimentación (84 mm/h) y proteína C reactiva (6,2
mg/L) elevadas, sin otra alteración.
La paciente es evaluada por el servicio de Reumatología, que
diagnostica espondiloartropatía inflamatoria con
marcadores inflamatorios persistentemente elevados sin cumplir criterios de
enfermedad reumatológica, por lo que se solicita tomografía por emisión de positrones
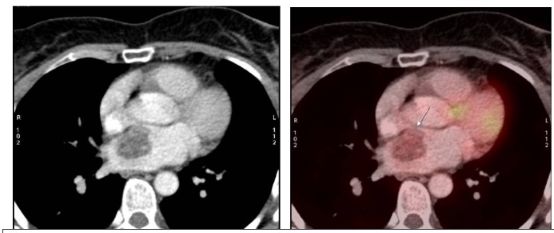
(PET) que evidencia tumor único en aurícula izquierda (Figura
1).
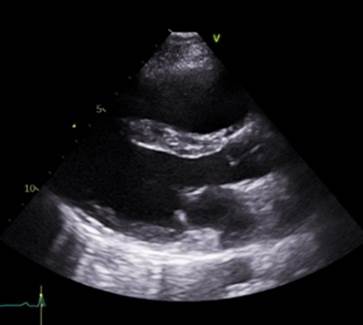
Fig. 1. PET que evidencia imagen hipodensa en aurícula izquierda con moderada actividad
metabólica.
Se prosigue con la realización de un ecocardiograma Doppler que evidencia imagen heterogénea redondeada en la
aurícula izquierda, adherida al septum interauricular, sésil, con amplio
movimiento anárquico, en contacto con la vena pulmonar superior derecha sin
invadirla. Dicha imagen no interfiere con la apertura y cierre de la válvula
mitral (Figura 2).
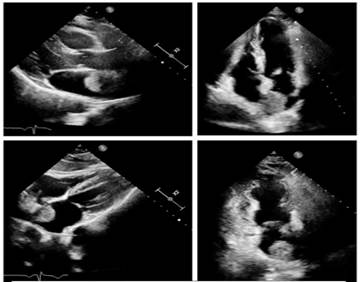
Fig. 2. Múltiples vistas de
ecocardiograma Doppler en las que se evidencia en
aurícula izquierda imagen heterogénea redondeada adherida al septum
interauricular.
Por ello se decide realizar una tomografía que evidencia masa en
la aurícula izquierda en contacto con el septum interauricular de 30 × 22 mm,
de densidad heterogénea, con bordes regulares, con realce luego de la
administración de contraste endovenoso, sin evidencia de invasión de venas
pulmonares. Se interpreta como posible mixoma
auricular, por lo que se decide resección quirúrgica. Se realiza abordaje transeptal, se reseca tumoración de 5 cm sin complicaciones
y se envía muestra a Anatomía Patológica.
Se recibe resultado, que informa proliferación de células
fusiformes, sin atipia, en regueros y perivasculares
en medio de estroma laxo con signos de hemorragia antigua y reciente, base con
escaso tejido fibroso y miocitos, compatible con mixoma.
Tras la resección quirúrgica, en el seguimiento la paciente
evoluciona con mejoría de los síntomas articulares hasta su desaparición y
normalización de los marcadores inflamatorios.
El mixoma representa el tumor cardíaco
benigno más frecuente; es más habitual en mujeres en edad adulta, (2) tal como el
caso presentado.
La localización más común es la aurícula izquierda (75%). Es un
tumor intracavitario, pediculado o sésil, móvil, y
suele estar adherido a través de una base de implantación al septum
interauricular.
Las manifestaciones clínicas de los mixomas
dependen de la localización, el tamaño y la movilidad. La tríada sintomática
más frecuente incluye obstrucción intracardíaca,
embolias y manifestaciones sistémicas.
Según una serie francesa de 112 casos, el 67% se presentó con
insuficiencia cardíaca secundaria a obstrucción de la válvula mitral, el 29% se
manifestó con embolias, las más frecuentes cerebrales, y un 34% con síntomas
generales como fiebre, pérdida de peso o símil enfermedad del tejido conectivo.
(3)
La obstrucción intracardíaca es
frecuente en los mixomas pediculados ubicados en la
aurícula izquierda que protruyen hacia el ventrículo izquierdo y que producen
déficit de coaptación de la válvula mitral y la consiguiente insuficiencia
valvular. Si bien menos frecuente, los localizados en la aurícula derecha pueden
protruir hacia la válvula tricúspidea y generar
regurgitación. En ambos casos pueden manifestarse con insuficiencia cardíaca o
síncope. (3)
Las embolias son más frecuentes en los mixomas
papilares, ya que pierden consistencia y se hacen más frágiles con el
movimiento anárquico. El sitio de embolia depende de la localización del tumor.
Los mixomas de la aurícula izquierda suelen embolizar al sistema nervioso, generando accidente
cerebro-vascular o amaurosis. La afección de las arterias coronarias, renales o
de miembros inferiores es menos frecuente. (4)
Los síntomas constitucionales pueden aparecer como enfermedades
del tejido conectivo, con mal estado general, pérdida de peso, anorexia y
fiebre. Estas manifestaciones son más frecuentes en mujeres que en hombres y en
mixomas ubicados en la aurícula derecha. (4)
Se cree que las manifestaciones extra cardíacas son causadas por
fenómenos embólicos e inflamación causada por la
liberación de citoquinas. (5) La polimialgia reumática, manifestación
que motiva a la consulta de nuestra paciente, es infrecuente. Se caracteriza
por dolor muscular en articulaciones proximales y aumento de los niveles de
marcadores inflamatorios en sangre, es frecuente en adultos jóvenes y afecta
con mayor frecuencia a mujeres (relación 3:1). (6)
El ecocardiograma Doppler es esencial
para el diagnóstico de los mixomas, para definir
localización, tamaño y complicaciones. Tanto la resonancia cardíaca como la
tomografía multicorte cardíaca aportan información
adicional para la toma de decisiones.
El tratamiento del mixoma es su
extirpación por cirugía, lo que reduce el riesgo de embolia. Si bien el riesgo
de recurrencias es bajo, se recomienda el seguimiento con ecocardiograma Doppler. (4)
En el caso presentando la paciente debuta con manifestaciones reumatologícas con marcadores inflamatorios
persistentemente elevados, por lo que se le solicitaron múltiples estudios en
los que se halló incidentalmente el mixoma auricular
izquierdo.
Sin
dudas el mixoma sigue siendo una entidad de difícil
diagnóstico. El hecho de que la mayoría sean asintomáticos o se presenten con
síntomas inespecíficos hace que sea una entidad poco sospechada y en su
mayoría diagnosticada incidentalmente. Es fundamental tener en cuenta las
posibles manifestaciones cardiovasculares y sistémicas para así sospecharlo,
diagnosticarlo y tratarlo oportunamente.
Esperanza Raimundo, Roberto Freue, Fernando PiccininiMTSAC, Florencia Castro, Martín
Vivas, Pablo ElissamburuMTSAC
Declaración
de conflicto de intereses
Los autores declaran que no tienen
conflicto de intereses.
Consideraciones
éticas
No aplican.
Rev Argent Cardiol 2023;91:164-166. http://dx.doi.org/10.7775/rac.es.v91.i2.20623
1. El Sabbagh A,
Al-Hijji MA, Thaden JJ, Pislaru SV, Pislaru C, Pellikka PA, et al. Cardiac myxoma: the great mimicker. JACC Cardiovasc Imaging 2017;10:203-6. https://doi.org/10.1016/j.jcmg.2016.06.018
2. Tyebally S, Chen D, Bhattacharyya S, Mughrabi
A, Hussain Z, Manisty C, et
al. Cardiac Tumors: JACC CardioOncology
State-of-the-Art Review. JACC CardioOncol. 2020;2:293-311. https://doi.org/10.1016/j.jaccao.2020.05.009
3. Pinede L, Duhaut P, Loire R.
Clinical presentation of left atrial cardiac myxoma.
A series of 112 consecutive cases. Medicine (Baltimore). 2001;80:159-72.
https://doi.org/10.1097/00005792-200105000-00002
4. Islam
AKMM. Cardiac myxomas: A narrative review. World J Cardiol. 2022;14:206-19. https://doi.org/10.4330/wjc.v14.i4.206
5. Macias E, Nieman E, Yomogida K, Petrucci O, Javidan C, Baszis K, et al. Rare
presentation of an atrial myxoma in an adolescent
patient: a case report and literature review. BMC Pediatr.
2018;18:373. https://doi.org/10.1186/s12887-018-1313-6
6. Mano Y, Yoshizawa
A, Itabashi Y, Ohki T, Takahashi T, Mori M, et al. Left atrial myxoma detected
after an initial diagnosis of polymyalgia rheumatica.
Intern Med. 2014;53:441-4. https://doi.org/10.2169/internalmedicine.53.1300
Tratamiento endovascular de
estenosis de vena pulmonar posterior a ablación de fibrilación auricular
La
ablación por radiofrecuencia con aislamiento de las venas pulmonares para el
tratamiento de la fibrilación auricular (FA) es un procedimiento mínimamente
invasivo y con una baja tasa de complicaciones. La estenosis de las venas
pulmonares es una de ellas, con una incidencia que oscila entre el 0,3 y 3,4%
pero una elevada morbilidad. (1-3)
Los síntomas de la estenosis de venas pulmonares incluyen disnea, tos,
hemoptisis y dolor precordial. (4)
Reportamos un caso de hemoptisis secundaria a estenosis de venas pulmonares
posterior a ablación por radiofrecuencia, tratada con angioplastia e implante
de un stent.
Paciente
de 42 años con antecedente de ablación de venas pulmonares por radiofrecuencia
en otro centro, y cuadro de neumonía de la comunidad de difícil resolución a
pesar del uso de diferentes esquemas antibióticos. El paciente acude 5 meses
después de la ablación a la central de emergencias de nuestro centro por
cuadro de hemoptisis intermitente y dolor en hemitórax izquierdo.
Al
ingreso se encuentra hemodinámicamente estable, afebril y sin signos de insuficiencia cardíaca congestiva.
En el laboratorio se evidencia hematocrito 37%, glóbulos blancos 5490/mm3,
plaquetas 229 300/mm3, eritrosedimentación
25 mm/h, y proteína C reactiva ultrasensible 10,6 mg/L. Ante la sospecha de tromboembolismo pulmonar (TEP) agudo se realiza angiotomografía de tórax que resulta negativa,
evidenciándose áreas con aumento de la atenuación en vidrio esmerilado, con
tendencia a la consolidación, distribuidas de manera difusa en el lóbulo
superior del pulmón izquierdo.
El
paciente se encuentra estable clínicamente, por lo cual es externado. Evaluado
de forma ambulatoria, realiza tratamiento empírico con antibióticos por
sospecha de neumonía atípica. Debido al antecedente reciente de ablación de FA
y el patrón evidenciado en la tomografía de tórax, se decide realizar angiotomografía cardíaca con el objetivo de evaluar las
venas pulmonares, que no pudieron ser visualizadas correctamente en la angiotomografía solicitada para TEP. En dicho estudio se
evidencia una estenosis de la vena pulmonar superior izquierda (VPSI), que
presenta un diámetro de 8,4 mm por 17 mm de largo, con marcado afinamiento en
pico de flauta y reducción crítica de la luz, con un trayecto de unos 16 mm
hasta la porción permeable intraparenquimatosa (Figura
1A). Las otras venas pulmonares están
permeables sin signos de estenosis.
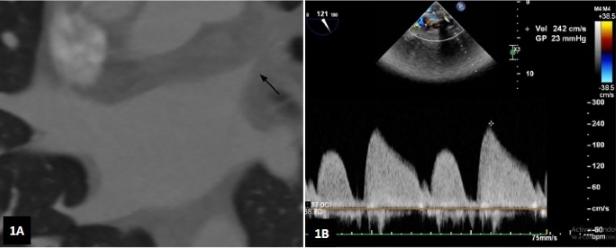
Fig.
1.
A. Imagen de angiotomografía donde se evidencia
estenosis de la vena pulmonar superior izquierda (flecha). B. Velocidad en la
vena pulmonar superior izquierda medida por ecocardiograma transesofágico
Ante
un paciente con hemoptisis y cuadro neumónico de lenta resolución y presencia de
estenosis de la VPSI, se decide angioplastia con colocación de stent en dicha vena. Durante el procedimiento
se realiza en primer lugar un ecocardiograma transesofágico
(ETE) que evidencia aumento de velocidades (velocidad pico 2,4 m/s, gradiente
pico 23 mmHg) en dicha vena, lo cual confirma el
diagnóstico (Figura 1B).
Se decide avanzar con una angioplastia, para la cual a través de un acceso
venoso femoral derecho se realiza punción transeptal
guiada por ETE y posteriormente venografia selectiva
que confirma nuevamente la estenosis de la VPSI (Figura
2A).
Posteriormente se avanzan balones de angioplastia coronaria de tamaños
crecientes, con los cuales se realiza predilatación
de la estenosis, seguido de implante de un stent
convencional de alta fuerza radial (Herculink 7,0 ×
18 mm) con un adecuado resultado angiográfico (Figura
2B),
y disminución de presiones y velocidades en el ETE (velocidad pico 1,3 m/s,
gradiente máximo 7 mmHg).
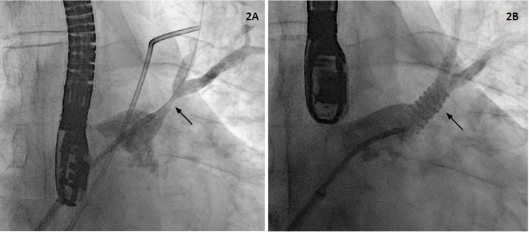
Fig.
2.
A. Venografía que evidencia estenosis de la vena
pulmonar superior izquierda (flecha). B. Venografía
posterior al implante del stent (flecha) en la vena
pulmonar superior izquierda.
El
paciente es dado de alta a las 24 horas, con anticoagulación con rivaroxabán 15 mg/d y antiagregación
con clopidogrel 75 mg/d. En el seguimiento a 3 meses
se encuentra asintomático para disnea y tos, con desaparición del dolor en
hemitórax izquierdo.
La
estenosis de venas pulmonares posterior a la ablación por radiofrecuencia es
una complicación poco frecuente y subdiagnosticada,
debido a que los síntomas pueden ser confundidos con otras patologías como la
neumonía, asma y TEP entre otros. (4)
El correcto diagnóstico de esta patología es de suma importancia, ya que la
demora puede llevar a la oclusión total de la vena pulmonar, lo cual puede
generar infarto pulmonar y hemoptisis masiva. La angioresonancia
y la angiotomografía son los métodos de diagnóstico
más precisos para detectar la estenosis de las venas pulmonares. La gravedad de
la estenosis se define de acuerdo al porcentaje de la luz comprometida, y se
divide en leve (<50%), moderada (50%-70%) y grave (>70%). El desarrollo
de síntomas suele estar asociado con la presencia de estenosis graves u
oclusiones totales, que en ocasiones pueden ser asintomáticas. El ETE es un
método diagnóstico que resulta de gran utilidad como guía durante el procedimiento,
ya que brinda información sobre la estructura de la aurícula izquierda, permite
optimizar la manipulación de los materiales como cuerdas guía y balones durante
el estudio, y además suma la evaluación del flujo y gradientes en las venas
pulmonares a fin de diagnosticar la estenosis y evaluar la efectividad del
tratamiento. (5)
En este caso se utilizó en el mismo procedimiento con fines diagnósticos, guía
para la punción transeptal (que idealmente es
inferior y anterior para mejor orientación a la VPSI) y medición de velocidades
con el tratamiento, además de permitir descartar complicaciones como el derrame
pericárdico.
El
tratamiento mediante angioplastia tiene como objetivo aliviar la presión venosa
y mejorar la perfusión del pulmón afectado. Comparada con la angioplastia con
balón, la colocación de stent se asocia
a menor tasa de reestenosis, especialmente cuando se
utilizan stents grandes (10 mm o más). (5,6) La definición del tamaño
del stent se realiza antes del
procedimiento mediante la angiotomografía, y durante
el procedimiento mediante angiografía, ya que la utilización de stents más grandes que la vena podría llevar a la ruptura y
el taponamiento cardíaco. Otros tratamientos incluyen la lobectomía pulmonar,
reservada para pacientes con oclusión o estenosis de venas pulmonares
clínicamente significativas, en los cuales la angioplastia ha resultado
frustra. (5)
Presentamos
este caso de hemoptisis, disnea y dolor secundarios a estenosis de una vena
pulmonar, tratado de forma exitosa con angioplastia con colocación de stent. Reconocer esta patología, diagnosticarla a
tiempo y tratarla adecuadamente es de suma importancia para disminuir la
morbilidad de los pacientes.
Juan Ignacio Damonte1, Ezequiel Lillo2, Mariano Falconi2, MAAC, Santiago Sánchez Bustamante2, Carla Agatiello1, MAAC, Ignacio M. Seropian1
1 Servicio de Hemodinamia y
cardiología intervencionista, Instituto de Medicina Cardiovascular, Hospital
Italiano de Buenos Aires, Argentina
2 Servicio de cardiología, Instituto de Medicina
Cardiovascular, Hospital Italiano de Buenos Aires, Argentina
Dirección para separatas: Ignacio M. Seropian, ignacio.seropian@hospitalitaliano.org.ar
Declaración
de conflicto de intereses
Los autores declaran que no tienen
conflicto de intereses.
Consideraciones éticas
No aplican.
Rev Argent Cardiol 2023;91:166-168. http://dx.doi.org/10.7775/rac.es.v91.i2.20623
1.
Correction to: Severe Pulmonary Vein Stenosis Resulting From Ablation for
Atrial Fibrillation: Presentation, Management, and Clinical Outcomes.
Circulation 2017;135(18):e1016. https://doi.org/10.1161/CIR.0000000000000494
2. Cappato R, Calkins H, Chen S-A, et al. Updated worldwide
survey on the methods, efficacy, and safety of catheter ablation for human
atrial fibrillation. Circ Arrhythm
Electrophysiol 2010;3:32–8. https://doi.org/10.1161/CIRCEP.109.859116
3. Saad EB, Rossillo A, Saad CP, et al. Pulmonary vein stenosis after
radiofrequency ablation of atrial fibrillation: functional characterization,
evolution, and influence of the ablation strategy. Circulation 2003;108:3102–7. https://doi.org/10.1161/01.CIR.0000104569.96907.7F
4. Fender
EA, Widmer RJ, Hodge DO, Packer DL, Holmes DR Jr.
Assessment and Management of Pulmonary Vein Occlusion After Atrial Fibrillation
Ablation. JACC Cardiovasc Interv
2018;11:1633–9. https://doi.org/10.1016/j.jcin.2018.05.020
5. Calkins
H, Brugada J, Packer DL, et al. HRS/EHRA/ECAS expert
consensus statement on catheter and surgical ablation of atrial fibrillation:
recommendations for personnel, policy, procedures and follow-up. A report of
the Heart Rhythm Society (HRS) Task Force on Catheter and Surgical Ablation of
Atrial Fibrillation developed in partnership with the European Heart Rhythm
Association (EHRA) and the European Cardiac Arrhythmia Society (ECAS); in
collaboration with the American College of Cardiology (ACC), American Heart
Association (AHA), and the Society of Thoracic Surgeons (STS). Endorsed and
approved by the governing bodies of the American College of Cardiology, the
American Heart Association, the European Cardiac Arrhythmia Society, the
European Heart Rhythm Association, the Society of Thoracic Surgeons, and the
Heart Rhythm Society. Europace 2007;9:335-79.
https://doi.org/10.1093/europace/eum120
6. Xuan Z,
Liu B, Ci M, Wang Z, Fan Y. Hemoptysis secondary to pulmonary vein stenosis
after radiofrequency ablation for atrial fibrillation: A case report and
literature review. J Interv Med 2020;3:98-100. https://doi.org/10.1016/j.jimed.2020.03.008
Septostomía transeptal auricular con
balón en paciente con hipertensión arterial pulmonar severa y lupus eritematoso
sistémico
Se
describe el caso de una paciente de sexo femenino de 20 años con diagnóstico
previo de enfermedad mixta del tejido conectivo en 2018, sin seguimiento en los
últimos 18 meses, tiroiditis de Hashimoto y bronquiectasias. Acudió a Guardia
Externa por dolor abdominal, náuseas y diarrea. A su ingreso se constataron
signos de insuficiencia cardíaca derecha (edemas en miembros inferiores,
ingurgitación yugular sin colapso inspiratorio, reflujo hepatoyugular
positivo y hepatomegalia), aumento de la intensidad del segundo ruido cardíaco
a expensas del componente pulmonar, y soplo sistólico en foco tricuspídeo. El estudio diagnóstico inicial incluyó un
electrocardiograma con signos de sobrecarga de cavidades derechas y bloqueo
completo de rama derecha, y radiografía de tórax con aumento del segundo arco
pulmonar derecho e índice cardiotorácico conservado. En el ecocardiograma Doppler se observó dilatación de cavidades derechas, disfunción
grave del ventrículo derecho, insuficiencia tricuspídea
grave con velocidad de regurgitación pico mayor que 4,5 metros por segundo
(m/s), presión sistólica de la arteria pulmonar (PSAP) de 105 mm Hg, presión
media de la arteria pulmonar (PAPm) de 55 mm Hg y
derrame pericárdico leve. (Figura 1).
Consecutivamente se realizó cateterismo cardíaco derecho que confirmó el
diagnóstico de hipertensión arterial pulmonar (HAP) grave con presión media de
aurícula derecha de 11 mm Hg, PAPm de 63 mm Hg,
presión de enclavamiento pulmonar de 10 mm Hg, resistencia vascular pulmonar de
21 unidades Woods (UW), gradientes transpulmonar y
diastólico de 53 mm Hg y 43 mm Hg respectivamente, gasto cardiaco (GC) de 3,20
L/min , índice cardíaco (IC) de 2,6 L/min/m2,
índice de volumen sistólico (IVS) 23 ml/lat/m2,
saturación venosa mixta de 65% y saturación arterial de 97%. Por falla
ventricular derecha marcada, inició infusión endovenosa continua de furosemida
sin respuesta favorable, soporte inotrópico con milrinona
a dosis máxima que posteriormente se rotó a levosimendán
0.1 ug/kg/ min y soporte vasopresor
con noradrenalina a dosis intermedias. La paciente evolucionó de forma desfavorable
con signos de bajo gasto cardíaco y falla grave del ventrículo derecho. Debido
a la falta de acceso inmediato a prostanoides parenterales,
se realizó septostomía transeptal
con balón de forma exitosa (fenestración de 5 mm) (Figura
2).
La paciente presentó mejoría del estado clínico, con derivación precoz a un
centro de mayor complejidad para valoración pretrasplante
e inicio de infusión continua de epoprostenol
endovenoso, con dosis en ascenso hasta 12 ng/kg/min,
previo destete y suspensión de inotrópicos, e inicio de ambrisentán
10 mg y tadalafilo 10 mg con buena tolerancia. En el
ecocardiograma Doppler control presentó dilatación
moderada de cavidades derechas, PSAP de 70 mm Hg y solución de continuidad
interauricular de 0,9 mm. (Figura
3)
El cateterismo cardiaco evolutivo demostró descenso de la PAPm,
RVP y mejoría del GC e IC (43 mm Hg, 7,3 UW, 4,8 l/min y 3,6 l/min/m2,
respectivamente). Fue valorada por el servicio de Reumatología que confirmó el
diagnóstico de lupus eritematoso sistémico por criterios clínicos e
inmunológicos y nefritis lúpica grado II por biopsia
renal.
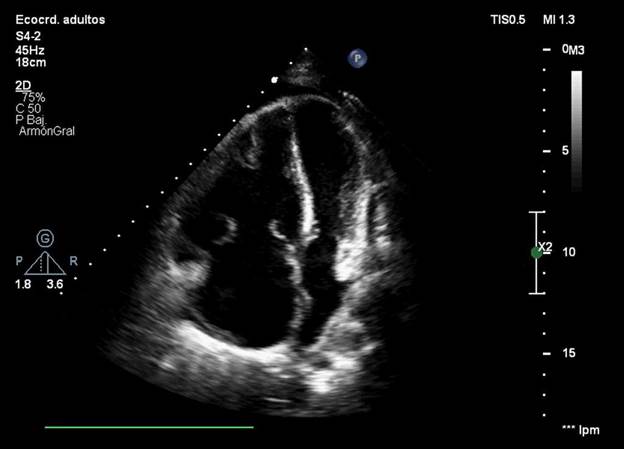
Fig.
1.
Ecocardiograma Doppler, ventana de 4 cámaras apical:
se observa gran dilatación de cavidades derechas, con marcado desplazamiento
del septum interventricular, disminución del diámetro del ventrículo izquierdo
e insuficiencia tricuspídea grave.
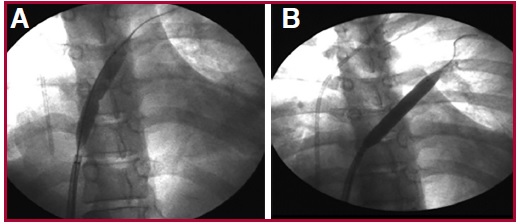
Fig.
2.
Septostomía atrial con balón. Se realiza dilatación
con balón alcanzando diámetro máximo de 5 mm guiado bajo fluoroscopía.
A: Inflado de balón sobre guía centrado en el septum interauricular. B: Inflado
total del balón.
Fig.
3.
Ventana eje paraesternal largo: se observa mejoría
evolutiva del diámetro del ventrículo derecho, con menor compresión hacia
ventrículo izquierdo e hipertrofia del septum interventricular.
La
prevalencia de HAP en enfermedad del tejido conectivo (ETC) es elevada,
principalmente en la esclerodermia y en segundo lugar en el lupus eritematoso
sistémico, con un valor que ronda entre 0,5 y 17,5%, de acuerdo al método
diagnóstico utilizado. (1)
Esta entidad continúa presentando una elevada morbimortalidad a pesar de la
evidencia observada con el tratamiento de drogas específicas, mayor comparada
con la HAP idiopática (sobrevida a 1 año en la HAP por ETC 86%, vs 93% en la
HAP idiopática). (2)
Los pacientes que no responden al tratamiento máximo combinado, incluyendo prostanoides parenterales, deben ser referidos a trasplante
bipulmonar.(3)
Sin embargo, muchos pacientes con HAP no son candidatos a trasplante o aguardan
tiempos excesivos y fallecen antes de llegar a ser trasplantados. Es por esto
que la septostomía transeptal
debe ser considerada en aquellos que se encuentran en lista de trasplante bipulmonar, que no responden al esquema terapéutico máximo
o en caso de que éste no sean tolerado o no estén disponible. (4) Es fundamental recordar que
este procedimiento está contraindicado en caso de saturación de oxigeno
arterial menor que 90%, presión en la aurícula derecha mayor que 20 mm Hg y
valor de hemoglobina menor que 12 mg/dL y debe ser
realizado en centros de referencia. Diversos estudios han reportado mejoría de
los síntomas y de variables hemodinámicas luego de la septostomía,
con descompresión del ventrículo derecho, aumento de la precarga del ventrículo
izquierdo y del transporte sistémico de oxigeno sin complicaciones asociadas al
procedimiento en centros con elevada experiencia. (5)
Recientemente
se publicó un metaanálisis de 6 estudios con 204
pacientes que observó una reducción en la presión de la aurícula derecha (p
<0,001), aumento del índice cardíaco (p <0,001) y de la presión de la
aurícula izquierda (p <0,001), pero con reducción significativa de la
saturación de oxígeno y una mortalidad a las 48 horas y 30 días de 4,8% y
14,6%, respectivamente. (6)
Estos
datos sugieren que la septostomía atrial es un
procedimiento invasivo y relativamente seguro en centros de experiencia y solo
debe indicarse en pacientes con HAP grave en estado avanzado como puente al
trasplante o cuando no hay respuesta al triple esquema que incluye un prostanoide parenteral, o en situaciones en que el
tratamiento farmacológico no está disponible.
Guillermina Sorasio1, Carola Zambrano1, Susana Taboada1, Fernando Di Tomasso1, Aldo Peruso1, Enrique Domine1, Ignacio Bluro2
1 Servicio de Cardiología, Hospital Rivadavia. Buenos
Aires. Argentina. Hospital Italiano de Buenos Aires.
2 Hospital Italiano de Buenos Aires
Dirección para separatas: Guillermina Sorasio - Tel 1156639403- guillerminasorasio@gmail.com
Declaración
de conflicto de intereses
Los autores declaran que no tienen
conflicto de intereses.
Consideraciones éticas
No aplican.
Rev Argent Cardiol 2023;91:168-170. http://dx.doi.org/10.7775/rac.es.v91.i2.20622
1. Tselios
K, Gladman D, Urowitz M.
Systemic lupus erythematosus and pulmonary arterial hypertension: links, risks,
and management strategies. Open Access Rheumatol 2016;9:1-9. https://doi.10.2147/OARRR.S123549
2. Chung L,
Liu J, Parsons L, Hassoun P, McGoon
M, Badesch D, et al. Characterization of connective
tissue disease-associated pulmonary arterial hypertension from REVEAL:
identifying systemic sclerosis as a unique phenotype. Chest.2010;138:1383-94. https://doi.org/10.1378/chest.10-0260
3. Stacel T, Latos M, Urlik M, Necki M, Antonczyk R, Hrapkowicz T Et al.
Interventional and Surgical Treatments for Pulmonary Arterial Hypertension. J. Clin. Med. 2021;10:3326. https://doi.org/10.3390/jcm10153326
4. Velázquez I, Albarrán A, Jiménez C,
García J, Martín R y Escribano P. Septostomía
auricular en el tratamiento de la hipertensión arterial pulmonar grave del
adulto. Rev Esp Cardiol
2016;69:78-81. https://doi.10.1016/j.recesp.2015.09.011
5. 5.Chiu
JS, Zuckerman WA, Turner ME, Richmond ME, Kerstein D,
Krishnan U Et al. Balloon atrial septostomy in pulmonary
arterial hypertension: effect on survival and associated outcomes. J Heart Lung
Transplant. 2015;34:376-80. https://doi.org/10.1016/j.healun.2015.01.004
6. Khan M,
MD; Memon, M; Amin E; Yamani N; Khan S; Vincent M.et
al Use of Balloon Atrial Septostomy in Patients with
Advanced Pulmonary Arterial Hypertension. A Systematic Review and
Meta-Analysis. Chest 2019; 156:53-63. https://doi.org/10.1016/j.ijcard.2019.02.051
Síndrome portopulmonar postrasplante hepático, una etiología de disnea poco
frecuente que no hemos de olvidar
Presentamos
el caso de un paciente de 54 años, con el único antecedente de trasplante
hepático en 2019 por cirrosis alcohólica. Como parte del estudio pretrasplante, por el dato de hipertensión pulmonar (HTP)
moderada en la ecocardiografía, se realiza un cateterismo derecho, que confirma
que se trata de una HTP por hiperflujo, con
resistencias pulmonares bajas.
A
los tres meses postrasplante, el paciente acude a
nuestro servicio de urgencias por disnea progresiva y signos de congestión
pulmonar y periférica, aunque estable con oxigenoterapia con cánula nasal. Se
realiza un electrocardiograma, que revela un bloqueo de rama derecha de nueva
aparición. En la analítica, elevación de dímero D (2980 ug/mL) y del NT-proBNP, (10 500 ng/L). Para descartar la sospecha inicial de tromboembolismo pulmonar, se solicita una angiotomografía computada de arterias pulmonares (Figura
1),
que no objetiva trombos, pero sí destaca una dilatación significativa de la
arteria pulmonar, sugestiva de HTP significativa. Dada la escasa mejoría con
diuréticos, es valorado por el servicio de Cardiología de nuestro centro. En la
ecocardiografía transtorácica (ETT) (Figura
2),
se distingue una dilatación y disfunción marcada del ventrículo derecho (VD),
con una presión sistólica de la arteria pulmonar (PSAP) estimada de 120 mmHg, sugestivo de HTP grave.
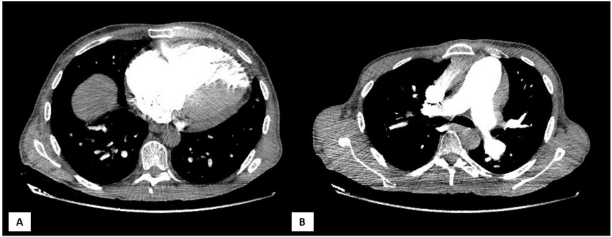
Fig.
1.
Angiotomografía computada de arterias pulmonares.
Cortes axiales a nivel de cavidades cardíacas ventriculares (A) y a nivel de
salida de grandes vasos y bifurcación de la arteria pulmonar (B). No se
aprecian defectos de repleción a nivel intravascular
en la arteria pulmonar ni imágenes sugestivas de trombo (B). Llama la atención
la dilatación de VD, con una relación ventrículo derecho/ventrículo izquierdo
>1 (A). VD: ventrículo derecho
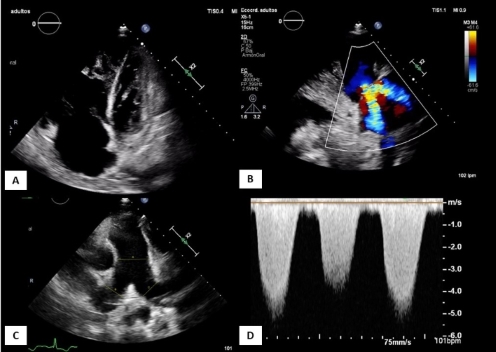
Fig.
2.
Ecocardiograma transtorácico al ingreso. Planos
apical 4 cámaras (A), paraesternal eje largo
modificado sobre VD (B), paraesternal eje corto a
nivel de grandes vasos (C) y Doppler continuo sobre
flujo de insuficiencia tricuspídea (D). En (A) se
aprecia dilatación y disfunción grave del VD, con insuficiencia tricuspídea grave funcional (B). Dilatación de la arteria
pulmonar (C). El gradiente VD-AD de la insuficiencia tricuspídea
por Doppler es de 120 mmHg
(D), sugestivo de HTP grave. AD: aurícula derecha; HTP: hipertensión pulmonar;
VD: ventrículo derecho
Dado
el rápido empeoramiento clínico, sobre todo a nivel respiratorio, con mayor
taquipnea y datos de insuficiencia cardiaca, se decide el ingreso en la Unidad
Coronaria, donde se inicia tratamiento endovenoso con dosis crecientes de dobutamina y furosemida (1 gramo en infusión continua). Se
realizan asimismo paracentesis evacuadoras, para manejo sintomático de la
ascitis, y se comprueba por eco Doppler el correcto
funcionamiento del injerto hepático.
Ante
un paciente con antecedentes de cirrosis, que se presenta con un cuadro de disnea
e insuficiencia cardiaca aguda, el diagnóstico diferencial a plantearnos es
amplio.
El
síndrome porto-pulmonar (PoPH) se engloba dentro de
la HTP grupo 1, (1)
y constituye el 10% del total de casos de esta entidad. Se define como la
presencia de hipertensión pulmonar arterial (HAP) asociada a hipertensión
portal. (2)
Ocurre en el 1-2% de estos pacientes; (1)
de hecho en el Registro REVEAL, (3)
estudio observacional multicéntrico de 3000 pacientes
con HAP, la prevalencia del PoPH fue del 5%, más
frecuente en mujeres y en cirrosis de causa autoinmune. La gravedad se define
en función del valor de la presión pulmonar media (PAPm),
de modo que se habla de PoPH leve en pacientes con PAPm <35 mmHg, y PoPH grave en caso de PAPm >45
mmHg. La patogénesis de esta entidad no está bien
aclarada, si bien se piensa que se debe a un desbalance entre mediadores
vasoconstrictores y vasodilatadores. La mayoría de los pacientes se encuentran
asintomáticos; entre los que tienen síntomas el más frecuente es la disnea de
esfuerzo, como el caso de nuestro paciente.
Las
guías europeas actuales más recientes (1)
recomiendan iniciar el estudio diagnóstico con el ETT, de modo que en aquellos
con datos indirectos de HTP (velocidad pico de la insuficiencia tricuspídea > 2,8 m/s, dilatación del VD, dilatación de
la arteria pulmonar o de la vena cava inferior) o con otros factores de riesgo,
se indicaría la realización de un cateterismo derecho, tal como se hizo en
nuestro paciente. El estudio reveló una HTP grave precapilar:
PAPm 57 mmHg, presión
capilar pulmonar (PCP) 11mmHg, gradiente transpulmonar
elevado, de 46 mmHg, y resistencia vascular pulmonar
(RVP) de 14,5 unidades Wood.
Los
criterios diagnósticos hemodinámicos actuales (1)
para concluir HAP son: PAPm >20 mmHg en reposo, PCP ≤15mmHg y RVP >2 UW. (1)
El
último criterio para el diagnóstico de certeza de PoPH
sería confirmar la presencia de hipertensión portal, generalmente por clínica,
siendo posible en caso de duda la realización de un cateterismo venoso para
medir el gradiente venoso hepático. (4)
En
el caso de nuestro paciente, este último criterio no se cumple, por lo que se
lo etiqueta como “probable síndrome portopulmonar”,
si bien se han descrito casos aislados en la bibliografía de diagnóstico de novo de PoPH en los primeros
6 meses postrasplante.
Se
trata de una entidad de mal pronóstico: sin tratamiento, se asocia a una
supervivencia del 14% a los 5 años, (2)
si bien se ha descrito una mejoría de la supervivencia a 5 años hasta el 51%
con tratamiento médico, y hasta el 81% con trasplante hepático. (5)
Pese
a que se han publicado resultados favorables con el tratamiento médico de la
HAP, la mayoría de estudios no van dirigidos a pacientes con PoPH (salvo el estudio PORTICO que demostró resultados
favorables a nivel hemodinámico con macitentán; o el
estudio PATENT-1, (6)
que incluyó una pequeña proporción de pacientes con PoPH,
con buenos resultados funcionales con riociguat); en
todo caso, se ha visto que esta terapia tiene efectos favorables a nivel
hemodinámico y funcional, pero sin efecto en la supervivencia.
Las
guías actuales (1)
recomiendan, en casos de riesgo elevado, como en nuestro paciente, comenzar
directamente con triple terapia con un antagonista de receptor de la endotelina, un inhibidor de la fosfodiesterasa-5 y un
agonista de la vía de prostaciclinas (recomendación
clase IIa). Se decide en nuestro paciente comenzar
con epoprostenol, sildenafil
y macitentán, y se consigue una lenta pero progresiva
mejoría, con retiro de los inotrópicos.
El
trasplante hepático clásicamente se ha considerado contraindicado en estos
pacientes, dada la elevada morbimortalidad perioperatoria,
y solamente estaría indicado en pacientes con indicación de trasplante por su
hepatopatía per se; en el caso de nuestro paciente, estando el injerto normofuncionante, no era algo a plantearse. Las guías
recomiendan iniciar tratamiento de la HAP si la PAPm
es >35 mmHg en pacientes que sean candidatos a
trasplante, (3)
que es contraindicado en pacientes con PoPH grave que
no mejore con tratamiento médico, ya que la mortalidad perioperatoria
en pacientes con PAPm>45 mmHg
se acerca al 100%.
Tras
un mes de ingreso, el paciente es dado de alta, con mantención de la triple
terapia, en control por hospitalización a domicilio. En el ETT de control a los
6 meses, se aprecia cómo la función del VD ha normalizado, y se pueden retirar
progresivamente los fármacos para su HAP.
El
diagnóstico diferencial ha de plantearse con la HTP por hiperflujo
(con RVP normal, sin que sea necesario iniciar tratamiento específico) y con el
síndrome hepatopulmonar (que clásicamente cursa sin
HTP, se caracteriza por shunts arteriovenosos en la circulación pulmonar, que ocasionan
hipoxemia, ortodesoxia y platipnea;
siendo el tratamiento de elección el trasplante hepático en casos graves).
Otras
entidades menos comunes, pero que no hemos de olvidar en pacientes con
antecedente de hepatopatía son la cardiopatía cirrótica, otras causas de
insuficiencia cardiaca clásicas, y causas extracardíacas
de disnea, comunes en este perfil de paciente, como anemia, ascitis, o
hidrotórax.
En
conclusión, la disnea en el paciente con antecedentes de hepatopatía
clásicamente ha sido un reto para el cardiólogo, no solo por el amplio abanico
de diagnósticos a valorar, sino también por su complejo perfil hemodinámico. El
síndrome portopulmonar constituye una entidad poco
frecuente. Pese a que en su definición clásica se contempla en pacientes con
hipertensión portal, es una entidad que comienza a describirse en pacientes ya
trasplantados, especialmente de forma precoz en los primeros 6 meses postrasplante, tal como reflejamos en este caso, por lo que
hemos de tenerla siempre en cuenta, dado su mal pronóstico y la ausencia de un
tratamiento específico per se.
Ana Ruiz Rodríguez1, Uxue Idiazábal Rodríguez1, Iñigo Pereiro Lili1
1 Servicio de Cardiología. Hospital Universitario de
Basurto (Bilbao, España).
Dirección para separatas: Ana Ruiz Rodríguez
- Email: anarrmo@gmail.com
Declaración
de conflicto de intereses
Los autores declaran que no tienen
conflicto de intereses.
Consideraciones
éticas
No aplican.
Rev Argent
Cardiol 2023;91:170-171. http://dx.doi.org/10.7775/rac.es.v91.i2.20617
1. Humbert
M, Kovacs G, Hoeper MM, et al. ESC/ERS Scientific
Document Group. 2022 ESC/ERS Guidelines for the diagnosis and treatment of
pulmonary hypertension. Eur Heart J
2022;43:3618-731. https://doi.org/10.1093/eurheartj/ehac237
2. Navarro-Vergara DI, Roldan-Valadez E,
Cueto-Robledo G, Jurado- Hernandez MY. Portopulmonary Hypertension: Prevalence, Clinical and Hemodynamic Features. Curr Probl Cardiol.
2021;46:100747. https://doi.org/10.1016/j.cpcardiol.2020.100747
3. Krowka MJ, Miller DP, Barst RJ, Taichman D, Dweik RA, Badesch DB, et al. Portopulmonary
hypertension: a report from the US-based REVEAL Registry. Chest. 2012;141:906-15. https://doi.org/10.1378/chest.11-0160
4. Thomas
C, et al. Portopulmonary Hypertension: From Bench to
Bedside. Front. Med. 7:569413. https://doi.org/10.3389/fmed.2020.569413
5. Savale L, Guimas M, Ebstein N, Fertin M, Jevnikar M, Renard S, et al. Portopulmonary hypertension in the current era of pulmonary
hypertension management. J Hepatol. 2020;73:130-9. https://doi.org/10.1016/j.jhep.2020.02.021
6. Cartin-Ceba R, Halank M, Ghofrani HA, Humbert M, Mattson
J, Fritsch A, et al. Riociguat treatment for portopulmonary hypertension: a subgroup analysis from the
PATENT-1/-2 studies. Pulm Circ. 2018;8:2045894018769305. https://doi.org/10.1177/2045894018769305