INTRODUCCIÓN
En
personas aparentemente sanas, el riesgo de un futuro evento cardiovascular se
relaciona con el número e intensidad de los factores de riesgo y la duración de
la exposición. (1)
Una
estrategia ampliamente difundida en prevención cardiovascular es identificar,
mediante puntajes de riesgo, a aquellos individuos con un riesgo elevado de
desarrollar enfermedad cardiovascular, y recomendar medidas preventivas según
el nivel de riesgo calculado. (1,2)
Los puntajes o funciones de riesgo son ecuaciones matemáticas que calculan la
probabilidad de que un individuo presente el evento de interés en un determinado
intervalo de tiempo, según el nivel de exposición a diferentes factores de
riesgo. (3)
Sin embargo, estos puntajes tienen grandes limitaciones relacionadas con la
calibración, la discriminación y la baja sensibilidad, ya que la mayor parte de
los eventos cardiovasculares se presentan en el grupo de la población con
riesgo bajo o intermedio. (4)
Múltiples
biomarcadores adicionales que permiten mejorar la
estratificación del riesgo cardiovascular han sido evaluados (moduladores de
riesgo). (5)
La detección de placas ateroscleróticas carotídeas
(PAC) mejora la predicción de eventos cardiovasculares con respecto a la
estimación realizada por modelos que solo consideran los factores de riesgo
convencionales. (6,7)
Asimismo, el puntaje de calcio arterial coronario (pCAC)
estimado por tomografía computada multicorte, se
asocia fuertemente y de manera gradual con el riesgo de presentar eventos
cardiovasculares, independientemente de la edad, el sexo, la etnia y los
factores de riesgo tradicionales. (8,9)
Finalmente, los niveles elevados de lipoproteína(a) [Lp(a)]
se asocian independientemente con mayor riesgo cardiovascular, producto de la
activación de mecanismos aterogénicos, inflamatorios
y protrombóticos. (10)
Considerando
lo expuesto previamente, los objetivos de este estudio fueron: 1) determinar la
prevalencia de moduladores de riesgo [PAC, pCAC y el
nivel de Lp(a)] en una población en prevención
primaria estratificada inicialmente a través de un puntaje de riesgo; 2) determinar
la concordancia entre los 2 métodos de detección de ateromatosis
subclínica (PAC y pCAC); 3) establecer qué proporción
de pacientes deberían recibir estatinas según la
estratificación de riesgo inicial y luego de ser recategorizados
mediante la pesquisa de moduladores de riesgo.
MATERIAL Y MÉTODOS
El
presente es un estudio descriptivo transversal, cuya muestra se obtuvo en los
consultorios de prevención cardiovascular pertenecientes al Servicio de
Cardiología de un centro privado de salud de la Ciudad Autónoma de Buenos
Aires.
Se
incluyeron los pacientes con una edad entre 18 y 79 años, que no presentaban
enfermedad cardiovascular o tratamiento hipolipemiante
previo y que acudieron para una evaluación del riesgo cardiovascular.
Definición de las variables
Se
calculó el puntaje de riesgo (ASCVD Risk Estimator) utilizado por las guías norteamericanas para
el manejo del colesterol (American College of Cardiology/American Heart Association) en los pacientes que contaban con el rango
etario y las variables para poder aplicarlo. (11)
Los pacientes con un puntaje menor que 5%, entre 5% y 7,4%, entre 7,5% y 19,9%,
e igual o mayor que 20%, fueron clasificados como de riesgo bajo, “limítrofe”,
moderado y alto, respectivamente.
Se
cuantificó la presencia de PAC en forma no invasiva mediante ultrasonido. Se
consideró placa cuando se cumplían los siguientes requisitos: 1) espesor de la
pared anormal (espesor íntima-media >1,5 mm), 2) estructura anormal
(protrusión hacia la luz, pérdida de alineación con la pared adyacente) y 3) ecogenicidad anormal de la pared.
Se
calculó el pCAC a través de una tomografía computada multicorte, no contrastada, adquirida con gatillado
electrocardiográfico y en una apnea de aproximadamente 5-7 segundos. El calcio
coronario se identificó como una zona a nivel del vaso con un umbral de
unidades Hounsfield por encima de 130, en un área de
al menos 1 mm2. El pCAC
obtenido se expresó en unidades Agatston.
El
nivel plasmático de Lp(a) fue obtenido mediante la
técnica de nefelometría y se expresó en mg/dL. Un
valor mayor o igual a 50 mg/dL fue considerado
elevado. Se utilizaron métodos colorimétricos y turbidimétricos
para medir los niveles plasmáticos de triglicéridos, colesterol total y
colesterol HDL (C-HDL). Se utilizó la fórmula de Friedewald
para calcular el colesterol LDL (C-LDL). (12)
La tasa de filtrado glomerular se estimó mediante la ecuación CKD-Epidemiology Collaboration (CKD-EPI).
(13)
Todos los pacientes realizaron las pruebas en un único laboratorio con la misma
metodología.
Para
este estudio, y con base en las recomendaciones actuales, se consideró la
indicación de estatinas en los siguientes grupos de
pacientes en prevención primaria luego de la estratificación inicial mediante
datos clínicos y puntaje de riesgo: a) hipercolesterolemia grave (C-LDL
≥190 mg/dL); b) diabetes mellitus; c)
insuficiencia renal moderada o grave (tasa de filtrado glomerular <60 mL/min/1,73 m2); d) alto riesgo por puntaje. (11-15) Luego de conocer la
información relacionada con la presencia de moduladores de riesgo, se
consideraron además los siguientes escenarios clínicos para recomendar estatinas según diferentes guías, documentos de posición y
consensos: a) pacientes con riesgo limítrofe o moderado con pCAC
>0 (14);
b) pacientes con riesgo bajo y un pCAC ≥ 100 o pCAC ≥ al percentil 75 esperado para sexo y edad (11,15,16); c) pacientes con
riesgo bajo, limítrofe o moderado con PAC (12,13);
d) sujetos con riesgo moderado y un valor de Lp(a)
≥ 50 mg/dL(17); e)
sujetos con riesgo bajo o limítrofe y un valor de Lp(a)
≥ 75 mg/dL. (17)
Análisis estadístico
Se
exploró la normalidad de las variables analizando la media, la desviación
estándar, la mediana, la skewness, la kurtosis, un histograma y utilizando la prueba de Shapiro-Wilk. La diferencia de variables continuas entre
dos grupos se analizó con la prueba de la t si la distribución de los
datos era normal o con la prueba de Mann-Whitney-Wilcoxon si no lo era. El análisis de los datos categóricos
se realizó con la prueba de chi cuadrado.
Se
analizó la concordancia entre los dos métodos para cuantificar ateromatosis subclínica (CAC por tomografía y PAC por
ultrasonido) con el índice kappa de Fleiss. Se
definió acuerdo pobre, discreto, moderado, sustancial o casi perfecto si el
valor de kappa era menor o igual a 0,20, de entre 0,21 y 0,40, de entre 0,41 y
0,60, de entre 0,61 y 0,80 y de entre 0,81 y 1, respectivamente. 111
Las
variables continuas se expresaron como media ± desviación estándar o mediana
(rango intercuartílico 25-75) según su distribución,
mientras que las variables categóricas se expresaron como porcentajes. Se
definió estadísticamente significativo un valor de p < 0,05, utilizando
pruebas de dos colas. Para el análisis estadístico se utilizó el programa STATA
11.1.
Consideraciones éticas
El
estudio se realizó siguiendo las recomendaciones en investigación médica
sugeridas por la Declaración de Helsinki, las Guías de Buenas Prácticas
Clínicas y las normativas éticas vigentes.
RESULTADOS
Se
incluyeron en nuestro estudio 348 pacientes en prevención primaria que no
recibían tratamiento hipolipemiante. La edad media
fue 55,6 ± 12,2 años y el 45,4% eran hombres. El 8,1% y el 40,2% mostraron
antecedentes de diabetes mellitus tipo 2 o hipertensión arterial,
respectivamente. El valor medio de colesterol total fue 242,5 ± 51,9 mg/dL. Las características de la población pueden observarse
en la Tabla 1.
Tabla
1.
Características de la población incluida en el estudio.
|
Variables continuas, media ± DE o mediana (RIC) |
n = 348 |
|
Edad, años |
55,6 ± 12,2 |
|
Tensión arterial sistólica, mmHg |
130,4 ± 16,5 |
|
Índice de masa corporal, kg/m2 |
27,4 ± 5,0 |
|
Colesterol total, mg/dL |
242,5 ± 51,8 |
|
C-HDL, mg/dL |
52,5 ± 15,7 |
|
C-LDL, mg/dL |
156,7 ± 48,1 |
|
Triglicéridos, mg/dL |
140,5 (88-201,5) |
|
Apolipoproteína B, mg/dL |
126,3 ± 34,3 |
|
Creatinina, mg/dL |
0,9 ± 0,5 |
|
Puntaje de riesgo*, % |
7,3 (3,2-15,2) |
|
Variables categóricas, n (%) |
|
|
Sexo masculino |
158 (45,4) |
|
Tabaquismo activo |
49 (14,1) |
|
Diabetes mellitus tipo II |
28 (8,1) |
|
Hipertensión arterial |
140 (40,2) |
|
Obesidad |
76 (22,4) |
|
AHF |
126 (36,3) |
|
Estrato de riesgo* Riesgo bajo Riesgo
“limítrofe” Riesgo
intermedio Riesgo alto |
109 (37,9) 41 (14,2) 94 (32,6) 44 (15,3) |
AHF: antecedentes familiares de enfermedad
cardiovascular precoz; C-HDL: colesterol HDL; C-LDL: colesterol LDL; DE:
desviación estándar; RIC: rango intercuartílico
25-75.
*El puntaje utilizado fue el “ASCVD Risk Estimator” (American College of Cardiology/American Heart Association), y se pudo
calcular en 288 pacientes.
El
82,8% (n = 288) de la población tenía las características adecuadas para poder
estimar el puntaje de riesgo. Al analizar esta subpoblación, el 37,9%, 14,2%,
32,6% y 15,3% de los pacientes fueron clasificados como de riesgo bajo,
“limítrofe”, moderado o alto, respectivamente.
En
el 17,2% (n = 60) de la población no se pudo estimar el puntaje de riesgo. Los
motivos fueron: una edad menor a 40 años (n = 37), la presencia de hipercolesterolemia
grave, colesterol total >320 mg/dL, (n = 20) o
ambas condiciones (n = 3).
En
total, 29,8%, 36,8% y 53,2% de los pacientes mostraron un valor de Lp(a) ≥50 mg/dL, PAC, o un pCAC > 0, respectivamente. El 17,5% y 8,3% de los
sujetos tenía un pCAC ≥100 o ≥300,
respectivamente. Sólo 5 pacientes mostraron un pCAC
≥1000.
Los
pacientes con niveles elevados de Lp(a) mostraron
mayores valores de colesterol total, C-LDL, C-HDL y apolipoproteína
B, en comparación con los sujetos con niveles bajos. Los pacientes con PAC
tuvieron mayor edad y mostraron más frecuentemente hipertensión arterial en
comparación a los pacientes sin ateromatosis carotídea. Finalmente, los individuos con un pCAC >0 mostraron más frecuentemente la mayoría de los
factores de riesgo evaluados (incluyendo la edad, el sexo masculino, los
valores lipídicos, la obesidad, la diabetes y la hipertensión arterial) en
comparación a los pacientes con un pCAC = 0. Las
características de la población según la presencia o ausencia de los moduladores
de riesgo pueden observarse en la Tabla
2.
Tabla
2.
Características de la población según la presencia o no de los moduladores de
riesgo
|
Variables continuas,
media ± DE o mediana (RIC) |
Lp(a)
< 50 mg/dL (n = 244) |
|
Sin placa carotídea (n = 220) |
Con placa carotídea (n = 128) |
PCAC = 0 (n = 163) |
PCAC > 0 (n = 185) |
|
Edad, años |
54,3
± 13,2 |
56,5
± 12,6 |
52,6
± 12,2 |
62,4
± 11,1* |
51,2
± 12,9 |
60,6
± 11,1* |
|
Tensión
arterial sistólica, mmHg |
127,6 ± 16,8 |
130,5 ± 17,6 |
127,4 ± 15,6 |
136,1 ± 16,9* |
126,1 ± 15,9 |
134,6 ± 16,2* |
|
Índice de
masa corporal, kg/m2 |
26,9 ± 4,9 |
26,7 ± 4,0 |
27,1 ± 5,3 |
27,6 ± 4,6 |
26,1 ± 4,3 |
28,3 ± 5,4* |
|
Colesterol
total, mg/dL |
242 ± 53,4 |
271,2 ± 57,6* |
238,4 ± 47,9 |
247,2 ± 57 |
233,8 ± 40,6 |
248,4 ± 58,7* |
|
C-HDL, mg/dL |
52 ± 15,6 |
56,9 ± 16,1* |
52,6 ± 16 |
53 ± 15,3 |
55,1 ± 16,9 |
50,1 ± 14,4* |
|
C-LDL, mg/dL |
156,4 ± 47,9 |
178,6 ± 59,4* |
152,9 ± 43,6 |
160,9 ± 54 |
149,2 ± 35,9 |
161,6 ± 55,5* |
|
Triglicéridos,
mg/dL |
132,5 (83,5-194,5) |
141,5 (88-197) |
135,5 (87-207) |
145 (89-195) |
121,5 (84,5-185,5) |
152 (93-218)* |
|
Apolipoproteína B, mg/dL |
123,7 ± 35,3 |
137,5 ± 33,1* |
123,8 ± 32,2 |
128,7 ± 37,4 |
119,7 ± 27,9 |
131,2 ± 38,7* |
|
Creatinina, mg/dL |
0,92 ± 0,6 |
0,84 ± 0,2 |
0,84 ± 0,2 |
0,95 ± 0,7 |
0,85 ± 0,2 |
0,91 ± 0,6 |
|
Variables categóricas, % |
|
|
|
|
|
|
|
Sexo masculino |
47,1 |
34,4 |
44,1 |
45,9 |
37,8 |
50,8* |
|
Tabaquismo activo |
13,1 |
14,1 |
12,6 |
15,6 |
12,2 |
15,1 |
|
Diabetes mellitus tipo II |
7,2 |
7,8 |
8,1 |
7,4 |
4,3 |
10,9* |
|
Hipertensión arterial |
34,0 |
35,9 |
32,9 |
55,6* |
26,8 |
53,9* |
|
Obesidad |
22,7 |
17,5 |
23,4 |
20,9 |
15,8 |
27,9* |
|
AHF |
35,3 |
42,2 |
32,5 |
38,3 |
36,7 |
34,1 |
AHF: antecedentes familiares de enfermedad
cardiovascular precoz; C-HDL: colesterol HDL; C-LDL: colesterol LDL; DE:
desviación estándar; Lp(a): lipoproteína(a); pCAC: puntaje de calcio arterial coronario; RIC: rango intercuartílico 25-75.
*p<0,05
En
la subpoblación que pudo estratificarse mediante el puntaje de riesgo (n =
288), el 27,2% tenían niveles de Lp(a) ≥50 mg/dL, con una mediana de 25 (9,9-57,7) mg/dL.
El 55,9% y el 39,2% de los sujetos tenían un pCAC
> 0 o PAC, respectivamente. Además, en el 18,9% y el 29,6% de los pacientes
se observó un pCAC ≥100 o ≥ al percentil
75 esperado para su sexo y edad. La presencia de moduladores de riesgo en las
diferentes categorías estimadas por el puntaje de riesgo cardiovascular puede
observarse en la Figura 1.
A pesar de no tener indicación de estatinas, una
proporción importante de los sujetos de bajo riesgo (n=109) tenían moduladores
de riesgo: Lp(a) ≥50 mg/dl el 25,7%; PAC el
22%; pCAC > 0 el 33%, pCAC
≥ al percentil 75 para sexo y edad, el 33%.
En
la subpoblación que no pudo estratificarse aplicando el puntaje de riesgo por
tener una edad menor a 40 años y en los que el colesterol total era menor a 320
mg/dL (n = 37), la mediana de Lp(a)
fue 18,6 (9,8-36,3) mg/dL, el 18,9% de los pacientes
con un valor ≥ 50 mg/dL. El 8,1% y el 2,7% de
los pacientes tenían un pCAC >0 o PAC,
respectivamente, con una prevalencia total de aterosclerosis subclínica del
11%. Vale la pena destacar que en los sujetos menores de 45 años y colesterol
total <320 mg/dL (n = 60) la prevalencia de PAC
fue de 18,3% mientras que el 10% tuvieron pCAC >0
(ningún paciente mostró pCAC ≥100) . La prevalencia total de ateromatosis
subclínica en sujetos menores de 45 años fue del 23%. La representación gráfica
de la prevalencia de los moduladores del riesgo cardiovascular en dicha
subpoblación puede observarse en la Figura
2.

Fig.
1.
Prevalencia de los moduladores de riesgo en las diferentes categorías de riesgo
cardiovascular (n = 288). *p<0,05
Lp(a):
Lipoproteína(a); p75: percentil 75; pCAC: Puntaje de
calcio arterial coronario

Fig.
2.
Prevalencia de moduladores de riesgo en los pacientes con una edad menor a 45
años (n = 60).
Lp(a):
Lipoproteína(a); pCAC: Puntaje de calcio arterial coronario.
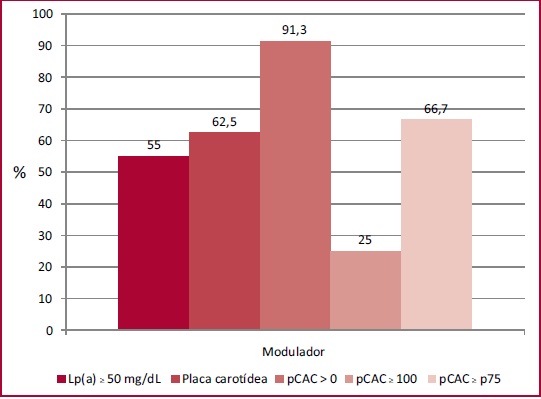
En
la subpoblación que no pudo estratificarse aplicando el puntaje de riesgo por
tener hipercolesterolemia grave (n = 23), la mediana de Lp(a)
fue 54,3 (20-72) mg/dL, el 55% de los pacientes con
un valor ≥50 mg/dL. Asimismo, el 91,3% y el
65,2% de los pacientes tenían un pCAC >0 o PAC
asociada, respectivamente. Además, el 25% y el 66,7% de los pacientes mostraron
un pCAC ≥100 o ≥al percentil 75 esperado
para su edad. La representación gráfica de la prevalencia de los moduladores
del riesgo cardiovascular en dicha subpoblación puede observarse en la Figura
3.
Fig.
3.
Prevalencia de moduladores de riesgo en los pacientes con hipercolesterolemia
severa (>320 mg/dL, n = 23).
Lp(a):
Lipoproteína(a); p75: percentil 75; pCAC: Puntaje de
calcio arterial coronario
Del
total de pacientes con PAC, el 75,8% tenía un pCAC
>0. Por otro lado, de todos los pacientes con un pCAC
>0, el 52,4% tenía PAC. La concordancia entre los dos métodos para determinar
la presencia de ateromatosis subclínica fue discreta
(kappa= 0,33), tanto en hombres (kappa = 0,35) como en mujeres (kappa = 0,30).
Por otro lado, la concordancia fue discreta (kappa = 0,29) en los sujetos con
una edad mayor o igual a 40 años y moderada (kappa = 0,45) en los pacientes más
jóvenes.
La
estratificación inicial basada en los datos clínicos y en el puntaje de riesgo
mostró que el 33% (n = 115) de la población sería candidata a recibir estatinas. Sin embargo, al considerar la presencia de
moduladores de riesgo, 110 pacientes (47,2%) que inicialmente no eran
candidatos para recibir hipolipemiantes cambiarían la
indicación (Figura 4).
Fig.
4.
Indicación de estatinas según la estratificación
inicial y luego de la pesquisa de los moduladores de riesgo. pCAC: Puntaje de calcio arterial
coronario; IRC: insuficiencia renal crónica; Lp(a):
Lipoproteína(a); PAC: placa aterosclerótica carotídea.
DISCUSIÓN
Nuestro
trabajo expone las limitaciones de estimar el riesgo cardiovascular basándonos
exclusivamente en un puntaje de riesgo, ya que muchos pacientes, jóvenes o con
un puntaje de riesgo bajo, tenían ateromatosis
subclínica o niveles elevados de lipoproteína(a).
En
nuestro estudio, no se pudo aplicar el puntaje de riesgo en 37 sujetos con una
edad menor a 40 años que no eran portadores de hipercolesterolemia grave. En
los 60 pacientes menores de 45 años, a pesar de tener disponible el resultado
del pCAC, no fue factible la evaluación del percentil
> 75 por sexo y edad, ya que los estudios epidemiológicos no reportaron los
percentiles en ese grupo etario. Contar con estos resultados es clínicamente
relevante ya que, aproximadamente, entre el 3% y el 10% de los síndromes
coronarios agudos ocurren en pacientes muy jóvenes. (18) A pesar de estos
resultados, el riesgo cardiovascular es a menudo subestimado en esta población.
Los pacientes muy jóvenes que debutan con enfermedad coronaria muestran una
alta prevalencia de sobrepeso, tabaquismo e hiperlipidemia. (19)
Nuestros datos mostraron que aproximadamente uno de cada 4 a 5 sujetos menores
a 45 años tenían ateromatosis subclínica (18% PAC,
10% pCAC>0). Hallazgos similares fueron reportados
recientemente por Razavi y col., en cuyo estudio uno
de cada diez jóvenes en la población general y uno de cada tres jóvenes con
factores de riesgo tradicionales tuvieron un pCAC elevado. (20)
Además, un estudio de cohorte, que incluyó más de 13 000 sujetos de 30 a 49
años encontró una prevalencia de pCAC >0 de 20,6%.
En el seguimiento alejado, el pCAC fue predictor independiente
de eventos vasculares y mortalidad. (21)
También, otro estudio evaluó la presencia de ateromatosis
subclínica en una población muy joven (entre 14 y 40 años). La prevalencia de
PAC fue de 5,2%, y más relevante aún, su presencia se asoció de forma
independiente con una mayor incidencia de eventos cardiovasculares y mortalidad
en el seguimiento. (22)
Por
otro lado, si bien nuestro trabajo mostró que, a mayor riesgo estimado con el
puntaje de riesgo, mayor prevalencia de ateromatosis
subclínica, un tercio de los pacientes clasificados como de “bajo riesgo”
mostraron un pCAC >0 y uno de cada 5 sujetos tenía
PAC. Similares resultados fueron reportados en estudios previos, en que entre
el 20 y 30% de los pacientes clasificados como de “bajo riesgo” por varios
puntajes mostraron PAC. (23,24)
Asimismo, en los grandes estudios poblacionales, el porcentaje de pacientes de
“bajo riesgo” que fueron reclasificados al considerar el pCAC
osciló entre 11% y 15%. (25)
Si bien los porcentajes son más bajos que los reportados en nuestro trabajo,
hay que considerar que nuestra muestra de pacientes está constituida por individuos
que consultaron para evaluar su riesgo cardiovascular, y que tenían una mayor
prevalencia de factores de riesgo en comparación a la población general.
Es
claro que los sujetos con hipercolesterolemia grave (muchos de ellos con
hipercolesterolemia familiar), los cuales no se pudieron estratificar
utilizando el puntaje de riesgo, constituyen una población de mayor riesgo
cardiovascular. Si bien la presencia de moduladores de riesgo en esta
población agrega información pronóstica, (26-29) no cambia la indicación
inicial de administrar estatinas de alta intensidad.
Nuestro trabajo mostró una alta prevalencia de moduladores de riesgo en esta
subpoblación, en coincidencia con otras publicaciones. Solo menos del 9% de los
pacientes con hipercolesterolemia grave no tenían ateromatosis
coronaria subclínica, mientras que el 65% tenía compromiso aterosclerótico de
ambos territorios.
La
evidencia actual sugiere que la estimación del pCAC
predice mejor los eventos cardiovasculares que la presencia de PAC. (30) Sin
embargo, la concordancia entre ambas determinaciones para detectar ateromatosis subclínica fue baja en nuestro trabajo. En
otras palabras, y coincidentemente con datos ya reportados por nuestro grupo,
una ecografía Doppler carotídea
“normal” no excluye la presencia de aterosclerosis subclínica coronaria y
viceversa. (31)
Además, nuestros hallazgos coinciden con los reportados por Moreyra
y col., en que la concordancia entre los territorios coronario y carotídeo en sujetos en prevención primaria fue débil
(kappa 0,21). (32)
Otro
hallazgo interesante de nuestro trabajo es que aproximadamente entre un 25 y
30% de los pacientes mostraron un nivel elevado de Lp(a)., incluyendo al subgrupo de bajo riesgo. Excepto por el
perfil lipídico, no hubo tampoco una asociación significativa entre los valores
altos de Lp(a) y los factores de riesgo tradicionales.
La asociación entre los valores elevados de Lp(a) y
el mayor riesgo de desarrollar enfermedad cardiovascular ha surgido de estudios
epidemiológicos y genéticos. (33,34)
La activación de mecanismos pro-aterogénicos, proinflamatorios y protrombóticos
explicarían la asociación de esta lipoproteína con el incremento del riesgo
cardiovascular. (35)
Recientemente, un documento de posición europeo recomienda medir la
concentración de Lp(a) al menos una vez en la vida en
la población adulta. Sin terapias específicas para reducir los niveles de Lp(a), dicho consenso recomienda contrarrestar el nivel
elevado de Lp(a) mediante el control temprano e
intensivo de los factores de riesgo, fundamentalmente el tratamiento de la
hipertensión arterial y la reducción del C-LDL. (17)
Adicionalmente,
varias guías de prevención cardiovascular recomiendan la pesquisa de ateromatosis subclínica, fundamentalmente en los pacientes
con “riesgo intermedio”, como un medio útil para reclasificar a los pacientes. (11,14, 16). El principal
objetivo de la reclasificación es identificar mejor a los pacientes que se
beneficiarán con el uso de estatinas. Las guías,
recomendaciones y consensos de lípidos también utilizan la detección de
moduladores de riesgo para recomendar metas de C-LDL y la intensidad del
tratamiento hipolipemiante. (11-16)
Nuestro trabajo mostró que un 47,2% de los sujetos que inicialmente no eran
candidatos para recibir estatinas, lo fueron al ser
reclasificados mediante la detección de moduladores de riesgo. Por lo tanto,
utilizando está modalidad híbrida de evaluación del riesgo vascular,
recomendaríamos la indicación de estatinas en el 65%
de nuestra muestra poblacional. A nuestro criterio, y considerando nuestros
resultados, la pesquisa de moduladores de riesgo debería ser considerada
también en los estratos de riesgo bajo.
Finalmente,
la estrategia de estimar el riesgo cardiovascular basada en los puntajes de
riesgo prácticamente no fue evaluada en ensayos clínicos aleatorizados.
Recientemente, un estudio mostró que la estratificación de riesgo basada en el pCAC, en comparación a una estrategia basada en el puntaje
de riesgo, puede ser más eficiente, personalizada, rentable y motivadora para
el inicio y mantenimiento de estatinas en pacientes
en prevención primaria. (36)
Si esto además se traduce en una reducción de eventos cardiovasculares se está
evaluando en un gran ensayo a largo plazo. (37)
Nuestro
estudio tiene ciertas limitaciones. Por un lado, en este trabajo sólo se
utilizó el puntaje de riesgo recomendado por las guías norteamericanas. La aplicación
de otras funciones de riesgo podría cambiar los resultados. Por otro lado, los
criterios para considerar las indicaciones de estatinas
fueron seleccionados por el grupo de investigadores, basándonos en varias guías
locales e internacionales vigentes. Finalmente, dado el diseño observacional de
nuestro trabajo, es esperable la presencia de sesgos y confundidores.
CONCLUSIÓN
La
presencia de moduladores de riesgo fue frecuente en esta población en prevención
primaria, incluso en los sujetos de bajo riesgo o en los individuos jóvenes.
Considerar la pesquisa simultánea de varios moduladores de riesgo podría
optimizar la estratificación inicial de nuestros pacientes y reconsiderar el
tratamiento con estatinas.
Declaración de conflicto de intereses
Los
autores declaran que no tienen conflicto de intereses
![]() https://creativecommons.org/licenses/by-nc-sa/4.0/
https://creativecommons.org/licenses/by-nc-sa/4.0/
©Revista Argentina de Cardiología
1. Graham IM, Di Angelantonio
E, Visseren F, De Bacquer
D, Ference BA, Timmis A, et
al. Systematic Coronary Risk Evaluation (SCORE): JACC
Focus Seminar 4/8. J Am Coll Cardiol
2021;77:3046-57. https://doi.org/10.1016/j.jacc.2021.04.052
2.
Lloyd-Jones DM, Braun LT, Ndumele CE, Smith Jr SD, Sperling LS, Virani SS, et al. Use of risk assessment tools to guide
decision-making in the primary prevention of atherosclerotic cardiovascular
disease. Circulation 2019;139:e1162–77. https://doi.org/10.1161/CIR.0000000000000638
3. Cui J.
Overview of risk prediction models in cardiovascular disease research. Ann Epidemiol 2009;19:711-7. https://doi.org/10.1016/j.annepidem.2009.05.005
4. Elosua R. Cardiovascular risk functions: usefulness and
limitations. Rev Esp Cardiol (Engl Ed) 2014; 67:77-9. https://doi.org/10.1016/j.rec.2013.09.012
5. Verma KP, Inouye M, Meikle PJ, Nicholls
SJ, Carrington MJ, Marwick TH, et al. New Cardiovascular Risk Assessment
Techniques for Primary Prevention: JACC Review Topic of the Week. J Am Coll Cardiol 2022; 80:373-87. https://doi.org/10.1016/j.jacc.2022.05.015
6. Nambi V, Chambless L, Folsom AR,
He M, Hu Y, Mosley T, et al. Carotid intima-media thickness and presence or
absence of plaque improves prediction of coronary heart disease risk: the ARIC
(Atherosclerosis Risk In Communities) study. J Am Coll Cardiol 2010;55:1600- 7. http://doi.org/cx9xd9
7. Nicolaides AN, Panayiotou AG,
Griffin MG, Tyllis T, Bond D, Georgiou N, et al.
Arterial Ultrasound Testing to Predict Atherosclerotic Cardiovascular Events. J
Am Coll Cardiol 2022;
79:1969-82. https://doi.org/10.1016/j.jacc.2022.03.352.116
8. Budoff MJ, Young R, Burke G, Carr JJ, Detrano
RC, Folsom AR, et al. Ten-year association of coronary artery calcium with
atherosclerotic cardiovascular disease (ASCVD) events: the multi-ethnic study
of atherosclerosis (MESA). Eur Heart J 2018;
39:2401-08. https://doi.org/10.1093/eurheartj/ehy217
9. Abuzaid A, Saad M, Addoumieh A, Ha LD, Elbadawi A,
Mahmoud AN, et al. Coronary artery calcium score and risk of cardiovascular
events without established coronary artery disease: a systematic review and
meta-analysis. Coron Artery Dis 2021; 32:317-28. http://dx.doi.org/10.1097/MCA.0000000000000974
10. Jawi MM, Frohlich J, Chan SY. Lipoprotein(a) the Insurgent: A New Insight into the
Structure, Function, Metabolism, Pathogenicity, and Medications Affecting
Lipoprotein(a) Molecule. J Lipids. 2020;2020:3491764. https://doi.org/10.1155/2020/3491764
11. Grundy
SM, Stone NJ, Bailey AL, Beam C, Birtcher KK, Blumenthal
RS, et al. 2018 AHA/ACC/AACVPR/AAPA/ABC/ACPM/ ADA/AGS/APhA/ASPC/NLA/PCNA
Guideline on the Management of Blood Cholesterol: A Report of the American
College of Cardiology/ American Heart Association Task Force on Clinical
Practice Guidelines. Circulation 2019;139:e1082-e1143.
https://doi.org/10.1161/CIR.0000000000000625
12. Friedewald WT, Levy RI,
Fredrickson DS. Estimation of the concentration of low-density lipoprotein
cholesterol in plasma, without use of the preparative ultracentrifuge. Clin Chem 1972;18:499-502.
13. Levey AS, Stevens LA. Estimating GFR
using the CKD Epidemiology Collaboration (CKD- EPI) creatinine
equation: More accurate GFR estimates, lower CKD prevalence estimates, and
better risk predictions. Am J Kidney 55:622-7.
Am J Kidney Dis.2010;55:622-7. https://doi.org/10.1053/j.ajkd.2010.02.337
14. Visseren FLJ, Mach F, Smulders
YM, et al. 2021 ESC Guidelines on cardiovascular disease prevention in clinical
practice. Eur Heart J. 2021;42:3227–37. https://doi.org/10.1093/eurjpc/zwab154
15. Sociedad Argentina de Cardiología.
Área de Consensos y Normas. Uso apropiado de estatinas
en Argentina: documento de posición. Rev Argent Cardiol 2018;86(Sup.1):1-13.
16.
Lloyd-Jones DM, Morris PB, Ballantyne CM, Birtcher KK, Covington AM, DePalma
SM, et al. 2022 ACC Expert Consensus Decision Pathway on the Role of Nonstatin Therapies for LDL-Cholesterol Lowering in the
Management of Atherosclerotic Cardiovascular Disease Risk: A Report of the
American College of Cardiology Solution Set Oversight Committee. J Am Coll Cardiol 2022;80:1366-418. https://doi.org/10.1016/j.jacc.2022.07.006
17. Kronenberg F, Mora S, Stroes ESG,
Ference BA, Arsenault BJ, Berglund L, et al.
Lipoprotein(a) in atherosclerotic cardiovascular disease and aortic stenosis: a
European Atherosclerosis Society consensus statement. Eur
Heart J 2022;43:3925-46. https://doi.org/10.1093/eurheartj/ehac361
18.
Davidson L, Wilcox J, Kim D, Benton S, Fredi J, Vaughan D. Clinical features of precocious acute coronary
syndrome. Am J Med 2014;127:140-4. https://doi.org/10.1016/j.amjmed.2013.09.025
19. Liu Q,
Shi RJ, Zhang YM, Cheng YH, Yang BS, Zhang YK, et al. Risk factors, clinical
features, and outcomes of premature acute myocardial infarction. Front Cardiovasc Med 2022;9:1012095. https://doi.org/10.3389/fcvm.2022.1012095
20. Razavi AC, Mortensen MB, Blaha
MJ, Dzaye O. Coronary artery calcium testing in young
adults. Curr Opin Cardiol 2023;38:32-8. https://doi.org/10.1097/HCO.0000000000001006
21. Reese
JA, Roman MJ, Deen JF, Ali T, Cole SA, Devereux RB,
et al. Subclinical atherosclerosis in adolescents and young adults and the risk
of cardiovascular disease: The Strong Heart Family Study (SHFS. Nutr Metab Cardiovasc
Dis 2022;32:1863-71. https://doi.org/10.1016/j.numecd.2022.04.024
22. Javaid A, Mitchell JD, Villines
TC. Predictors of coronary artery calcium and long-term risks
of death, myocardial infarction, and stroke in young adults. J Am Heart Assoc 2021;10(22): e022513. https://doi.org/10.1161/JAHA.121.022513
23. Coll B, Betriu A, Feinstein SB, Valdivielso JM, Zamorano JL, Fernández E. The role of carotid ultrasound
in assessing carotid atherosclerosis in individuals at low-to-intermediate
cardiovascular risk. Rev Esp Cardiol (Engl Ed) 2013;66:929-34. https://doi.org/10.1016/j.rec.2013.05.030
24. Masson W,
Lobo M, Huerín M, Molinero G, Manente
D, Pángaro M, et al. Estratificación del riesgo
cardiovascular con diferentes puntajes de riesgo en prevención primaria y sus
implicaciones en la indicación de estatinas. Rev Argent Cardiol 2014;82:480-6. http://dx.doi.org/10.7775/rac.es.v82.i6.4527
25. Lluberas N.
Score de calcio coronario en la estratificación de riesgo cardiovascular. Rev Urug Cardiol
2019;34:341-8. https://doi.org/10.29277/cardio.34.3.23
26. Bea AM, Civeira
F, Jarauta E, Lamiquiz-Moneo
I, Pérez-Calahorra S, Marco-Benedí V, et al. Association Between the
Presence of Carotid Artery Plaque and Cardiovascular Events in Patients With
Genetic Hypercholesterolemia. Rev Esp
Cardiol (Engl Ed). 2017;70:551-8. https://doi.org/10.1016/j.rec.2017.01.023
27. Gallo A, Pérez de Isla L, Charrière S, Vimont A, Alonso R,
Muñiz- Grijalvo O, et al. The Added Value of Coronary Calcium Score in
Predicting Cardiovascular Events in Familial Hypercholesterolemia. JACC Cardiovasc Imaging 2021;14:2414-24. https://doi.org/10.1016/j.
jcmg.2021.06.011
28. Alonso R, Andrés E, Mata N,
Fuentes-Jiménez F, Badimón L, López-Miranda J, et al.
Lipoprotein(a) levels in familial hypercholesterolemia: an
important predictor of cardiovascular disease independent of the type of LDL
receptor mutation. J Am Coll Cardiol.
2014;63:1982-9. https://doi.org/10.1016/j.jacc.2014.01.063
29. Mattina A, Giammanco A, Giral P, Rosenbaum D, Carrié A, Cluzel P, et al. Polyvascular
subclinical atherosclerosis in familial hypercholesterolemia: The role of
cholesterol burden and gender. Nutr Metab Cardiovasc Dis. 2019;29:1068-76. https://doi.org/10.1016/j.numecd.2019.06.015
30. Gepner AD, Young R, Delaney JA, Tattersall MC, Blaha MJ, Post WS, et al. Comparison of coronary artery
calcium presence, carotid plaque presence, and carotid intima-media thickness
for cardiovascular disease prediction in the Multi-Ethnic Study of
Atherosclerosis. Circ Cardiovasc
Imaging 2015;8:e002262. https://doi.org/10.1161/CIRCIMAGING.114.002262
31. Siniawski D,
Masson W, Bluro I, Falconi M, Pérez De Arenaza D, De Stefano L, et al.
Precisión diagnóstica del espesor íntima-media carotídeo
para la detección de aterosclerosis coronaria. Utilidad en la práctica clínica.
Rev Argent Cardiol 2013;81:136-43. http://dx.doi.org/10.7775/rac.es.v81.i2.2114
32. Moreyra E Jr, Moreyra C, Tibaldi MA, Crespo F, Arias V, Lepori
AJ, et al. Concordance and
prevalence of subclinical atherosclerosis in different vascular territories. Vascular 2020;28:285-294. http://dx.doi.org/10.1177/1708538119894178
33. Forbes
CA, Quek RG, Deshpande S,
Worthy G, Wolff R, Stirk L, et al. The relationship
between Lp(a)
and CVD outcomes: a systematic review. Lipids Health Dis 2016;15:95.
https://doi.org/10.1186/s12944-016-0258-8
34. Saleheen D, Haycock PC, Zhao W, Rasheed
A, Taleb A, Imran A, et al. Apolipoprotein(a)
isoform size, lipoprotein(a) concentration, and coronary artery disease: A mendelian randomisation analysis.
Lancet Diabetes Endocrinol 2017;5:524-33.
https://doi.org/10.1016/S2213-8587(17)30088-8
35. Kamstrup PR. Lipoprotein(a) and
Cardiovascular Disease. Clin Chem
2021;67:154-66. https://doi.org/10.1093/clinchem/hvaa247
36. Muhlestein JB, Knowlton KU, Le VT, Lappe
DL, May HT, Min DB, et al. Coronary Artery Calcium Versus Pooled Cohort
Equations Score for Primary Prevention Guidance: Randomized Feasibility Trial. JACC
Cardiovasc Imaging 2022;15:843-55.
https://doi.org/10.1016/j.jcmg.2021.11.006
37. Effectiveness
of a Proactive Cardiovascular Primary Prevention Strategy, With or Without the
Use of Coronary Calcium Screening, in Preventing Future Major Adverse Cardiac
Events (CorCal). Acceso el
11/01/2023 desde: https://clinicaltrials.gov/ct2/show/NCT03439267