INTRODUCCIÓN
Los dispositivos cardíacos electrónicos implantables (DCEI), como los desfibriladores automáticos implantables (DAI) y los dispositivos de terapia de resincronización cardíaca con desfibrilador (TRC-D), constituyen una piedra angular en el tratamiento de pacientes con riesgo de muerte súbita cardíaca y aquellos con insuficiencia cardíaca avanzada. (1) Estos dispositivos no solo entregan terapias que salvan vidas, sino que también funcionan como herramientas diagnósticas sofisticadas y permiten recopilar continuamente gran cantidad de datos sobre el ritmo cardíaco y parámetros fisiológicos del paciente.
En la última década, la monitorización remota (MR) ha revolucionado el seguimiento de esta población de pacientes, pasando de ser una tecnología complementaria a un estándar de cuidado recomendado por las principales guías de práctica clínica internacionales. (2-4) La MR permite la transmisión automática y programada de datos desde el dispositivo del paciente hasta un centro de seguimiento, facilitando una vigilancia continua y proactiva. Se ha demostrado de manera consistente que la MR reduce el tiempo hasta la detección de eventos clínicos y técnicos accionables, como arritmias auriculares y ventriculares, o disfunciones de electrodos. (5-7) Además, ha probado ser efectiva en reducir la incidencia de choques inapropiados del DAI y disminuir la necesidad de visitas presenciales de rutina, optimizando así los flujos de trabajo clínico y mejorando la conveniencia para el paciente. (8,9)
A pesar de estos beneficios establecidos, el impacto de la MR en los resultados clínicos “duros”, como la mortalidad por todas las causas y las hospitalizaciones, ha sido un área de intenso debate con resultados heterogéneos en la literatura. Mientras que algunos estudios observacionales y ensayos clínicos han sugerido una asociación entre la MR y una mejor supervivencia, (10-12) otros ensayos controlados aleatorizados de gran escala y metaanálisis han reportado hallazgos neutros, sin demostrar un beneficio claro en estos puntos finales primarios. (13-15) Esta discrepancia resalta la importancia de la evidencia generada en el “mundo real”, que refleja la práctica clínica habitual en poblaciones de pacientes más diversas y complejas que las típicamente incluidas en los ensayos clínicos.
Las arritmias ventriculares, que van desde taquicardia ventricular no sostenida (TVNS) hasta taquicardias ventriculares sostenidas (TV) y fibrilación ventricular (FV), son eventos frecuentemente detectados por la MR en pacientes con DAI/TRC-D. La aparición de estas arritmias no solo desencadena terapias del dispositivo, sino que también puede ser un marcador de progresión de la cardiopatía subyacente y un indicador de mal pronóstico. (16) Por lo tanto, comprender la incidencia de estas alertas y su asociación con resultados a largo plazo como la supervivencia es de suma importancia clínica.
El objetivo de este estudio fue doble: primero, caracterizar demográfica y clínicamente a nuestra cohorte de pacientes portadores de DAI y TRC-D bajo seguimiento con MR en un entorno de práctica habitual en Argentina; y segundo, evaluar el valor pronóstico de la aparición de alertas por arritmias ventriculares (TV, FV o TVNS) sobre la supervivencia por todas las causas en esta población.
MATERIAL Y MÉTODOS
Se realizó un estudio de cohorte, descriptivo y retrospectivo, en un hospital de población cerrada de la Ciudad Autónoma de Buenos Aires. Se construyó una base de datos a partir de los registros de pacientes con DCEI. Para el presente análisis, se seleccionaron todos los pacientes portadores de un DAI o un TRC-D, cuyo implante se realizó entre agosto de 2018 y enero de 2025, y que contaban con un sistema de MR activo. Los criterios de exclusión fueron: 1) pacientes con dispositivos que no fueran DAI o TRC-D, 2) seguimiento documentado menor a 6 meses y 3) datos incompletos en variables clave como la fecha de implante o el estado vital al final del seguimiento. La cohorte final para el análisis consistió en 62 pacientes que cumplieron con todos los criterios.
Los datos se obtuvieron de dos fuentes principales, vinculadas a través de un identificador único de paciente: una base de datos de gestión de pacientes y un registro sistemático de las alertas recibidas a través de las plataformas de MR.
Se extrajeron las siguientes variables basales: edad al momento del implante, sexo, tipo de dispositivo (DAI vs. TRC-D), historia de fibrilación auricular (FA) previa al implante, uso de anticoagulación basal, y comorbilidades como hipertensión arterial, diabetes mellitus, diagnóstico de insuficiencia cardíaca y enfermedad renal crónica. Fármacos como los inhibidores del cotransporte sodio-glucosa tipo 2 no se analizaron, dado que un número significativo de pacientes inició su seguimiento en la cohorte previo a la publicación de los trabajos que establecieron su uso como estándar de cuidado. Los inhibidores duales de angiotensina-neprilisina tampoco se incluyeron en el análisis basal, ya que estos datos no se recolectaron de forma sistemática en la base de datos retrospectiva.
Para el seguimiento, se registraron la fecha de implante del dispositivo, la fecha del último control o de fallecimiento, y el estado vital. A partir de estas fechas, se calcularon el tiempo de seguimiento y el tiempo de supervivencia en días para cada paciente.
Se analizaron todas las alertas transmitidas y clasificadas por el dispositivo como TVNS, TV o FV. Para cada alerta, se documentó si el evento fue sintomático y si generó una consulta no programada. La respuesta del dispositivo a la alerta fue categorizada como “Monitor”, “ATP” (terapia de estimulación anti taquicárdica) o “Choque”. El manejo clínico subsecuente fue categorizado como “Ajuste farmacológico”, “Ajuste de programación por choque inapropiado”, u otros. Se creó una variable dicotómica para clasificar a los pacientes en dos grupos: aquellos que presentaron al menos una de estas alertas durante el seguimiento y aquellos que no.
La programación basal estándar utilizada para las alertas siguió las recomendaciones de las guías internacionales para la reducción de terapias inapropiadas. (17) Se estableció una zona de monitoreo de TV, con un corte de detección de intervalo de 340 ms (> 176 lpm) y un contador de 28 intervalos para la detección. En esta zona se programaron activos los discriminadores de inicio súbito (Onset 20 %), Estabilidad (48 ms) y discriminadores de morfología. La zona de terapia (FV) se programó con un intervalo de 320 ms (> 188 lpm) y un contador de 18 sobre 24 intervalos para la detección, con terapias de ATP (Ráfaga) seguido de choques.
Se aclara que esta era la programación basal; en pacientes de prevención secundaria o tras un episodio, esta programación podía ser individualizada. Sin embargo, estos valores se utilizaron como los criterios mínimos para definir los eventos.
Con esta programación, las 40 alertas analizadas se clasificaron como: Alertas de TVNS (n=4), definidas como episodios no sostenidos (p.ej., duración menor a los 28 latidos) que solo generaron una alerta de ‘Monitor’; y Alertas de TV/FV (n=36), definidas como episodios sostenidos que alcanzaron el contador de detección en la zona de terapia y recibieron ATP o Choque.
La totalidad de las 40 alertas analizadas fueron confirmadas manualmente por un electrofisiólogo del staff para validar su origen ventricular y excluir artefactos o taquicardias supraventriculares.
Análisis estadístico
Se aplicó estadística descriptiva para resumir las características de la cohorte. Las variables continuas se presentaron como media y mediana con sus rangos. Las variables categóricas se expresaron como frecuencias absolutas (n) y porcentajes ( %).
Para comparar las características basales entre el grupo de pacientes con alertas y sin alertas, se utilizó la prueba exacta de Fisher para todas las variables categóricas. Para la comparación de la variable continua “Edad al Implante”, que no seguía una distribución normal, se utilizó la prueba de U de Mann-Whitney.
Para el análisis de supervivencia, se definió el evento de interés como la mortalidad por todas las causas. El tiempo hasta el evento se calculó desde la fecha de implante del dispositivo hasta la fecha de fallecimiento o la fecha del último seguimiento. Se utilizó el método de Kaplan-Meier para estimar y visualizar las probabilidades de supervivencia a lo largo del tiempo para cada grupo. Se empleó la prueba de Log-Rank para comparar formalmente las curvas de supervivencia.
Un valor de p < 0,05 fue considerado estadísticamente significativo. Todos los análisis se realizaron utilizando R versión 4.4.2 (R Foundation for Statistical Computing, Viena, Austria).
Consideraciones éticas
El estudio fue conducido en adhesión a los principios de la Declaración de Helsinki. (18) Se garantizó la confidencialidad de los datos mediante la anonimización de la base de datos final. Todos los pacientes habían otorgado un consentimiento informado al inicio de la monitorización remota, autorizando el uso de sus datos para fines de investigación. Dado el carácter retrospectivo y anonimizado del análisis, el estudio fue considerado exento de necesidad de aprobación específica por parte del comité de ética institucional.
RESULTADOS
Características basales de la cohorte
Se incluyeron en el análisis un total de 62 pacientes portadores de DAI o TRC-D. Las características demográficas y clínicas basales de la cohorte se resumen en la Tabla 1. La edad promedio al implante fue de 61,8 años (mediana 64; rango 16-87). La población fue predominantemente de sexo masculino (47 pacientes, 75,8 %). El tiempo de seguimiento promedio fue de 2,61 años (mediana 2,2 años; rango 0,6-7,2).
Tabla 1
Características basales de la cohorte de pacientes con DAI/TRC-D (N=62)
| Característica | Valor (N=62) |
|---|---|
| Edad al Implante (años) | |
| - Mediana (RIC) | 64,8 (55,8-73,8) |
| - Rango (Mín-Máx) | 16-87 |
| Sexo, n (%) | |
| - Hombres | 47 (75,8%) |
| - Mujeres | 15 (24,2%) |
| Tipo de Dispositivo, n (%) | |
| - DAI solo | 49 (79,0%) |
| - TRC-D | 13 (21,0%) |
| Comorbilidades Basales, n (%) | |
| - FA Previa al Implante | 7 (11,3%) |
| - Anticoagulación Basal | 13 (21,0%) |
| - Insuficiencia Cardíaca | 41 (66,1%) |
| - Hipertensión Arterial (HTA) | 53 (85,5%) |
| - Diabetes Mellitus | 19 (30,6%) |
| - Enfermedad Renal Crónica | 16 (25,8%) |
| FEVI (mediana, RIC) | 30% (22-34) |
| Etiología, n (%) | |
| - Isquémica | 19 (30,6%) |
| - No isquémica | 42 (67,7%) |
| Clase Funcional (NYHA), n (%) | |
| - NYHA I | 45 (72,6%) |
| - NYHA II-IV | 17 (27,4%) |
| Medicación Basal, n (%) | |
| - Betabloqueantes | 55 (88,7%) |
| - Bloqueo SRAA | 49 (79,0%) |
| - ARM | 39 (62,9%) |
| - Amiodarona | 31(50,0%) |
| Tiempo de Seguimiento (años) | |
| - Mediana (RIC) | 2,2 (1.2 - 3.6) |
| - Rango (Mín-Máx) | 0,6-7,2 |
ARM: Antagonista de los receptores mineralocorticoides; DAI: defibrilador automático implantable; FA: fibrilación auricular; FEVI: fracción de eyección ventricular izquierda; NYHA: New York Heart Association; RIC: rango intercuartílico; SRAA: Sistema renina angiotensina aldosterona; TRC-D: terapia de resincronización cardíaca con desfibrilador
Incidencia y manejo de alertas de arritmias ventriculares
Durante el período de seguimiento, 22 de los 62 pacientes (35,5 %) presentaron un total de 40 alertas por arritmias ventriculares (TV, FV o TVNS). De estas 40 alertas, 15 (37,5 %) fueron sintomáticas y 17 (42,5 %) motivaron una consulta no programada.
La respuesta del dispositivo asociada a estas alertas fue: solo monitorización en 4 casos (10 %), terapia con ATP en 11 (27,5 %), y terapia con choque en 25 (62,5 %). El manejo clínico documentado tras las alertas consistió en ningún cambio en 24 casos (60 %), ajuste farmacológico en 11 (27,5 %), ajuste de programación en 4 (10 %) y derivación para ablación en 1 (2,5 %). Es de destacar que, de los 25 choques, 3 (12 %) fueron seguidos de una reprogramación por ser considerados inapropiados. El detalle del manejo según la respuesta del dispositivo se resume en la Tabla 2.
Tabla 2
Manejo clínico según la respuesta del dispositivo a las alertas de arritmias ventriculares (N=40 alertas)
| Respuesta del Dispositivo | Ajuste Farmacológico | Ajuste Programación | Ablación | Sin Cambio | Total Alertas |
|---|---|---|---|---|---|
| Monitor | 0 | 0 | 0 | 4 | 4 |
| ATP | 2 | 1 | 0 | 8 | 11 |
| Choque | 9 | 3* | 1 | 12 | 25 |
| Total | 11 | 4 | 1 | 24 | 40 |
*Corresponde a "Choque_Inapropiado_Ajuste_Programacion"
ATP: marcapaseo antitaquicardia
Análisis comparativo de subgrupos
Se compararon las características basales de los pacientes que presentaron alertas de arritmias ventriculares (n=22) versus aquellos que no (n=40), como se detalla en la Tabla 3. Se observó tendencia hacia una mayor edad (mediana 67 vs. 62 años; p=0,063) y mayor prevalencia de hipertensión arterial (95,5 % vs. 77,5 %; p=0,082) en el grupo con alertas. La fracción de eyección ventricular izquierda (FEVI) fue significativamente menor en el subgrupo con alertas, y la prevalencia de insuficiencia cardíaca mayor. (Tabla 3) El hallazgo más relevante fue la asociación estadísticamente significativa entre la aparición de alertas ventriculares y una mayor mortalidad por todas las causas (40,9 % vs. 7,5 %; p=0,003), con un odds ratio de 8,54 (IC 95 % 2,05-41,5, p= 0,003).
Tabla 3
Comparación de características basales entrepacientes con y sin alertas de arritmias ventriculares
| Característica Basal | Pacientes con Alertas (N=22) | Pacientes sin Alertas (N=40) | Valor p |
|---|---|---|---|
| Edad al Implante (años, mediana) | 67 | 62 | 0,063 |
| Sexo masculino | 86,4% | 70,0% | 0,218 |
| TRC-D | 31,8% | 15,0% | 0,191 |
| FA previa al implante | 13,6% | 10,0% | 0,691 |
| Insuficiencia cardíaca | 77,3% | 60,0% | 0,262 |
| Hipertensión arterial | 95,5% | 77,5% | 0,082 |
| Diabetes Mellitus | 22,7% | 35,0% | 0,395 |
| Enf. renal crónica | 31,8% | 22,5% | 0,546 |
| FEVI (% mediana) | 28,5 | 38 | 0,003 |
| Etiología isquémica | 45,5% | 22,5% | 0,085 |
| NYHA II-IV | 54,5% | 12,5% | 0,005 |
| Betabloqueantes | 95,5% | 85,0% | 0,371 |
| Bloqueo SRAA | 100% | 67,5% | 0,002 |
| ARM | 86,4% | 50,0% | 0,005 |
| Amiodarona | 50,0% | 50,0% | 1,000 |
ARM: antagonistas de los receptores mineralocorticoides; FA: fibrilación auricular; FEVI: fracción de eyección ventricular izquierda; NYHA: New york Heart Association; SRAA: sistema renina angiotensina aldosterona; TRC-D: terapia de resincronización cardíaca con desfibrilador
Análisis de supervivencia
Para evaluar el impacto pronóstico de la aparición de alertas de arritmias ventriculares sobre la mortalidad por todas las causas, se realizó un análisis de supervivencia utilizando el método de Kaplan-Meier. Se comparó la supervivencia a lo largo del tiempo entre el grupo de pacientes que presentó al menos una alerta por TV, FV o TVNS (n=22) y el grupo que no presentó dichas alertas (n=40).
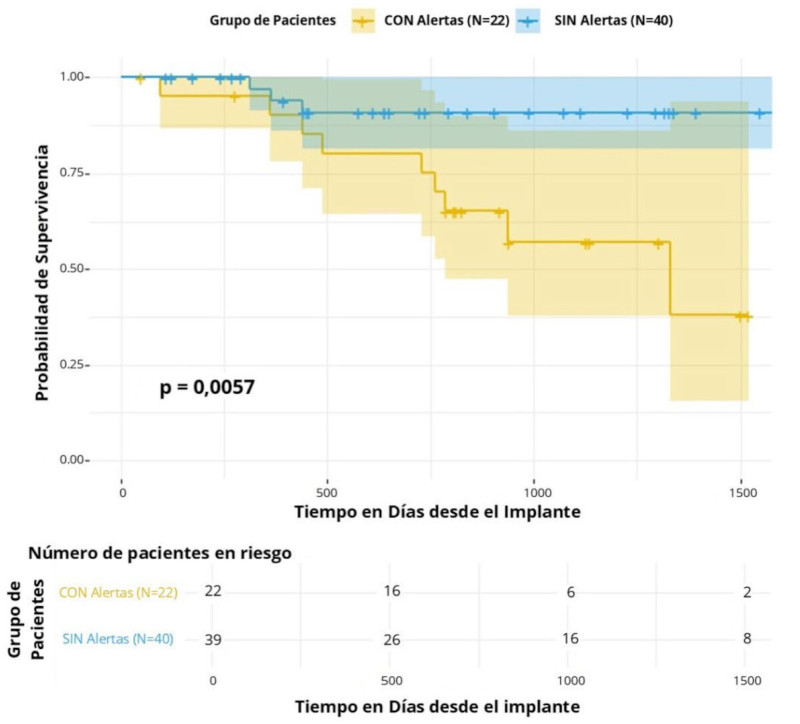
La Figura 1 muestra las curvas de supervivencia para ambos grupos. Se observó una separación clara y temprana de las curvas, con probabilidad de supervivencia consistentemente menor a lo largo del tiempo en el grupo de pacientes con alertas en comparación con el grupo sin alertas.
La prueba de Log-Rank confirmó que esta diferencia en la supervivencia fue altamente estadísticamente significativa (p = 0,006). Para ajustar por la duración heterogénea del seguimiento (rango 0,6-7,2 años), se calculó la mortalidad anualizada por grupo. Esta fue marcadamente superior en el grupo con alertas (18,33 muertes por 100 personas-año) comparado con el grupo sin alertas (2,74 muertes por 100 personas-año).
Estos hallazgos indican que la aparición de alertas por arritmias ventriculares, detectadas por monitorización remota, fue un fuerte predictor de un aumento en la mortalidad en nuestra cohorte de pacientes con DAI/TRC-D.
DISCUSIÓN
Este estudio del mundo real caracteriza a una cohorte de pacientes con DAI/TRC-D y demuestra que la aparición de alertas por arritmias ventriculares detectadas por MR es un potente marcador de mal pronóstico. El hallazgo principal de nuestro trabajo es la asociación estadísticamente significativa entre la presencia de alertas por TV, FV o TVNS y un aumento en la mortalidad por todas las causas. El análisis de supervivencia de Kaplan-Meier no solo confirma este hallazgo, sino que también permite visualizar cómo el riesgo diverge a lo largo del tiempo, con una separación notable de las curvas después de los 500 días.
Este resultado alinea nuestra experiencia con la de otros estudios que han identificado a las arritmias ventriculares como un factor de riesgo independiente para la mortalidad en esta población. (16,19) La capacidad de la MR para detectar estos eventos de forma temprana es, por lo tanto, crucial no solo para el manejo inmediato de la arritmia, sino también para la estratificación del riesgo a largo plazo. Es relevante contextualizar nuestros hallazgos con los de grandes estudios internacionales, aunque con diferencias en sus objetivos. A diferencia de ensayos aleatorizados como el REM-HF (9) o estudios como REMOTE-CIED, (14) que reportaron hallazgos neutrales sobre el impacto de la MR en la mortalidad por todas las causas, nuestro estudio no evalúa la MR per se, sino el valor pronóstico de las alertas detectadas. En este sentido, nuestros resultados se alinean con los de grandes registros observacionales, como el estudio ALTITUDE, (11) que sí sugirió una asociación entre la monitorización remota y una mejor supervivencia. (20) La diferencia de casi siete veces en la tasa de mortalidad ajustada por tiempo de exposición refuerza el hallazgo de la curva de Kaplan-Meier y sugiere que la asociación entre las alertas ventriculares y un peor pronóstico es robusta, y no un mero artefacto del seguimiento diferencial. (21)
La capacidad de la MR para identificar tempranamente a pacientes de alto riesgo, como aquellos con arritmias ventriculares, sigue siendo un valor clínico fundamental. Un paciente que presenta estas alertas podría ser candidato a una intensificación de la terapia para la insuficiencia cardíaca, una reevaluación de la terapia antiarrítmica, o la consideración de terapias más avanzadas como la ablación.
Somos conscientes de las limitaciones de nuestro estudio. Su diseño retrospectivo y observacional no permite establecer causalidad, sino únicamente asociación. El tamaño de la cohorte es modesto (n=62), lo que restringe la potencia estadística.
La principal limitación es la ausencia de un análisis multivariado (p.ej., regresión de Cox) para ajustar por factores de confusión evidentes. Como muestra el análisis comparativo (Tabla 3), el grupo que presentó alertas tenía un perfil de riesgo basal significativamente mayor: una FEVI mediana marcadamente más baja, mayor prevalencia de etiología isquémica , una proporción mucho mayor de pacientes sintomáticos según la clasificación funcional de la New York Heart Association (NYHA II-IV) y un uso más elevado de medicación para la insuficiencia cardíaca (como antagonistas de los receptores mineralocorticoides y bloqueo del sistema renina angiotensina aldosterona.
Aunque se consideró un análisis de Cox, dado el bajo número de eventos de mortalidad en la cohorte (n=12), intentar ajustar por múltiples confundidores resultaría en un sobreajuste (overfitting) del modelo, generando resultados estadísticamente inestables y poco fiables. Por lo tanto, el odds ratio informado para la mortalidad probablemente sobreestima la asociación real, ya que es un cálculo no ajustado.
CONCLUSIÓN
En conclusión, en nuestra cohorte, la aparición de alertas de monitorización remota por arritmias ventriculares fue un hallazgo frecuente y se asoció de manera significativa como marcador pronóstico con una menor supervivencia. Este hallazgo subraya el valor pronóstico de la información obtenida a través de la MR y su importancia para la estratificación de riesgo y la toma de decisiones clínicas en pacientes con desfibriladores implantables.
Declaración de conflicto de interés
Los autores declaran no tener conflicto de intereses. (Véase formularios de conflictos de interés de los autores en la Web).