http://dx.doi.org/10.7775/rac.es.v91.i1.20592
ARTÍCULO
DE REVISIÓN
Efecto del alcohol sobre el corazón y el
sistema cardiovascular: hipertrofia, remodelamiento y
disminución del strain. Información actual
Alcohol
Impact on the Heart and Cardiovascular System - Hypertrophy, Remodeling and
Strain Impairment - Contemporary State-of-the-Art
Piotr
Hamala1, Karina Wierzbowska-Drabik2
1
Primer Departamento y Cátedra de
Cardiología, Medical University of Lodz, Lodz, Polonia
2
Departamento de Medicina Interna y
Farmacología Clínica, Medical University of Lodz, Lodz, Polonia
Dirección
para separatas: Piotr Hamala. E-mail: piotrhamala@gmail.com
RESUMEN
Datos recientes muestran que el abuso crónico de alcohol puede
conducir a disfunción cardiovascular, a partir de dosis de etanol
tradicionalmente consideradas bajas, y que la aparición de arritmias,
incluyendo la fibrilación auricular, aumenta aún en consumidores de alcohol
moderados.
Los otros mecanismos comunes del impacto negativo del etanol están
relacionados con el desarrollo de hipertensión y su consecuencia directa, la
hipertrofia, fibrosis y disfunción diastólica.
Debido a que la probabilidad de reversibilidad del remodelamiento cardíaco depende de un diagnóstico temprano
de disfunción cardíaca, se debería recomendar la aplicación más amplia de
métodos nuevos y más sensibles de evaluación de la función miocárdica,
incluyendo el strain longitudinal
ventricular izquierdo y derecho, así como de los protocolos adaptados a la
ecocardiografía de estrés.
Palabras clave: Etanol - Consumo de bebidas alcohólicas/Efectos Adversos -
Cardiomiopatía Alcohólica - Miocardiopatía Tóxica
ABSTRACT
The recent data show that chronic overuse
of alcohol may lead to cardiovascular dysfunction, starting from traditionally
judged as low ethanol doses, and that the burden of arrhythmias, including
atrial fibrillation, increases even in moderate alcohol consumers.
The other common mechanisms of the
disadvantageous impact of ethanol are related to the development of
hypertension and its direct aftermath, hypertrophy, fibrosis, and diastolic
dysfunction.
Since the chance of the reversibility of
cardiac remodeling depends on the early diagnosis of cardiac dysfunction, the
wider application of novel and sensitive methods of myocardial function
assessment, including longitudinal strain of the left and right ventricles, as
well as the adapted protocols for stress echocardiography, should be
recommended.
Key words:
Ethanol - Alcohol Drinking/Adverse Effects - Alcoholic Cardiomyopathy - Toxic
cardiomyopathy
1. Introducción
Según
información reciente de la Organización Mundial de la Salud (OMS), el 49% de la
población mundial adulta consume alcohol. En Europa, este valor es aún más
elevado, y alcanza el 60%. Las enfermedades relacionadas al alcohol son:
arritmias cardíacas, especialmente fibrilación auricular, miocardiopatía
alcohólica, hipertensión, accidente cerebrovascular, epilepsia, depresión,
esteatosis y cirrosis hepática, así como pancreatitis y numerosos cánceres. En
etapas tempranas, se cree que el daño miocárdico relacionado con el alcohol es
reversible luego de cesar de beber, pero los predictores de reversibilidad no
están bien definidos. De manera similar, la cantidad exacta de alcohol
recomendada para que todavía sea segura para la salud cambia de acuerdo a las
diferentes personas, su sexo, edad, y estado general y cardiovascular. Sin
embargo, el conocimiento en este campo se ha ampliado considerablemente
recientemente con estudios que proporcionan asociaciones entre datos clínicos y
de laboratorio, la cantidad de alcohol consumida y nuevos parámetros ecocardiográficos que describen la morfología y la función
del corazón. Esta revisión repasa brevemente los efectos epidemiológicos y
fisiopatológicos del exceso de alcohol, y resume los datos actuales respecto
del impacto del consumo de alcohol sobre la función del sistema cardiovascular
y el corazón.
2.1 Epidemiología del
consumo de alcohol
De acuerdo con el informe de la OMS de 2018, aproximadamente 2,4
mil millones de personas en el mundo beben alcohol, 43% de la población adulta
de más de 15 años. (1) El mayor consumo de alcohol
corresponde a Europa, donde alcanza al 60% de la población. La segunda región
con consumo más elevado de alcohol es América del Norte y del Sur, con 54%. En
comparación, el uso de tabaco se estima en una amplia escala en 1,33 mil
millones (22%) a través del mundo. (2)
El consumo de alcohol mundial, presentado como litros de etanol
puro per cápita [alcohol puro per capita (APC) por
año, que incluye a personas >15 años], ha ido en aumento desde el año 2000.
Según el informe de la OMS mencionado, el APC alcanzó 5,7 litros en el año 2000
y subió a 6,4 litros en 2016. Es de notar que simultáneamente con el incremento
del índice de APC, el número de bebedores de alcohol disminuyó en
aproximadamente 683 millones. (1)
En cuanto a la diferencia entre sexos respecto del consumo de
alcohol, el 69% de los hombres y el 50% de las mujeres beben alcohol en Europa,
mientras en América del Norte y Sur, el 67% de los hombres y el 42% de las
mujeres consumen alcohol. (1)
2.2 Impacto del alcohol
sobre la salud
Los factores genéticos pueden tener influencia sobre el nivel de
consumo de alcohol, así como sobre la tolerancia al etanol. Holmes y
colaboradores investigaron un grupo de 260 000 personas para evaluar el impacto
de la mutación rs 1229984 en el gen que codifica la
enzima alcohol deshidrogenasa 1B (ADH1B) sobre el comportamiento frente a la
bebida. Esta mutación parece estar relacionada con un comportamiento específico
de beber, caracterizado por la tendencia a consumir menores volúmenes de
alcohol (17% menor en comparación con el grupo sin la mutación). Debido a que
los portadores de esta mutación estuvieron expuestos a síntomas más severos
asociados al metabolismo del alcohol, al limitar la cantidad de etanol
consumido, mostraron luego menor riesgo de complicaciones relacionadas al
alcohol. En este estudio, el riesgo menor de enfermedad isquémica se observó en
el grupo con dicha mutación [Odds Ratio (OR) 0,90 e
intervalo de confianza del 95% (IC95%) 0,84-0,96]. (3)
No obstante, se ha postulado el efecto beneficioso del consumo
bajo o moderado de alcohol sobre el cuerpo humano. El efecto beneficioso se ha
vinculado con la reducción documentada del comienzo de enfermedad isquémica,
accidente cerebrovascular y diabetes. (1) En un metaanálisis realizado por el Dr. Castelnuovo
y colaboradores en 209 418 pacientes, se observó reducción del riesgo
cardiovascular [riesgo relativo (RR) 0,68, IC95% 0,59-0,77] en el grupo que
consumía 150 ml de vino por día, en comparación con los totalmente abstemios. (4) El efecto beneficioso del vino y la cerveza se asoció
con la presencia de ingredientes específicos pertenecientes a los polifenoles, tales como el resveratrol,
cuyo efecto molecular está basado en liberar señales de monitoreo como el
factor nuclear derivado de eritroide 2, similar al
factor 2 en el vitíligo (Nrf2), el factor nuclear potenciador de las
cadenas ligeras kappa de las células B activadas (NF-κΒ),
sirtuina-1 deacetilasa dependiente de NAD (Sirt1),
5’proteína quinasa activada por AMP (AMPK), así como la reducción del estrés
oxidativo y la apoptosis, como se observó en estudios experimentales. (5,6) En un metaanálisis que
incluyó 1 902 605 participantes, dosis bajas de alcohol (10-14 gramos por día)
indujeron un 18% de reducción sobre el comienzo de la diabetes en mujeres. (7) El mecanismo postulado de este efecto fue la mayor
sensibilidad a la insulina relacionada con el consumo de alcohol. La variedad
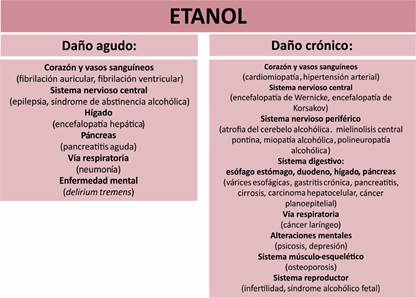
de impactos dañinos del alcohol sobre el cuerpo humano se presentan en la Figura 1. (1,8,9)
Fig. 1. Órganos blanco del impacto
tóxico del alcohol
2.3 Metabolismo del
alcohol
Dos enzimas: alcohol-deshidrogenasa (ADH) y el citocromo P450 2E1 (CYP450)
están involucradas en la vía principal del metabolismo del alcohol. El producto
intermedio de esta reacción es el acetaldehído, responsable de la influencia
tóxica sobre el cuerpo humano. Luego, el acetaldehído es convertido por la acetaldehído deshidrogenasa y la acetaldehído oxidasa en
ácido acético, que entra en el ciclo de Krebs. Una cierta cantidad de
acetaldehído deja el hígado y es dirigida a los tejidos periféricos, donde es
metabolizado a acetil-coenzima A (acetil-CoA), así
como a colesterol, esteroides, ácidos grasos, cuerpos cetónicos
y CO2 (Figura 2). El metabolismo del alcohol comienza en la mucosa
gástrica, cuyas células contienen ADH. Luego de su absorción en el sistema
gastrointestinal a través de la vena porta, el alcohol es dirigido a los
hepatocitos, donde tiene lugar la mayor parte del metabolismo, ya que el
citoplasma, mitocondrias y microsomas de los
hepatocitos contienen las cantidades más elevadas de ADH y CYP450. (10) Una gran variedad de factores pueden modificar la
tasa del metabolismo del alcohol. El aumento de la temperatura corporal durante
la tarde, asociado con el ciclo diario, acelera el metabolismo del alcohol. El
ejercicio físico tiene una influencia insignificante sobre la aceleración del
metabolismo del alcohol, más vinculado con la elevación de la temperatura
corporal. La juventud es un factor que reduce la velocidad del metabolismo del
alcohol debido a una expresión menor de ADH y CYP450. La isoforma
ADH Beta 3 se caracteriza por una eficiencia más elevada del metabolismo del
alcohol en comparación con otras isoformas. Cederbaum y colaboradores observaron una mayor prevalencia
de la isoforma ADH Beta 3 entre los individuos
afroamericanos (15%), y menos frecuente entre las personas japonesas,
sudamericanas (excepto poblaciones indígenas) y europeas. La prevalencia de la isoforma ADH Beta 3 en este grupo determina la tasa de
metabolismo del alcohol y el riesgo de complicaciones relacionada con el
alcohol. (10) De acuerdo al menor contenido de
agua corporal en comparación con los hombres, las mujeres son más sensibles a
los efectos tóxicos del alcohol. Otros factores que tienen impacto sobre el
metabolismo del alcohol son el nivel de nutrición y la exposición a otras
drogas como la nicotina, cannabinoides y cocaína. (11,12)
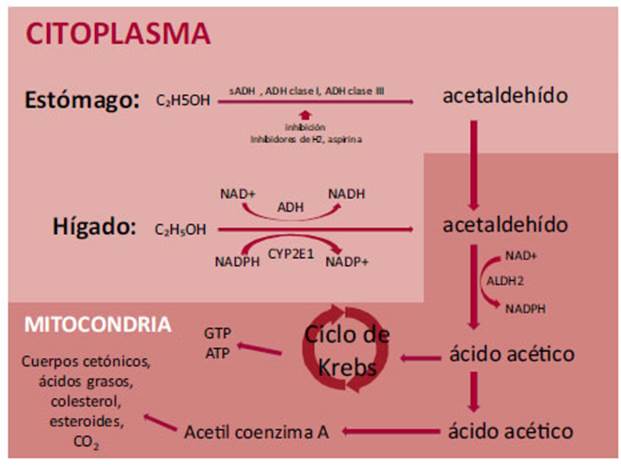
Fig. 2. Diagrama que ilustra el
metabolismo del alcohol en las células del estómago e hígado. σADH: Isoforma
sigma de alcohol-deshidrogenasa. ADH clase 1: Alcohol-deshidrogenasa clase uno.
ADH clase 3: Alcohol-deshidrogenasa clase tres. ATP: Adenosin
trifosfato. CYP2E1: Citocromo P450 2E1. ALDH2:
Aldehído deshidrogenasa mitocondrial 2/acetaldehído oxidasa. C2H5OH: etanol. CO2: dióxido
de carbono. GTP: Guanosin trifosfato.
H2: receptor de histamina tipo 2. NAD+: nicotinamida
adenina dinucleótido oxidada. NADP+: nicotinamida adenina dinucleótido
fosfato oxidada. NADH: nicotinamida adenina dinucleótido reducida. NADPH: nicotinamida
adenina dinucleótido fosfato reducida.
2.4. Influencia del
consumo de alcohol sobre el sistema cardiovascular
2.4.1. Primeros estudios
En 1861, Friedrich L. Goltz documentó la
relación entre la hipertrofia ventricular y el abuso persistente de alcohol.
Luego, en 1873, Walter H. Walshe, autor del texto
médico “El Diagnóstico Físico de las Enfermedades Pulmonares” implementó el
término “cirrosis cardíaca” para describir los fenómenos de fibrosis observados
simultáneamente tanto en el corazón como en el hígado de pacientes con
antecedentes de abuso alcohólico. (13,14) En
1884, en Munich, Otto von Bollinger
describió casos de “corazón de cerveza” (“Bierherz”)
y vinculó
esta observación a antecedentes de abuso de la cerveza, que alcanzaba hasta 432
litros de cerveza por año. En estudios histopatológicos, el “corazón de
cerveza” se caracteriza por hipotrofia, fibrosis y esteatosis. (15,16) A fines del siglo XIX Graham Steell
probó la relación entre la insuficiencia cardíaca y altas dosis de consumo
crónico de alcohol. (17) En 1969, se observó en
Quebec una serie de pacientes con miocardiopatía relacionada con el consumo de
cerveza. Todos los casos mencionados se notificaron en un período de siete
meses. Curiosamente, todos los pacientes consumieron cerveza derivada del mismo
origen, y el análisis de los ingredientes comprobó exceso de concentración de
cobalto (en esa época, el cobalto se aplicaba como estabilizador de la espuma
en la cerveza). (18) Los autores postularon al
alcohol y al cobalto como la etiología de la miocardiopatía en estos casos.
2.4.2 Dosis de alcohol cardiotóxica
Una
de las primeras comunicaciones que mencionan la relación entre la dosis de
alcohol y su impacto cardiotóxico fue publicada por Tadashi Koide y colaboradores en
1974. Los autores investigaron la asociación entre la dilatación ventricular
izquierda en radiografías de tórax y la dosis de alcohol consumido. El estudio
demostró que una dosis de etanol puro ≥125 mL
por día se relacionaba con un incremento del índice cardiotorácico (ICT)
>0,5. Se observaron valores de ICT más elevados en el 33% de los pacientes
que bebían ≥125 mL por día y en el 4% de los
pacientes que bebían entre 75 a 125 mL, así como en
2,9% de los pacientes que bebían <75 mL. Los
autores no mencionaron la duración del consumo en este grupo de pacientes. (19) Otros autores sugieren que las curvas en forma de J o
U pueden describir la relación entre la dosis de alcohol y el efecto deletéreo
sobre el corazón. (20) Por ejemplo, Ronksley y colaboradores, en un metaanálisis
que incluyó 84 estudios, reveló que beber 15-30 gramos de alcohol puro por día
tiene como resultado una disminución de la tasa de mortalidad cardiovascular [hazard ratio (HR) 0,66, IC95% 0,59-0,75] y también el grupo
que bebía 2,5- 14,9 gramos por día (HR 0,80, IC95% 0,74-0,87). La disminución
de la mortalidad por todas las causas se observó en el grupo de bebedores en comparación
con los totalmente abstemios (HR 0,87, IC95% 0,83-0,92). En este estudio, el
impacto negativo del alcohol (rama ascendente de la curva J) se observó en el
grupo que bebía 30-60 gramos de alcohol por día (HR 1,15, IC95% 0,98-1,35). (21)
En
los estudios que consideran el consumo crónico de alcohol y su relación con la
toxicidad cardíaca, la dosis de alcohol se expresa generalmente como la
cantidad de alcohol y la duración del alcoholismo. En la literatura, los
autores postulan como tóxica una dosis de 80 gramos de etanol puro bebida todos
los días durante 5 años. (22-25) Otros autores
proponen puntos de corte de 40 gramos por día, o en promedio 14 gramos por día
durante un mínimo de 10 años. (20,26)
2.4.3. Hipertensión inducida por el
alcohol
La
relación entre el consumo de alcohol y la elevación de la presión arterial
puede ser temporaria y terminar cuando se cesa de beber alcohol. (27) El efecto hipertensivo del alcohol parece ser
independiente del índice de masa corporal (IMC), el tabaquismo, la actividad
física y antecedentes de hipertensión arterial coexistente. (20)
Este efecto es provocado por diversos mecanismos: aumento de la actividad del
eje renina-angiotensina-aldosterona y del sistema nervioso simpático, aumento
de la secreción de cortisol, cambios en la sensibilidad de la insulina,
disfunción endotelial y reducción en la producción de óxido nítrico. (28) La modulación de la actividad del sistema nervioso
central luego de la exposición al alcohol es un motivo importante de la
elevación de la presión arterial. Los tractos nerviosos vulnerables al alcohol
son el bulbo raquídeo rostro-lateral ventral y el núcleo intermedio-lateral,
así como el reflejo baroreceptor, que pasa a través
del núcleo solitario y causa la reacción hipertensiva. (20)
Según las guías de Sociedad Europea de Cardiología para el manejo de la
hipertensión, no se recomienda una dosis de alcohol por encima de 14 unidades
de alcohol (UA) por semana (una UA contiene 10 gramos de etanol) en hombres y 8
UA por semanas en mujeres. (29) El aumento de la
dosis consumida tiene correlación con el riesgo de desarrollo de hipertensión
arterial. (28) Dicha relación es independiente del
sexo, pero en mujeres se puede observar a partir de una dosis de 2 UA por
semana. (30) En un metaanálisis
realizado por Roerecke y colaboradores, se observó
una reducción media de 5 mmHg en la presión sistólica
y de 4 mmHg en la presión diastólica en pacientes que
reducían la dosis de 6 UA por día a 0 UA. (31)
2.4.4. Miocardiopatía dilatada
La
prevalencia de miocardiopatía dilatada en el estudio realizado por Fernández Solá y colaboradores fue más alta entre los pacientes que
consumían alcohol en comparación con la población general, y alcanzó 0,43% en
hombres (cantidad media de alcohol puro consumido durante toda la vida: 30 ± 7
kg/kg de masa corporal durante un promedio de 29 ± 6 años), y 0,25% en mujeres
(cantidad media de alcohol puro consumido durante toda la vida: 17 ± 7 kg/kg de
masa corporal durante un promedio de 23 ± 7 años), mientras que en la población
general la prevalencia de miocardiopatía dilatada alcanza a 1:2500 individuos
(0,4‰). (32-34) En los países occidentales, el
abuso de alcohol es la principal causa de miocardiopatía no isquémica. En la
literatura, la tasa de abuso de alcohol estimada entre pacientes diagnosticados
con miocardiopatía dilatada oscila entre 3,8% y 47%. (23,35) Factores tales
como la malnutrición, el kwashiorkor, deficiencia de
vitaminas, electrolitos y microelementos (sodio,
potasio, calcio, magnesio, fósforo y selenio) así como la exposición a otros psicoestimulantes como cocaína, anfetaminas y nicotina,
incrementan el riesgo de la miocardiopatía alcohólica. (33,36)
No
existen signos típicos de miocardiopatía alcohólica. En forma similar a otras
etiologías de miocardiopatía dilatada, se encuentran presentes la atrofia miofibrilar, mitocondriopatías
(la diferenciación anormal de la forma y tamaño de las mitocondrias debido a la
exposición crónica a toxinas incluyendo el etanol, y la presencia de megamitocondrias), necrosis de cardiomiocitos
y fibrosis. (11,14) La exposición del músculo miocárdico
al alcohol en la matriz extracelular conduce a la activación de fibroblastos y
a la excesiva producción de colágeno tipo I. (37)
Asimismo, en fibroblastos expuestos al alcohol, se activan vías de señalización
proinflamatorias (los grupos de proteína MAPK
quinasa, el factor de transcripción STAT3 y el factor nuclear NF-κB) que provocan la liberación de citoquinas proinflamatorias del fibroblasto (IL-6, TNF-a, IL-1b,
IL-33) y la disfunción de cardiomiocitos. (37,38) Este proceso también lleva a una menor expresión
de genes que codifican proteínas contráctiles, como Acta 1, Actc1 (que codifica
la actina) y Myh7 (que codifica la cadena pesada alfa de miosina
y la miosina beta). Además, el alcohol ejerce una
influencia directa sobre los cardiomiocitos (mediada
por TNF-α, sin fibroblasto como mediador de la reacción), intensificando
los procesos que conducen a una disminución de la contractilidad de las fibras
musculares. (37)
El
acetaldehído es un metabolito del alcohol. Igual que el etanol, el acetaldehído
tiene un efecto negativo sobre el músculo cardíaco, pero la influencia de sus
propiedades cardiotóxicas es aún más potente que la
del alcohol. (33) Ambas moléculas tienen un
impacto directo sobre la síntesis de proteínas en los miocitos
y la peroxidación lipídica, reducen la contractilidad
de las miofibrillas y aumentan el estrés oxidativo. (33,39)
En estudios de resonancia magnética, Liu y
colaboradores observaron valores T1 nativos más cortos y mayor volumen
extracelular en el miocardio (similarmente a imágenes observadas en amiloidosis y sarcoidosis
cardíacas) de un grupo de pacientes que consumía >28 gramos de etanol por
día, durante un mínimo de 10 años, en comparación con un grupo control
(incluyendo personas que tomaban <100 gramos de alcohol por mes). Cambios
similares se perciben en resonancia magnética cuando se eleva el contenido de
moléculas de grasa en la célula. (26) Matyas y colaboradores observaron esteatosis cardíaca en
ratones expuestos a etanol en comparación con un grupo control que recibía una
dieta ajustada en calorías, pero sin la exposición a etanol. (40)
En
imágenes registradas mediante tomografía por emisión de positrones con acetato
marcado con carbono 11, se observó actividad metabólica del miocardio
disminuida en alcohólicos crónicos (promedio de 26 años) que consumían altas
dosis de alcohol (167 gramos de etanol puro por día) en comparación con
pacientes que bebían una menor cantidad de alcohol (50 gramos por día) durante
un período similar, lo que sugiere una disminución de la función mitocondrial
luego de la exposición crónica al alcohol. (26)
El
umbral de vulnerabilidad miocárdica al alcohol varía de persona en persona y no
ha sido claramente definido. La bibliografía sugiere que la sensibilidad
también puede ser determinada por genes. Se estima que los antecedentes
genéticos de susceptibilidad están presentes en 20% a 37% de los casos de
miocardiopatía dilatada. Actualmente, las posibles mutaciones relacionadas a la
miocardiopatía alcohólica se encuentran identificadas en más de 50 genes, (41) siendo mayoría los que codifican proteínas tales como
la titina, posterofilina-2, proteína C unida a miosina, desmoplaquina, receptor
de rianodina 2, desmocolina-2, desmogleína-2 y SCNSA.
(42) Ware y
colaboradores evaluaron el efecto de la presencia de genes relacionados a la
ocurrencia de miocardiopatía dilatada sobre la función cardíaca en pacientes
que consumían alcohol. El grupo consistió en 715 pacientes de 55±14 años y 70%
hombres. En el subgrupo con mutación de la titina (la
proteína humana más grande, crucial para la base molecular de la función
diastólica), el exceso de consumo de alcohol (>21 UA/ semana en hombres o
>14 UA/semana en mujeres) resultaba en una reducción del 8,7% de la fracción
de eyección ventricular izquierda (FEVI) (IC95% 2,3%- 15,1%; p=0,007), en
comparación con pacientes sin esta mutación. (43)
Las variantes del gen que codifica la titina,
asociadas con el desarrollo de miocardiopatía dilatada, fueron más prevalentes
en el grupo con miocardiopatía alcohólica en comparación con el grupo control.
En el grupo de pacientes con miocardiopatía alcohólica, se observó una
correlación entre la cantidad de consumo de alcohol y la disminución de la
FEVI. Esto significa que en individuos sensibles el alcohol también puede ser
un desencadenante en el proceso de desarrollo de miocardiopatía dilatada.
Asimismo, el hallazgo de una mayor prevalencia de mutaciones de genes de titina en el grupo con miocardiopatía alcohólica indica la
necesidad de la búsqueda activa de signos y síntomas de miocardiopatía entre
los familiares de pacientes con este diagnóstico. (44)
El
efecto tóxico de metabolitos del alcohol sobre el corazón resulta en remodelamiento ventricular izquierdo y derecho, dilatación
auricular, e insuficiencia secundaria mitral y tricuspídea.
(11) De acuerdo a la literatura, se postula que la
disfunción diastólica tiene lugar primero, seguida de la hipertrofia de la
pared ventricular izquierda, comparable a lo observado en la hipertensión
arterial. Asimismo, se observa un aumento del diámetro sistólico ventricular
izquierdo (DSVI) y del diámetro diastólico ventricular izquierdo (DDVI), que
tienen lugar en paralelo con la reducción de la FEVI. (11,25,33,45,46)
Los
datos disponibles actualmente sugieren que la exposición crónica al alcohol
también daña al ventrículo derecho. (47) En un
estudio de los efectos cardíacos de una única exposición al alcohol, Cali y
colaboradores observaron un grupo de 64 voluntarios (edad media 25 ± 4 años, 29
mujeres) antes y 60 minutos después del consumo de 0,5 gramos/kg de alcohol, y
lo compararon con un grupo control. La excursión sistólica del plano
del
anillo tricuspídeo (TAPSE) fue de 22,1 ± 3,3 en el
grupo de estudio y 24,0 ± 3,1 mm en el grupo control, p=0,003, y la presión
sistólica de la arteria pulmonar (PSAP) alcanzó 23,7 ± 3,2 mmHg
en el grupo expuesto vs. 20,2±4,9 mmHg en el control;
p = 0,0002. (48) Esta influencia del alcohol sobre
la función hemodinámica del ventrículo derecho puede estar relacionada con un
aumento de la resistencia de las arterias pulmonares debido a la
vasoconstricción provocada por leucotrienos liberados
de los leucocitos luego de la exposición al alcohol. (49)
Guzzo-Merello
y col. postularon que la falta de tratamiento betabloqueante, la existencia de
fibrilación auricular y el ensanchamiento del complejo QRS son predictores independientes
de peor pronóstico en la miocardiopatía alcohólica, con un incremento de la
incidencia de muerte y trasplante cardíacos. En los pacientes que redujeron su
ingesta alcohólica por debajo de 80 gramos por día, el riesgo de muerte
cardíaca o trasplante durante 59 meses de seguimiento se redujo a un nivel
comparable al de la población general. (23) La
falta de abstinencia en los pacientes con miocardiopatía dilatada relacionada
al alcohol resultó en alta mortalidad, alcanzando 50% en 4 años, lo que
posiciona a la miocardiopatía alcohólica cercanamente a los pacientes con
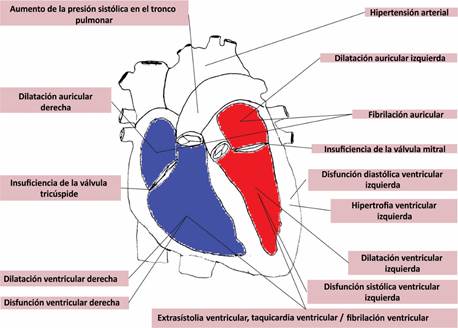
diagnóstico de cáncer. (50) Los efectos pleiotrópicos del alcohol sobre el corazón se muestran
esquemáticamente en la Figura 3.
Fig.
3.
Efectos pleiotrópicos de la cardiotoxicidad
alcohólica
Debido
a que el problema clave para el diagnóstico temprano de miocardiopatía alcohólica
puede ser el uso de métodos diagnósticos adecuados, vale la pena mencionar el
potencial poco utilizado todavía de los protocolos adaptados a la
ecocardiografía de estrés en la detección temprana de disfunción diastólica,
así como de hipertensión pulmonar. (51) Vriz y colaboradores realizaron ecocardiografía Doppler de ejercicio en un grupo de 155 pacientes
hipertensos y en 145 sujetos normales, y documentaron que la TAPSE durante el
ejercicio era menor en el grupo hipertenso mientras que la PSAP, así como su
valor indexado al volumen minuto alcanzado durante el ejercicio, era mayor. (52)
En
un análisis llevado a cabo recientemente por nuestro grupo, la mediana y el
rango intercuartilo (RIC) de la masa ventricular
izquierda fue de 119 (91- 155) g/m2 en
pacientes que bebían alcohol [mediana 30 (11-51) UA por semana] vs. 93 (75-110)
g/m2 en un
grupo control que bebía hasta 2 UA por semana, (p = 0,008); y el espesor
parietal relativo en el grupo alcohólico fue de 0,5 (0,4-0,6) vs. 0,4 (0,4-0,4)
en los controles; p = 0,001. En el mismo estudio, el strain
longitudinal global (SLG) y los strain
específicos de las capas del corazón mostraron valores absolutos menores en el
grupo con abuso de alcohol en comparación con los controles. Todos los
parámetros con strain anormales estuvieron asociados
con una mayor incidencia de un punto final combinado (mayor riesgo clínico de
muerte o internación cardiovascular). Los mejores valores de corte predictivos
fueron un SLG <18%, strain de la
capa endocárdica <19% y de la capa epicárdica <15%. (53)
2.4.5. Arritmias relacionadas con el
alcohol
La
fibrilación auricular (FA) es la arritmia más común observada entre las
personas que abusan del alcohol. Larsson y col.
probaron que durante la exposición crónica al alcohol un incremento de consumo
de 1 UA por día aumenta el riesgo de FA en un 8%. (54)
Más a menudo, las arritmias se observan como consecuencia de la ingesta de una
única dosis alta de alcohol en un tiempo breve, y numerosos autores han
mencionado esto como “síndrome del corazón en vacaciones”. Este síndrome fue
descripto por primera vez por Ettinger y
colaboradores en 1978. (55, 56) El consumo crónico
de alcohol se asocia positivamente con un aumento del riesgo de FA en el
seguimiento a largo plazo. En el estudio realizado por Larsson
y colaboradores (con 12 años de seguimiento), el RR (IC95%) de FA para 7-14 UA/
semana fue de 1,12 (1,02-1,23), y para >21 UA/semana de 1,43 (1,25-1,65) en
comparación con los controles. (54) Las arritmias
se observan más frecuentemente en pacientes diagnosticados con miocardiopatías
más que en aquellos sin anomalías estructurales. Asimismo, los episodios de
abstinencia pueden ser desencadenantes de arritmia en pacientes con abuso de
alcohol crónico, debido al aumento de la actividad adrenérgica observada al comienzo
de la abstinencia y las deficiencias simultáneas de macro y micronutrientes
(sodio, potasio, magnesio, calcio, fósforo, selenio) y vitaminas (tiamina)
asociadas al abuso de alcohol previo. (33,57,58)
2.4.6. Miocardiopatía cirrótica
Los
trastornos observados en el síndrome hepato-cardíaco
también pueden contribuir a la patogénesis de la miocardiopatía alcohólica. (59) La función sistólica está disminuida tanto en reposo
como durante el estrés, y esta alteración está asociada con una disminución de
la actividad de los receptores b1 a través de la reducción en la expresión de
la proteína G en el citosol, relacionada a disfunción
hepática. (59-61) Paralelamente, se observa disfunción
diastólica en relación con hipertrofia ventricular izquierda, fibrosis y
disfunción endotelial. (59,62) Los factores
mencionados conducen a una mayor frecuencia cardíaca secundaria y aumento del
volumen minuto, dando como resultado una taquimiocardiopatía . Los criterios diagnósticos de la miocardiopatía cirrótica
se establecieron en 2005 durante el Congreso Mundial de Gastroenterología y se
describen en la Tabla 1. (59,63)
Tabla
1.
Criterios diagnósticos de la Miocardiopatía Cirrótica - Congreso Mundial de
Gastroenterología 2005
|
Definición: Disfunción en pacientes con cirrosis caracterizada por
respuesta contráctil disminuida al stress y/o relajación diastólica alterada con
anomalías electrofisiológicas en ausencia de otras enfermedades cardíacas
conocidas |
|
|
Disfunción
diastólica (una con lo mencionado arriba |
-Relación E/A <1,0 (corregida por edad) -Tiempo de desaceleración prolongado (>200 ms) -Tiempo de
relajación isovolumétrica prolongado (>80 ms) (18) |
|
Criterios de
apoyo |
- Reacción
cronotrópica inadecuada al ejercicio, evaluada durante un tilt test cuando la
frecuencia cardíaca es >22% en pacientes en clase B y >17% en pacientes
en clase C de Child-Pugh (64) |
FEVI: fracción de eyección ventricular izquierda BNP:
péptido natriurético B NT-proBNP:
fragmento amino terminal del péptido B
Declaración
de conflicto de intereses
Los autores declaran que no tienen
conflicto de intereses
(Véanse formularios de conflicto de
intereses de los autores en la web/Material suplementario).