http://dx.doi.org/10.7775/rac.es.v91.i1.20606
ARTÍCULO
ORIGINAL
Autotrasplante
cardíaco como estrategia de tratamiento de tumores malignos de corazón
Los tumores cardíacos primarios malignos, por lo general sarcomas,
representan un subgrupo poco frecuente dentro de las masas cardíacas. Sin
embargo, constituyen procesos de mal pronóstico, y el tratamiento quirúrgico es
la alternativa terapéutica más favorable en términos de supervivencia.
La literatura sobre sarcomas cardíacos alojados en cavidades
izquierdas pone de manifiesto que los pacientes son sometidos a reintervenciones por recurrencia local, en general
relacionadas con resecciones incompletas, probablemente debidas a una
exposición anatómica subóptima durante la cirugía, lo
cual condiciona resecciones inadecuadas y reconstrucciones técnicamente dificultosas.
En ocasiones, para cumplir con los objetivos de una resección
oncológica radical y facilitar la reconstrucción de las estructuras cardíacas
resecadas, se debe recurrir al explante del corazón
para resecar el tumor con adecuados márgenes y reconstruir las cavidades o
estructuras involucradas, reimplantando finalmente el corazón tratado en la
cirugía de banco (autotrasplante cardíaco).
Se presenta una paciente de 73 años, sexo femenino, sin
antecedentes clínicos de relevancia que se internó por cuadro de disnea
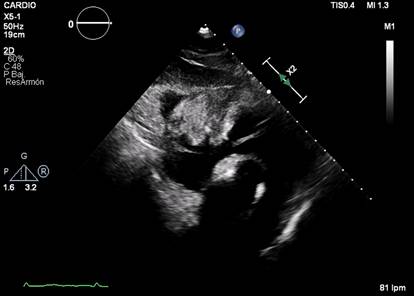
progresiva y anemia. En el algoritmo diagnóstico se objetivó en el
ecocardiograma transtorácico: aurícula izquierda
dilatada ocupada por masa heterogénea, no móvil con íntima relación al anillo
mitral que ocupa por completo la orejuela izquierda de 4,8 cm × 2,8 cm, e
insuficiencia mitral grave con jet central.
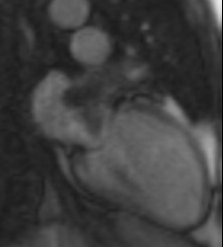
Para completar la evaluación de la masa se realizó una resonancia
magnética cardíaca que evidenció el mencionado tumor con aspecto heterogéneo en
secuencias potenciadas de T1 y T2, pre y post contraste, así como en las
secuencias de perfusión y realce tardío. No se evidenció captación de contraste
en el sector del tumor que protruye a la aurícula izquierda, lo que se
interpretó como componente trombótico agregado (Figura 1). El mismo estudio evidenció ausencia de compromiso del pericardio
y venas pulmonares. Se inició anticoagulación profiláctica y se realizó
tomografía por emisión de positrones/tomografía computarizada (PET-TC) de
cuerpo entero para evaluación local y búsqueda de eventuales metástasis.
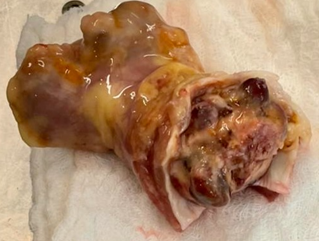
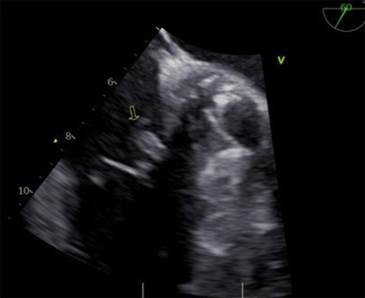
Fig. 1. A. Resonancia magnética nuclear: sarcoma de aurícula izquierda
alojado en la orejuela. B. Pieza operatoria con resección completa de la
lesión. Se evidencian márgenes de resección sobre tejido no comprometido por
tumor
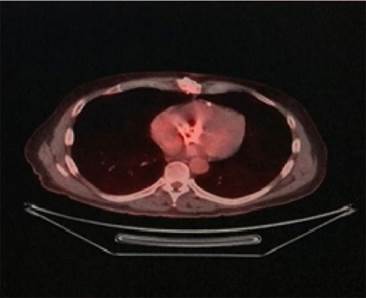
La PET evidenció masa hipermetabólica de
5,9 cm × 3,4 cm × 2,4 cm (SUV 8,5) en la ubicación ya conocida, lesiones
focales hepáticas compatibles con hemosiderosis y
ausencia de secundarismos.
Debido a la condición y características clínicas de la paciente,
la estadificación de la enfermedad y su pronóstico
sin resección, se decidió tratamiento quirúrgico. En virtud de la localización
de la lesión a resecar, en intimo contacto con el anillo mitral, la arteria circunfleja y el seno coronario, se infirió la posibilidad
de que, para realizar una resección oncológica adecuada, se debiera recurrir a explante del corazón y reconstrucción en banco (ex situ)
con posterior autotrasplante.
En cirugía, se realizó esternotomía
mediana, canulación de ambas cavas y aorta.
Se exploró el tumor ingresando a la aurícula izquierda por el
surco interauricular, como habitualmente se realiza para un procedimiento sobre
la válvula mitral. Se constató ausencia de compromiso de las venas pulmonares
y crecimiento tumoral hasta la vecindad del anillo mitral.
Al tener en cuenta que la resección oncológica comprendería
resecar el anillo y parte de la válvula mitral y ante la dificultad para
definir, por el mencionado abordaje, el límite externo de la resección en
relación con estructuras del surco auriculoventricular,
se decidió explantar el corazón y se resecó el tumor
en banco.
Se seccionaron las venas cavas, aorta y arteria pulmonar, y se
extendió la atriotomia dejando un casquete que
contenía las venas pulmonares. Se resecó el tumor ex situ (cirugía de
banco), lo cual implicó resecar un sector del anillo mitral a nivel de P1
dejando expuestos los vasos del surco auriculoventricular
y el miocardio ventricular. Se reconstruyó el anillo mitral y la aurícula izquierda
con parche de pericardio bovino y se reemplazó la válvula mitral con prótesis
biológica porcina # 25.
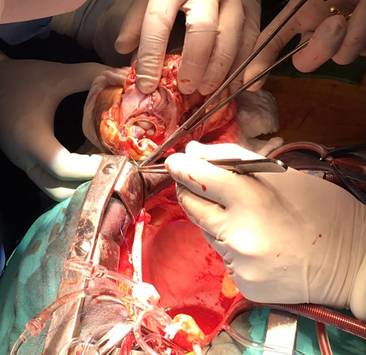
Se reimplantó el órgano con técnica de autotrasplante (Figura 2)
Fig. 2.
Autotrasplante cardíaco: se observa la aurícula izquierda reparada con
pericardio bovino y prótesis mitral
El tiempo de circulación extracorpórea fue de 232 minutos y el de clampeo de 175 min. El curso postoperatorio fue acorde a
la envergadura del procedimiento, y se requirió inotrópicos por 72 hs. Entre otras intercurrencias
la paciente presentó un episodio de aleteo auricular que se controló con amiodarona y registros subfebriles aislados con cultivos
negativos.
La anatomía patológica informó sarcoma pleomórfico
indiferenciado grado III, lo cual implica un nivel máximo de malignidad e
indiferenciación.
La prevalencia de tumores cardíacos primarios en series de
autopsia es del 0,02%; el 25% de ellos son malignos, de los cuales el 75% son
sarcomas. (1) La mediana de supervivencia en las series publicadas oscila entre
9 y 33 meses. (2) La mayoría son clínicamente silentes hasta un estadio avanzado y,
a menudo, se consideran irresecables debido a la
proximidad a estructuras críticas. Sin embargo, las
técnicas quirúrgicas y de imágenes han mejorado dando lugar a intervenciones
más agresivas, que apuntar a lograr una resección microscópicamente negativa
(R0), situación en la que existe un claro beneficio de supervivencia. (3)
El
autotrasplante cardíaco es un procedimiento descripto hace años, para la
resección de tumores de difícil abordaje o de manejo intraoperatorio
complejo. (4)
Con
el paso del tiempo, la técnica se reprodujo para el manejo de esta patología en
múltiples pacientes (5),
y mejoraron los resultados iniciales en términos de calidad de la resección
oncológica y en supervivencia. (6)
Con
adecuado entrenamiento quirúrgico la técnica es reproducible y debería
considerarse una alternativa de valor en el arsenal terapéutico a fin de
ofrecer oportunidades a pacientes con patología oncológica grave y mal
pronóstico sin cirugía.
Declaración de conflicto de
intereses
Los autores declaran que no tienen
conflicto de intereses
(Véanse formularios de conflicto de
intereses de los autores en la web/Material suplementario).
Ricardo G. Marenchino1, Edgar F.
Montalvo1,
Juan C. Climente1,
Diego E. Pinto1, Alejandra
Ferro2,
María E. González3
1 Servicio de Cirugía Cardiovascular -
Hospital Privado de Comunidad
2 Servicio de Cardiología - Hospital Privado
de Comunidad
3 Servicio de Cuidados Intensivos - Hospital
Privado de Comunidad
Dirección para separatas: Ricardo G.
Marenchino - Córdoba 4545 CP: B7602CBM Mar del Plata
- Provincia de Buenos Aires - Argentina - Tel: + 54223-4990000 - E-mail:
rmarenchino@gmail.com
1. Burazor I, Aviel-Ronen S, Imazio M, Markel G, Grossman Y, Yosepovich
A, et al. Primary malignancies of the heart and pericardium. Clin Cardiol 2014;37:582-8. https://doi.org/10.1002/clc.22295
2. Chen TW,
Loong HH, Srikanthan A.
Primary cardiac sarcomas: a multinational retrospective review. Cancer Med 2019;8:104-10. https://doi.org/10.1002/cam4.1897
3. Putnam
JB Jr, Sweeney MS, Colon R. Primary cardiac sarcomas. Ann Thorac
Surg. 1991;51:906-10. https://doi.org/10.1016/0003-4975(91)91003-E
4. Cooley
D, Reardon M, Fraizer O, Angelini
P. Human Cardiac Explantation and Autotrasnplantation: Application in a Patient with a Large
Cardiac Pheocromocytoma. Tex Heart Inst J 1985;2:171-6.
5. Ranlawi B, Al-Jabbari O, Blau L, Davies M, Bruckner B, Blackmon S et al. Autotransplantation for the resection of complex left heart
tumors. Ann Thorac Surg
2014;98:863-8. https://doi.org/10.1016/j.
athoracsur.2014.04.125
6. Hassan
S, Witten J, Collier P, Tong M, Petterson G, Smedira N, et al. Outcomes after resection of primary
cardiac sarcoma. JTCVS Open 2021;8:384-90. https://doi.org/10.1016/j.xjon.2021.08.038
http://dx.doi.org/10.7775/rac.es.v91.i1.20603
Masa
compresiva en el pericardio anterior: la dificultad del diagnóstico diferencial
Presentamos
el caso de un varón de 79 años, fumador, hipertenso, portador de diabetes tipo
2, con un síndrome coronario crónico con revascularización quirúrgica en 2009,
y un adenocarcinoma de próstata en control por Urología mediante vigilancia
activa. El paciente fue derivado a Urgencias por disnea de moderados esfuerzos
de tres semanas de evolución y el hallazgo de un derrame pleural derecho en una
radiografía de tórax. A su llegada, se encontraba hemodinámicamente
estable (tensión arterial 153/93 mmHg, frecuencia
cardiaca 99 lpm) y con una saturación de oxígeno a
aire ambiente del 89%, pero sin taquipnea en reposo. En la exploración física
destacaban una ingurgitación yugular hasta el tercio medio del músculo
esternocleidomastoideo, la abolición del murmullo vesicular en la base pulmonar
derecha, y edemas bilaterales con fóvea hasta ambas rodillas.
El
electrocardiograma (ECG) mostraba ritmo sinusal, a 89
lpm con ondas T negativas de V1-V4, ya presentes en
estudios previos. En la analítica se objetivó función renal normal (urea 31 mg/dL, creatinina 0,77 mg/dL, tasa
de filtración glomerular 86 ml/ min/1,73 m2)
con todos los iones en rango, proteína C reactiva 25,98 mg/L, lactato
deshidrogenasa 950 U/L, creatinina kinasa 55 U/L, NT-proBNP 950 pg./mL, troponina T ultrasensible 25 ng/L,
hemoglobina 11,2 g/dL, 335000 plaquetas, 11430
leucocitos, dímero D 4860 ng/mL.
Para completar el diagnóstico, se realizó una tomografía computarizada (TC) no
sincronizada en la que se describía una lesión hipodensa
localizada sobre las cavidades cardiacas derechas (Figura
1). Como primera posibilidad diagnóstica se
planteó un hemopericardio por rotura cardíaca o
dehiscencia del bypass, siendo probable también el diagnóstico de una
neoplasia. Ante estos hallazgos, se solicitó valoración por Cardiología. En el
ecocardiograma (ETT) se objetivó una masa sólida y heterogénea en el saco
pericárdico anterior, con adherencias en las cavidades derechas y compresión
del surco auriculoventricular derecho, que no captaba
contraste ecocardiográfico (Figura
2). El cuadro no impresionaba una rotura
cardíaca, no solo por los hallazgos ecocardiográficos,
también porque no había presentado dolor torácico ni alteraciones sugestivas de
isquemia aguda en el ECG, y se encontraba hemodinámicamente
estable, lo que, a su vez, hacía poco probable la dehiscencia del bypass.
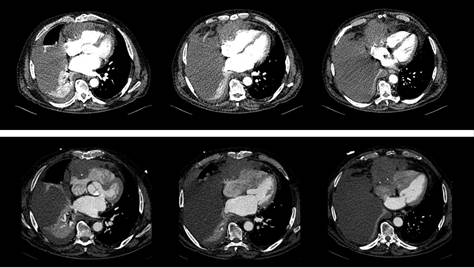
Fig. 1.
Tomografía computarizada (TC). Arriba: TC no sincronizada, con una lesión hipodensa localizada sobre las cavidades cardiacas derechas
y un derrame pleural derecho grave con atelectasias asociadas. Abajo: TC
sincronizada, con una masa pre-cardiaca derecha de 8,5 × 10 cm, que realza tras
la administración de contraste. La masa ejerce efecto masa y posiblemente
infiltra la aurícula derecha, se encuentra en contacto con dudosa infiltración
del ventrículo derecho y contacta con la pared torácica anterior.
Fig. 2.
Ecocardiograma transtorácico, acceso subcostal. Masa
de aspecto sólido y heterogéneo en el saco pericárdico anterior que comprime el
surco auriculoventricular y parece que se adhiere a
la pared ventricular.
Dada
la discordancia, se decidió realizar una TC sincronizada para una mejor
caracterización de la lesión, que mostró una masa pre-cardíaca derecha de 8,5 ×
10 cm, de aparente dependencia pericárdica y que mostraba realce tras la
administración de contraste intravenoso (Figura
1). Estos hallazgos planteaban el
diagnóstico diferencial con metástasis o una neoplasia pericárdica primaria.
El
diagnóstico diferencial de las masas mediastínicas se
basa principalmente en la localización de la masa, su composición y la edad del
paciente. (1)
Las diferentes técnicas radiológicas, incluyendo TC y resonancia magnética
cardíaca (RMC) resultan de gran utilidad en el diagnóstico. Teniendo en cuenta
la localización de la lesión, anterior al corazón y que llegaba a contactar con
la pared torácica anterior, se planteó un amplio diagnóstico diferencial que
incluía tanto las diferentes lesiones que se pueden presentar a nivel del
mediastino anterior como las masas dependientes del tejido pericárdico.
Los
timomas se presentan como una masa ovalada,
homogénea, de contornos bien definidos en la TC, a diferencia de lo que ocurría
en nuestro paciente. El bocio tiroideo y los teratomas suelen acompañarse de
calcificaciones o áreas quísticas, (1,2)
y teniendo en cuenta que los hallazgos de la TC de nuestro caso no mostraban
calcificaciones, estas dos últimas entidades parecían poco probables. Los
linfomas representan el 20% de los tumores mediastínicos
en los adultos, y los linfomas de Hodgkin son el
subtipo más frecuente. (1-3)
Dentro de este último grupo, el linfoma B mediastínico
de células grandes constituye una entidad independiente dentro de la
clasificación de neoplasias linfoides malignas, con una frecuencia estimada en
torno a un 2-3% de los linfomas no Hodgkin y entre un
6-10% de los linfomas de células B grandes. Este tumor suele presentarse como
una masa mediastínica de expansión rápida y puede
asociarse a derrame pleural y pericárdico. (4,5)
El
paciente ingresó en planta de Cardiología para completar el estudio. Se realizó
una toracocentesis guiada por ecografía del derrame
pleural, y se obtuvo un líquido serohemático
compatible con un exudado según los criterios de Light, que mostraba en el
estudio citológico una extensión hipercelular de
características compatibles con un proceso linfoproliferativo
B. Para completar el estudio se practicó una biopsia de aguja gruesa de la masa
mediastínica y se confirmó el diagnóstico de linfoma
B de células grandes primario mediastínico.
Finalmente se inició el primer ciclo del tratamiento quimioterápico
con rituximab, ciclofosfamida,
doxorrubicina liposómica no
pegilada, vincristina y prednisolona. Tras cuatro ciclos de tratamiento, presentó
remisión parcial objetivada mediante TC, y tras completar los seis ciclos de
quimioterapia, en la tomografía por emisión de positrones se observó una
remisión metabólica completa. Durante el seguimiento el paciente ha presentado
una buena situación clínica, y en el último control se decidió retirar el
reservorio.
Este
caso clínico ilustra la importancia de realizar un diagnóstico diferencial
adecuado de las masas mediastínicas, ya que algunas
de estas tienen un tratamiento curativo, y la utilidad del diagnóstico multimodal
de imagen para poder realizar una adecuada caracterización de algunas lesiones
Declaración
de conflicto de intereses
Los
autores declaran que no tienen conflicto de intereses
(Véanse
formularios de conflicto de intereses de los autores en la web/Material
suplementario).
Uxue Idiazabal
Rodriguez1, Adrián
Costa Santos1,
Lara Ruiz Gómez2, Alain Laskibar Asua1, Iván Cano González1, Ana Ruiz Rodríguez1
1
Hospital
Universitario Basurto: Servicio de Cardiología, planta de hospitalización. Osakidetza. Bilbao, España.
2
Hospital
Universitario Basurto: Servicio de Cardiología, sección de Imagen Cardiaca. Osakidetza. Bilbao, España.
Dirección para separatas: Uxue Idiazabal Rodriguez. Correo
electrónico: uxue_278@hotmail.com
BIBLIOGRAFÍA
1. Prosch H, Röhrich S, Tekin ZN, Ebner L. The role of
radiological imaging for masses in the prevascular
mediastinum in clinical practice. J Thorac Dis 2020;12:7591-7. https://doi.org/10.21037/jtd-20-964
2. Nakazono T, Yamaguchi K, Egashira
R, Mizuguchi M, Irie H.
Anterior mediastinal lesions: CT and MRI features and differential diagnosis. Jpn J Radiol 2021;39:101-17. https://doi.org/10.1007/s11604-020-01031-2
3. Pfau D, Smith DA, Beck R, Gilani KA, Gupta A, Caimi P. Primary Mediastinal Large B-Cell Lymphoma: A
Review for Radiologists. AJR Am J Roentgenol 2019;213:W194-W210.
https://doi.org/10.2214/AJR.19.21225
4. Lees C,
Keane C, Gandhi MK, Gunawardana J. Biology and
therapy of primary mediastinal B-cell lymphoma: current status and future
directions. Br J Haematol 2019;185:25-41.
https://doi.org/10.1111/bjh.15778
5. Martelli M, Ferreri A, Di Rocco
A, Ansuinelli M, Johnson PW. Primary mediastinal
large B-cell lymphoma. Crit Rev Oncol
Hematol 2017;113:318-27. https://doi.org/10.1016/j.critrevonc.2017.01.009
http://dx.doi.org/10.7775/rac.es.v91.i1.20604
Endocarditis
infecciosa de válvula tricúspide nativa
Al
Director:
La
endocarditis infecciosa derecha es poco habitual, pero con capacidad de ser
mortal. Representa 5-10% de todos los casos. Está asociada la mayoría de las
veces al uso de drogas intravenosas, se presenta con menor frecuencia en
pacientes con acceso venoso, dispositivos intravasculares
o cardiopatías congénitas de base, y excepcionalmente en pacientes no adictos
ni con malformaciones cardíacas. (1)
Presentamos
el caso de un paciente masculino de 58 años con hipertensión arterial y dislipidemia, y el antecedente de cirugía de reemplazo de
la válvula aortica con prótesis mecánica por estenosis aortica en 2019.
Es
ingresado a sala general por síndrome febril en estudio. Al examen físico
cardiovascular no se detecta alteración en los ruidos cardíacos, ni signos de
insuficiencia cardiaca congestiva. En el ECG: taquicardia sinusal
y bloqueo aurículo ventricular de primer grado (PR
220 mseg).
En
la analítica de ingreso se destacan: leucocitos 31 840/mm3 (neutrófilos
96%, linfocitos 1,7%), proteína C reactiva 58,9 mg/L (rango normal 0-5), procalcitonina 4,55 ng/mL (rango normal 0-0,1), bilirrubina total 1,33 mg/dL, indirecta 0,83 mg/dL, y
directa 0,50 mg/dL.
Durante
la internación se detecta en hemocultivos Staphilococcus
Aureus metilicilino
sensible. Por sospecha de endocarditis infecciosa se realiza ecocardiograma transesofágico, en donde no se detectan vegetaciones y la
válvula mecánica es normofuncionante. Al cuarto día
de antibióticos se toman nuevos hemocultivos, sin desarrollo de crecimiento
bacteriano, y al décimo día se realiza nuevamente ecocardiograma transesofágico, sin observarse vegetaciones en válvulas
cardiacas, razón por la cual se descarta endocarditis infecciosa. El paciente
cumple 14 días de antibióticos endovenosos y posteriormente recibe el alta.
A
la semana reingresa por fiebre y decaimiento general; se constata mayor
prolongación del intervalo PR en el ECG, de 270 mseg
(Figura 1A).
En la analítica: leucocitos 11 870/mm3 (neutrófilos
87%, linfocitos 4,7%), proteína C reactiva 25,6 mg/L, procalcitonina
0,19 ng/mL, eritrosedimentación 32 mm/h. Se toman nuevos hemocultivos,
donde se aísla Staphilococcus Aureus metilicilino sensible.
Se realiza ecocardiografía transtorácica, que revela
imagen con movilidad independiente a nivel de la válvula tricúspide, de 0,6 cm
x 0,6 cm. Se corrobora en el ecocardiograma transesofágico
(ETE) una vegetación de 0,9 cm por 0,6 cm a nivel de la valva septal, insuficiencia tricuspídea
leve y válvula protésica normofuncionante (Figura 2).
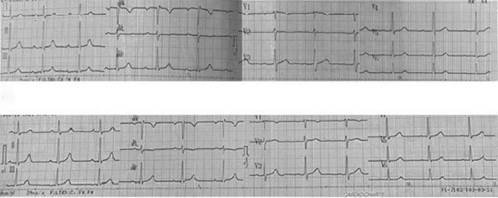
Fig. 1.
A. ECG: PR prolongado (270 msg). B. ECG: PR normal (200 msg)
Fig. 2. ETE:
Vista 60° se observa vegetación en valva septal tricuspidea
Se
decide tratamiento conservador con cefazolina
endovenosa por 6 semanas. El bloqueo AV de primer grado mejora a la quinta
semana de antibiótico (Figura
1B). Se efectúa ecocardiograma transtorácico de control a la segunda y sexta semana de
tratamiento, que no evidencia vegetación en la válvula tricúspide.
Por
sospecha de afectación de la válvula protésica se realiza de forma ambulatoria
tomografía por emisión de positrones/tomografía computarizada (PET /TC) que
evidencia moderada captación difusa del radiotrazador
en la topografía del reemplazo valvular aórtico, lo cual en ausencia de foco hipercaptante dominante y SUV max
3,5 sugiere ausencia de proceso infeccioso activo (Figura
3).
Fig. 3. PET/TC con flúor-18- desoxiglucosa:
proyección transversa. Se aprecia captación difusa en la prótesis aórtica
La
endocarditis infecciosa derecha es usual en adictos a drogas de uso parenteral y
malformaciones cardiacas; es una patología potencialmente grave, con una
mortalidad que fluctúa entre el 23 y el 31 %. La endocarditis izquierda y
derecha, simultánea, se presentan en un 13%, y la derecha por sí sola en un
10%. (1,2)
La
endocarditis de la válvula tricúspide nativa aislada (EITNA) suele darse de
forma espontánea, sin un precedente evidente de procedimientos dentales o
quirúrgicos; sin embargo, la piel suele ser la puerta de entrada más frecuente
(sobre todo en el caso de S. Aureus). En este
caso clínico no se pudo identificar el factor predisponente. El agente
infeccioso más frecuentemente aislado es Staphylococcus
aureus (70% de los casos), seguidos por Streptococcus y Enterococcus.
(3)
En
relación con la presentación clínica, constantemente aparece fiebre
persistente ligada a fenómenos pulmonares, anemia y microhematuria
(síndrome tricuspídeo de Nandakumar
y Raju). Además, se resalta la ausencia de estigmas
periféricos de endocarditis y de soplos cardíacos destacables en la mayoría de
los pacientes. (4)
Si
la fiebre es prolongada (si permanece luego de 2 semanas de tratamiento
antibiótico adecuado) suele asociarse a extensión perivalvular
de la infección, a nuevas embolizaciones sépticas o a
infección nosocomial sobreagregada. El cuadro
clínico, la positividad en los hemocultivos y la ecocardiografía, son los
instrumentos diagnósticos fundamentales en la EITNA. (4)
La
utilidad de la PET/TC es relevantemente mayor en la endocarditis de válvula
protésica que en la endocarditis infecciosa de válvula nativa, y es una
excelente alternativa, en caso de estudios ecográficos negativos o dudosos. La
integración de la PET/TC como una herramienta diagnóstica en la endocarditis,
permite reclasificar al 76% de los pacientes con endocarditis infecciosa
válvula protésica de “posible” a “definitiva” (5)
En
lo referente al tratamiento, el 80 % de pacientes con EITNA consiguen ser
tratados de manera exitosa con terapia médica. Sin embargo, se aconseja
realizar cirugía en casos de infección no controlada o insuficiencia cardíaca
derecha con insuficiencia tricúspidea refractaria al
tratamiento. El tratamiento quirúrgico repara la disfunción valvular y elimina
el foco infeccioso, razón
por la cual su aporte es valioso para disminuir la mortalidad asociada a la
insuficiencia cardíaca (6)
En relación con el pronóstico con el tratamiento médico
(antibiótico) se consigue una elevada tasa de éxito, la instauración de la
insuficiencia cardíaca es infrecuente y solo el 25% de los casos precisan recambio
valvular o cirugía. (1). La mortalidad en la EITNA es menor que la declarada para la
endocarditis con condición predisponente. (6)
Este caso nos indica la necesidad de tener en cuenta la EITNA, su
presentación clínica, tratamiento y pronostico, así como la utilidad del PET/TC
para confirmar la afectación valvular protésica.
Declaración de conflicto de intereses
Los autores declaran que no presentan conflicto de intereses.
(Véanse formularios de conflicto de intereses de los autores en la
web/ Material suplementario).
Consideraciones éticas
No aplican
Mauricio Tituana1,
Diana Tituana1, Ramiro Ayala1,
Gabriel Quiroga1,
Andrea Trevisán1,
Luis Mantilla1
Dirección para
separatas: Servicio de Cardiología. Sanatorio Adventista del Plata, Entre
Ríos, Argentina - E-mail: manu2792@hotmail.com
1. Zaldívar AÁ, Cardoso AA, Ramon RD. Endocarditis Infecciosa Derecha. Presentación de
un caso. Rev Cub Cardiol Cirug Cardiovasc
2019;25(4).
2. Pérez Domínguez JA, Aguilar
Almaguer O, González Céspedes JC, Escandell Reyes A,
Leyva Castro R, Rodríguez Peña MM. Complicaciones sistémicas en endocarditis
infecciosa de válvula tricúspide. Multimed 2019;23:543-51.
3. Salamanca MA. Endocarditis tricuspídea secundaria a infección asociada a catéter
venoso central. Reporte de dos casos. In Anales de la Facultad de Medicina 2020;81:330-32. UNMSM. Facultad de Medicina.
4. Alkan
G, Emiroglu M, Sert A, Kartal A, Öc M. Endocarditis
infecciosa de la válvula tricúspide asociada con meningitis aséptica: presentación
infrecuente en una niña. Arch Argent Pediatr 2020:e22-e25.
5. Ladrón-de-Guevara H, Canelo L,
Bitar H, Ramón Soto J. Imágenes en endocarditis infecciosa: No todo es
ecocardiografía. Rev Chil infectol, 2021;38:260-70.
6. Álvarez F, Torrez J,
Galleguillos G, Saavedra J. Endocarditis infecciosa cámaras derechas. Reporte
de un caso. Rev Chil Anest 2021;50.